
| A. | 7.8gNa2O2與CO2反應,轉移的電子數為0.2NA | |
| B. | 1mol/L的CaCl2溶液中含Cl-的數目為2 NA | |
| C. | 常溫常壓下,17g NH3含氫原子數目為3NA | |
| D. | 1mol氫氧根離子中含有的電子數為9NA |
分析 A、求出過氧化鈉的物質的量,然后根據過氧化鈉與二氧化碳的反應為歧化反應來分析;
B、溶液體積不明確;
C、求出氨氣的物質的量,然后根據1mol氨氣中含3mol氫原子來分析;
D、氫氧根中含10個電子.
解答 解:A、7.8g過氧化鈉的物質的量為0.1mol,而過氧化鈉與二氧化碳的反應為歧化反應,故0.1mol過氧化鈉與二氧化碳反應轉移0.1mol電子即0.1NA個,故A錯誤;
B、溶液體積不明確,故溶液中的氯離子的個數無法計算,故B錯誤;
C、17g氨氣的物質的量為1mol,而1mol氨氣中含3mol氫原子,故為3NA個,故C正確;
D、氫氧根中含10個電子,故1mol氫氧根中含10mol電子即10NA個,故D錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
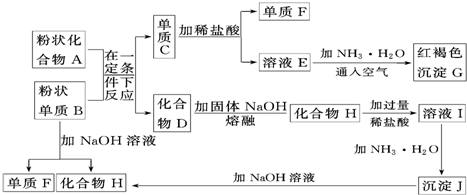
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
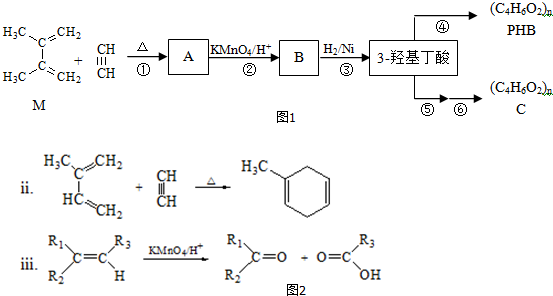
 .
. ;
;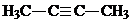 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25% | B. | 80% | C. | 10% | D. | 20% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電離時能夠產生H+的化合物是酸 | |
| B. | 難溶的物質(如CaCO3)不能發生離子反應 | |
| C. | 電解質在水中不一定能導電,在水中導電的化合物不一定是電解質 | |
| D. | 膠體加入電解質可產生沉淀,而溶液不能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液氨常被用作制冷劑 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蝕印刷電路板 | |
| C. | 為便于儲存和使用,可用液氯代替氯水漂白干燥棉布上的有色物質為便于儲存和使用,可用液氯代替氯水漂白干燥棉布上的有色物質 | |
| D. | 已知3Cl2+2NH3═N2+6HCl,工業上可用濃氨水檢查氯氣管道是否漏氣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com