
砷(As)在地殼中含量不大,但砷的化合物卻是豐富多彩。
(1)基態砷原子的電子排布式為 ;砷與溴的第一電離能較大的是 。
(2)AsH3是無色稍有大蒜味的氣體。AsH3的沸點高于PH3,其主要原因是 。
(3)Na3AsO4可作殺蟲劑。As 的空間構型為 ,與其互為等電子體的一種分子為 。
的空間構型為 ,與其互為等電子體的一種分子為 。
(4)某砷的氧化物俗稱“砒霜”,其分子結構如圖所示。該化合物的化學式為 ,As原子采取 雜化。

(5)GaAs等是人工合成的新型半導體材料,其晶體結構與金剛石相似。GaAs晶體中,每個As與 個Ga相連,As與Ga之間存在的化學鍵有 (填字母)。
A.離子鍵 B.σ鍵 C.π鍵 D.氫鍵 E.配位鍵 F.金屬鍵 G.極性鍵
(1)[Ar]3d104s24p3 Br(或溴)
(2)AsH3的相對分子質量大于PH3的,故AsH3分子間的范德華力大于PH3的
(3)正四面體 CCl4(或其他合理答案)
(4)As4O6 sp3
(5)4 BEG
【解析】(1)從K開始數數到As為15,所以As的核外電子排布式為[Ar]3d104s24p3,為第四周期ⅤA族的元素,第一電離能小于同周期第ⅦA族的元素;(4)As、O最外層電子數分別為5、6,分別形成3、2個共價鍵達到8電子穩定結構,所以黑球為O、灰球為As;As形成3個σ鍵,參加成鍵的電子數為3,孤對電子對數=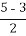 =1;(5)金剛石中一個碳原子與四個碳原子相連,Ga、As最外層電子數分別為3、5,Ga、As形成三個σ鍵,Ga還差2個電子達到8電子穩定結構,As有一對孤對電子,兩者之間形成配位鍵
=1;(5)金剛石中一個碳原子與四個碳原子相連,Ga、As最外層電子數分別為3、5,Ga、As形成三個σ鍵,Ga還差2個電子達到8電子穩定結構,As有一對孤對電子,兩者之間形成配位鍵


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2013-2014學年高考化學二輪沖刺選擇題限時提速專練 定量分析練習卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值,下列說法正確的是( )
①常溫常壓下,17 g甲基(—14CH3)中所含的中子數為9NA
②常溫常壓下,6.4 g Cu與40 mL 10 mol·L-1濃HNO3作用,產生NO2分子的數目為0.2NA
③1.6 g甲烷中含有的C—H鍵數目為0.1NA
④某溫度時,1 L pH=6的純水中含有1.0×10-6NA個H+
⑤7.8 g 中含有的碳碳雙鍵數目為0.3NA
中含有的碳碳雙鍵數目為0.3NA
⑥20 g氖氣中所含的原子數目為NA
⑦25℃時,pH=12的NaHCO3溶液中含有OH-的數目為0.01NA
⑧含NA個陰離子的Na2O2溶于水形成1 L溶液,其濃度為1 mol·L-1
A.①②⑦ B.④⑥ C.③⑤⑧ D.②③⑤⑥
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題復習 電化學練習卷(解析版) 題型:填空題
某課外活動小組同學用如圖裝置進行實驗,試回答下列問題:

(1)若開始時開關K與a連接,則B極的電極反應為 。
(2)若開始時開關K與b連接,則B極的電極反應為 ,總反應的離子方程式為 。有關上述實驗,下列說法正確的是(填序號) 。
①溶液中Na+向A極移動 ②從A極處逸出的氣體能使濕潤KI淀粉試紙變藍 ③反應一段時間后加適量鹽酸可恢復到電解前電解質的濃度 ④若標準狀況下B極產生2.24 L氣體,則溶液中轉移0.2 mol電子
(3)該小組同學模擬工業上用離子交換膜法制燒堿的方法,可以設想用如圖裝置電解硫酸鉀溶液來制取氫氣、氧氣、硫酸和氫氧化鉀。

①該電解槽的陽極反應為 。
此時通過陰離子交換膜的離子數 (填“大于”“小于”或“等于”)通過陽離子交換膜的離子數。
②通電開始后,陰極附近溶液pH會增大,請簡述原因 。
③若將制得的氫氣、氧氣和氫氧化鉀溶液組合為氫氧燃料電池,則電池正極的電極反應為 。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題復習 物質結構和元素周期律練習卷(解析版) 題型:選擇題
下圖是部分短周期元素原子半徑與原子序數的關系圖。則下列說法正確的是( )

A.Z、N兩種元素的離子半徑相比,前者較大
B.X、M兩種元素的氣態氫化物的穩定性相比,前者較弱
C.由X與M兩種元素組成的化合物不能與任何酸反應,但能與強堿反應
D.Z的氧化物能分別溶解于Y的氫氧化物和N的氫化物的水溶液
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題復習 物質結構與性質(選修3)練習卷(解析版) 題型:填空題
(1)鋅是一種重要的金屬,鋅及其化合物有著廣泛的應用。
①指出鋅元素在周期表中的位置: 周期, 族, 區。
②NH3分子中氮原子的雜化軌道類型為 ,基態氮原子的核外電子排布式是 。

③如圖表示鋅與某非金屬元素X形成的化合物晶胞,其中Zn和X通過共價鍵結合,該化合物的化學式為 ;該化合物的晶體熔點比干冰高得多,原因是 。
(2)氫氣作為一種清潔能源,必須解決它的儲存問題,C60可用作儲氫材料。
①已知金剛石中的C—C的鍵長為154.45 pm,C60中C—C鍵長為140~145 pm,有同學據此認為C60的熔點高于金剛石,你認為是否正確 ,并闡述理由 。

②科學家把C60和K摻雜在一起制造了一種富勒烯化合物,其晶胞如右圖所示,該物質在低溫時是一種超導體。該物質的K原子和C60分子的個數比為 。
③繼C60后,科學家又合成了Si60、N60。C、Si、N原子電負性由大到小的順序是 。Si60分子中每個硅原子只跟相鄰的3個硅原子形成共價鍵,且每個硅原子最外層都滿足8電子穩定結構,則Si60分子中π鍵的數目為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com