
| A、0.1molCuO |
| B、0.1molCuCO3 |
| C、0.1molCu(OH)2 |
| D、0.1molCu2(OH)2CO3 |


 導學全程練創優訓練系列答案
導學全程練創優訓練系列答案科目:高中化學 來源: 題型:
| 實驗步驟 | 實驗現象 |
| ①向裝有硫化亞鐵的試管中加入足量鹽酸; | 溶液無渾濁,有大量臭雞蛋氣味的氣體逸出 |
| ②將生成的硫化氫氣體通入蒸餾水中達到飽和,取適量飽和溶液于試管中,不斷振蕩后,觀察試管中的變化. | 試管中無明顯的渾濁現象 |
| 實驗步驟 | 實驗現象 |
| 將新配制的硫化鈉溶液分成兩等份, 分別裝入兩支試管中 | |
| 向一支試管中直接加入鹽酸; | 溶液稍顯渾濁,有臭雞蛋氣味的氣體逸出 |
| (1)向另一支試管中通入一定量氧氣,觀察溶液變化; (2)再加入鹽酸; | (1)溶液沒有明顯變化; (2)溶液明顯渾濁,有少量臭雞蛋氣味的氣體逸出. |
| 實驗步驟 | 預期現象和結論 |
| 向一裝有硫化鈉試管中加入足量的 溶液,以除去 沉淀,再將濾液裝入試管中,加入鹽酸. |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
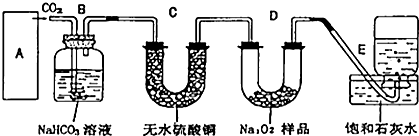
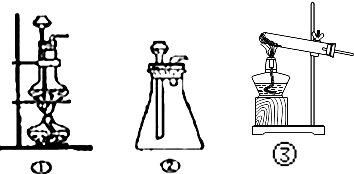
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、某溶液加AgNO3溶液生成白色沉淀,說明原溶液中有Cl- |
| B、某溶液加BaCl2溶液生成白色沉淀,說明原溶液中有SO42- |
| C、某溶液加NaOH溶液生成藍色沉淀,說明原溶液中有Cu2+ |
| D、某溶液加KOH溶液生成紅褐色沉淀,說明原溶液中有Mg2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、氯堿工業中通常使用陽離子交換膜將電解池的陽極區與陰極區隔開 | ||||
| B、合成氨工業中,將NH3不斷液化分離有利于加快反應速率 | ||||
| C、在銅質餐具上鍍銀時,應將餐具與電源的正極相連 | ||||
D、高爐煉鐵的主要反應為:Fe2O3+3CO
|
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:


查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com