
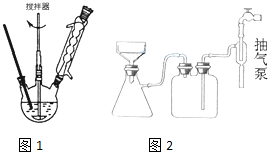
 羧酸通常用芳香烴的氧化來制備.芳香烴的苯環比較穩定,難于氧化,而環上的支鏈不論長短,在強烈氧化時,最終都氧化成羧基.某同學用甲苯的氧化反應制備苯甲酸.反應原理:
羧酸通常用芳香烴的氧化來制備.芳香烴的苯環比較穩定,難于氧化,而環上的支鏈不論長短,在強烈氧化時,最終都氧化成羧基.某同學用甲苯的氧化反應制備苯甲酸.反應原理:

| 名稱 | 相對分 子質量 | 性狀 | 熔點 | 沸點 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 無色液體易燃易揮發 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片狀或針狀晶體 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
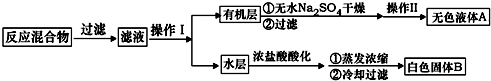
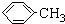 .操作Ⅱ為蒸餾.
.操作Ⅱ為蒸餾.分析 一定量的甲苯和適量的KMnO4溶液在100℃反應一段時間后停止反應,按如圖流程分離出苯甲酸和回收未反應的甲苯,苯甲酸能溶于水,甲苯不溶于水,互不相溶的液體采用分液方法分離,根據實驗目的知,從而得到有機層和水層,有機層中含有甲苯、水層中含有苯甲酸,有機層中的甲苯采用蒸餾方法得到無色液體A,A是甲苯,將水層鹽酸酸化再蒸發濃縮,根據苯甲酸的溶解度知,得到的固體B是苯甲酸,
(1)A是甲苯;分離互溶且沸點不同的液體采用蒸餾方法;
(2)如果濾液呈紫色,說明高錳酸鉀過量,要先加亞硫酸氫鉀,將高錳酸鉀還原,否則濃鹽酸可能被氧化成氯氣;
(3)A.抽濾時,瓶中壓強較小,可以加快過濾速度;
B.為了防止攪拌棒下端打壞三頸燒瓶底或溫度計,因此不能與它們接觸;
C.圖1回流攪拌裝置應采用水浴加熱的方法;
D.冷凝管中水的流向與蒸汽的流向相反;
(4)甲苯與NaOH不反應,苯甲酸與NaOH反應生成苯甲酸鈉,分液,苯甲酸鈉溶液中加鹽酸可以制得苯甲酸;
(5)苯甲酸和KOH溶液發生酸堿中和反應,根據苯甲酸和KOH之間的關系式計算苯甲酸的質量,從而計算苯甲酸的質量分數.
解答 解:一定量的甲苯和適量的KMnO4溶液在100℃反應一段時間后停止反應,按如圖流程分離出苯甲酸和回收未反應的甲苯,苯甲酸能溶于水,甲苯不溶于水,互不相溶的液體采用分液方法分離,根據實驗目的知,從而得到有機層和水層,有機層中含有甲苯、水層中含有苯甲酸,有機層中的甲苯采用蒸餾方法得到無色液體A,A是甲苯,將水層鹽酸酸化再蒸發濃縮,根據苯甲酸的溶解度知,得到的固體B是苯甲酸,
(1)A是甲苯,其結構簡式為: ;有機層中物質互溶且沸點不同,所以可以采用蒸餾方法分離,則操作II為蒸餾
;有機層中物質互溶且沸點不同,所以可以采用蒸餾方法分離,則操作II為蒸餾
故答案為: ;蒸餾;
;蒸餾;
(2)如果濾液呈紫色,說明高錳酸鉀過量,要先加亞硫酸氫鉀,除去未反應的高錳酸鉀,否則濃鹽酸酸化時可能被高錳酸鉀氧化成氯氣,
故答案為:除去未反應的高錳酸鉀氧化劑,否則用鹽酸酸化時會發生鹽酸被高錳酸鉀所氧化,產生氯氣;
(3)A.抽濾時,瓶中壓強較小,可以加快過濾速度,得到較干燥的沉淀,故A正確;
B.為了防止攪拌棒下端打壞三頸燒瓶底或溫度計,因此不能與它們接觸,所以在攪拌時,攪拌棒下端不能與三頸燒瓶底、溫度計等接觸,故B正確;
C.沸水浴加熱便于控制溫度和使容器受熱均勻,圖1回流攪拌裝置應采用水浴加熱的方法,故C錯誤;
D.冷凝管中水的流向與蒸汽的流向相反,則冷凝管中水的流向是下進上出,故D正確;
故答案為:ABD;
(4)除去殘留在苯甲酸中的甲苯應先加入,應該先加NaOH溶液,甲苯與NaOH不反應,苯甲酸與NaOH反應生成苯甲酸鈉,分液,苯甲酸鈉溶液中加鹽酸可以制得苯甲酸,
故答案為:NaOH溶液;濃鹽酸酸化;
(5)設苯甲酸的物質的量濃度為x,則25mL苯甲酸溶液中苯甲酸的物質的量為0.025xmol,
C6H5COOH+KOH→C6H5COOK+H2O
1mol 1mol
0.025xmol 2.40×10-3mol
1mol:1mol=0.025xmol:2.40×10-3mol
x=$\frac{2.4×1{0}^{-3}mol×1mol}{1mol×0.025mol}$=0.96,
則100mL苯甲酸中苯甲酸的質量=0.096mol/L×0.1L×122g/mol=1.1712g,其質量分數=$\frac{1.1712g}{1.220g}$=96%,
故答案為:96%.
點評 本題考查了實驗方案設計、混合物的分離和提純,側重考查分析問題能力、計算能力,明確物質的性質是解本題關鍵,知道根據物質的性質選取合適的分離方法,題目難度中等.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸 | B. | 漂白粉 | C. | 氫氧化鈉 | D. | 食鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定有銀、鐵和鎂 | B. | 僅有銀和鐵 | C. | 可能含鎂 | D. | 只有銀 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 大氣壓強對許多物理實驗和化學實驗有著重要影響.
大氣壓強對許多物理實驗和化學實驗有著重要影響.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 25℃ | pH | 25℃ | pH |
| 飽和H2S溶液 | 3.9 | FeS開始沉淀 | 3.0 |
| SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
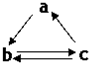 下表所列各組物質中,物質之間通過一步反應就能實現如圖所示轉化的是( )
下表所列各組物質中,物質之間通過一步反應就能實現如圖所示轉化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | SO3 | H2SO4 | S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com