
【題目】乙烯是一種重要的化工原料,可由乙烷為原料制取,回答下列問題。
(1)傳統的熱裂解法和現代的氧化裂解法的熱化學方程式如下:
①C2H6(g)=C2H4(g) +H2(g) ΔH1=+136 kJ/mol
②C2H6(g)+ ![]() O2(g)= C2H4(g)+H2O(g) ΔH2=-110 kJ/mol
O2(g)= C2H4(g)+H2O(g) ΔH2=-110 kJ/mol
已知反應相關的部分化學鍵鍵能數據如下:
化學鍵 | H-H(g) | H-O(g) | O=O(g) |
鍵能( kJ/mol) | 436 | X | 496 |
由此計算x=_________,通過比較△H1和△H2,說明和熱裂解法相比,氧化裂解法的優點是_______________________________(任寫一點)。
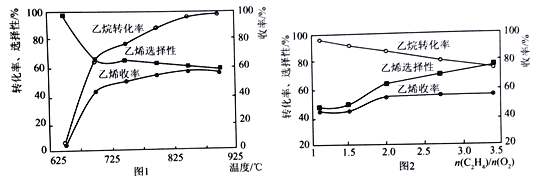
(2)乙烷的氧化裂解反應產物中除了C2H4外,還存在CH4、CO、CO2等副產物(副反應均為放熱反應),圖1為溫度對乙烷氧化裂解反應性能的影響。乙烷的轉化率隨溫度的升高而升高的原因是______,反應的最佳溫度為____________(填選項序號)。
A.700℃ B.750℃ C.850℃ D.900℃
[乙烯選擇性=![]() ;乙烯收率=乙烷轉化率×乙烯選擇性]
;乙烯收率=乙烷轉化率×乙烯選擇性]
(3)烴類氧化反應中,氧氣含量低會導致反應產生積炭,堵塞反應管。圖2為n(C2H6)/n(O2)的值對乙烷氧化裂解反應性能的影響。判斷乙烷氧化裂解過程中n(C2H6)/n(O2)的最佳值是_______________,判斷的理由是__________________________________。
(4)工業上,保持體系總壓恒定為100kPa的條件下進行該反應,通常在乙烷和氧氣的混合氣體中摻混惰性氣體(惰性氣體的體積分數為70%),摻混惰性氣體的目的是___________________________。
反應達平衡時,各組分的體積分數如下表:
C2H6 | O2 | C2H4 | H2O | 其他物質 |
2.4% | 1.0% | 12% | 15% | 69.6% |
計算該溫度下的平衡常數Kp=_________(用平衡分壓代替平衡濃度,平衡分壓=總壓×體積分數)
【答案】 465 氧化裂解反應是放熱反應,節約能源;氧化裂解反應熱力學趨勢上大 溫度升高,反應速率加快,轉化率升高 C 2 比值小于2時,乙烯的收率降低;比值大于2時,乙烯的收率并未增加且產生更多的積炭,堵塞反應管 正反應是氣體分子數增多的反應,恒壓充入惰性氣體相當于擴大容器體積,降低分壓,有利于平衡正向移動 KP = 75![]()
【解析】(1)②-①:![]() O2(g)+ H2(g) = H2O(g) ΔH=-246 kJ/mol,H-H(g)= 436 kJ/mol, H-O(g)= X
O2(g)+ H2(g) = H2O(g) ΔH=-246 kJ/mol,H-H(g)= 436 kJ/mol, H-O(g)= X
O=O(g)= 496 kJ/mol由此計算x= 465 kJ/mol,
通過比較△H1和△H2,說明和熱裂解法相比,氧化裂解法的優點是氧化裂解反應是放熱反應,節約能源;氧化裂解反應熱力學趨勢上大。
(2)乙烷的氧化裂解反應產物中除了C2H4外,還存在CH4、CO、CO2等副產物,因為副反應均為放熱反應升高溫度,不利于副產物的生成;因為乙烯選擇性=![]() ,所以由圖知溫度升高,反應速率加快,轉化率升高為;由圖觀察溫度在850℃和900℃之間,乙烷的轉化率都比較大,乙烯收率較高和乙烯選擇性較,所以,選擇850℃較好,答案:溫度升高,反應速率加快,轉化率升高 C。
,所以由圖知溫度升高,反應速率加快,轉化率升高為;由圖觀察溫度在850℃和900℃之間,乙烷的轉化率都比較大,乙烯收率較高和乙烯選擇性較,所以,選擇850℃較好,答案:溫度升高,反應速率加快,轉化率升高 C。
(3)由圖2觀察知n(C2H6)/n(O2)<2時,乙烯的收率降低;比值大于2時,乙烯的收率并未增加且產生更多的積炭,堵塞反應管,所以當n(C2H6)/n(O2)=2時最佳值。答案2 比值小于2時,乙烯的收率降低;比值大于2時,乙烯的收率并未增加且產生更多的積炭,堵塞反應管。
(4)由C2H6(g)+ ![]() O2(g)= C2H4(g)+H2O(g) ΔH2=-110 kJ/mol,知正反應是氣體分子數增多的反應,工業上,保持體系總壓恒定為100kPa的條件下進行該反應,如果在乙烷和氧氣的混合氣體中摻混惰性氣體相當于擴大容器體積,降低分壓,有利于平衡正向移動,提高反應物的轉化率。
O2(g)= C2H4(g)+H2O(g) ΔH2=-110 kJ/mol,知正反應是氣體分子數增多的反應,工業上,保持體系總壓恒定為100kPa的條件下進行該反應,如果在乙烷和氧氣的混合氣體中摻混惰性氣體相當于擴大容器體積,降低分壓,有利于平衡正向移動,提高反應物的轉化率。
因為總壓恒定為100kPa,
C2H6(g) +![]() O2(g) = C2H4(g)+ H2O(g)
O2(g) = C2H4(g)+ H2O(g)
平衡量2.4%![]() 1.0%
1.0%![]() 12%
12%![]() 15%
15%![]() kPa
kPa
該溫度下的平衡常數就是反應達到平衡時Kp=生成物濃度冪次方的乘積比反應物濃度冪次方的乘積,所以Kp=![]() =75
=75![]()
答案:正反應是氣體分子數增多的反應,恒壓充入惰性氣體相當于擴大容器體積,降低分壓,有利于平衡正向移動,75![]()


科目:高中化學 來源: 題型:
【題目】現有下列幾種有機物:
A.![]() B.
B.![]() C.
C.![]() D.CH2 = CH—CH = CH2E.環戊烷
D.CH2 = CH—CH = CH2E.環戊烷
(1)上述有機物中互為同系物的是_____________,互為同分異構體的是____________。
(2)用系統命名法對B進行命名____________________________________。
(3)A與Cl2反應的類型為_____________;D使溴水褪色的反應類型為___________。
(4)B發生加聚反應的化學方程式為 ____________________________________。
(5)如圖表示的是一種叫做雙烯合成的有機反應,請寫出B與D發生雙烯合成所得產物的結構簡式__________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液一定呈中性的是 )
A. cOH)=cH+)的溶液 B. 鹽溶液
C. pH=3的酸與pH=11的堿等體積混合所得溶液 D. pH=7的溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究黑色固體 X(僅含兩種元素)的組成和性質,設計并完成如下實驗:

請回答:
(1) X 的化學式是______。
(2) 固體甲與稀硫酸反應的離子方程式是______。
(3) 寫出 X 在隔絕空氣高溫反應的化學方程式______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應4A(s)+3B(g)═2C(g)+D(g),經2min,B的濃度減少0.6mol/L.對此反應速率的表示正確的是( )
A.用A表示的反應速率是0.4 mol(Lmin)﹣1
B.分別用B,C,D表示的反應速率其比值是3:2:1
C.在2min末的反應速率,用B表示是0.3 mol(Lmin)﹣1
D.在這2min內用B和C表示的反應速率的值都是逐漸減小的
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應屬于加成反應的是( )
A. CH4+Cl2![]() CH3Cl + HCl
CH3Cl + HCl
B. H2+ Cl2![]() 2HCl
2HCl
C. CH2=CH2+ H2O![]() CH3CH2OH
CH3CH2OH
D. 2NaOH + Cl2=NaClO + NaCl + H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能源短缺是人類社會面臨的重大問題.甲醇是一種可再生能源,具有廣泛的開發和應用前景.
(1)工業上一般采用下列兩種反應合成甲醇: 反應I:CO(g)+2H2(g)CH3OH(g)△H1
反應II:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2
①上述反應符合“原子經濟”原則的是(填“I”或“Ⅱ”).
②下表所列數據是反應I在不同溫度下的化學平衡常數(K).
溫度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中數據判斷△H10 (填“>”、“=”或“<”).
③某溫度下,將2mol CO和6mol H2充入2L的密閉容器中,充分反應,達到平衡后,測得c(CH3OH)=0.8mol/L,則CO的轉化率為 , 此時的溫度為(從上表中選擇).
④恒溫、恒容時,下列情況不能說明反應I已經達到化學平衡狀態的是 .
a、容器各物質的濃度保持不變; b、容器內壓強保持不變;
c、υ(CO)消耗═1/2υ(H2)生成 d、容器內的密度保持不變
(2)25℃、101kPa時,燃燒16g液體甲醇生成CO2和H2O(l),放出的熱量為363.26kJ,寫出甲醇燃燒的熱化學方程式: .
(3)某實驗小組依據甲醇燃燒的反應原理,設計一個燃料電池電解Na2SO4溶液(圖如下).請根據圖示回答下列問題: 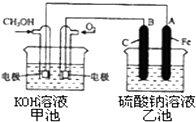
①通入甲醇蒸氣的電極應為極(填寫“正”或“負”),該電極上發生的電極反應是(填字母代號).
a.2CH3OH﹣12e﹣+3O2═2CO2+4H2O
b.CH3 OH﹣6e﹣+8OH﹣═CO32﹣+6H2O
c.O2+2H2O+4e﹣═4OH﹣
d.O2﹣4e﹣+4H+═2H2O
②寫出電極A的名稱 . 寫出B電極的電極反應式 .
③當堿性甲醇燃料電池消耗3.36L 氧氣時(折合為標準狀況),理論上電解Na2SO4溶液生成氣體的總物質的量是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
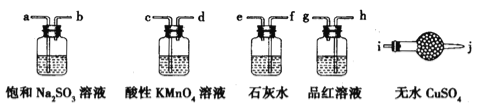
【題目】某化學興趣小組為合成1-丁醇,查閱資料得知如下合成路線CH3CH=CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
已知:CO 的制備原理:HCOOH ![]() CO↑+H2O。
CO↑+H2O。
(1)正丁醛經催化加氫得到含少量正丁醛的 1-丁醇粗品。為純化 1-丁醇,該小組查閱文獻得知:
①R—CHO+NaHSO3(飽和) →RCH(OH)SO3Na↓;
②沸點:乙醚 34℃,1-丁醇 118℃,并設計出如下提純路線:
![]()
試劑1為 ,操作3為 。
(2)原料氣CH3CH=CH2、CO和H2的制備裝置圖設計如下:
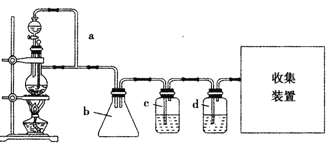
填寫下列空白:
①若用上述裝置制備干燥純凈的CO氣體,裝置b的作用是 ;c中盛裝的試劑是 。
②若用上述裝置制備氫氣,收集裝置可選用下列裝置
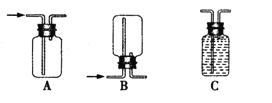
③實驗室現有鋅粒、稀硝酸、稀鹽酸、濃硫酸、2-丙醇,從中選擇合適的試劑制備丙烯,寫出反應的化學方程式: 。 制丙烯時,產生的氣體除了丙烯及水蒸氣外,還存在CO2、SO2;為檢驗這四種氣體,下列裝置按氣流方向的連接順序為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com