
分析 (1)NaHSO4為強電解質,完全電離,電離出鈉離子、氫離子、硫酸根離子;
(2)NaHSO4固體加熱熔融電離出鈉離子和硫酸氫根離子;
(3)電離中只有化學鍵斷裂,沒有化學鍵生成;
(4)共價化合物熔融狀態不電離.
解答 解:(1)NaHSO4固體溶于水電離方程式為NaHSO4=Na++H++SO42-,斷裂的化學鍵為離子鍵和共價鍵,故答案為:NaHSO4=Na++H++SO42-;離子鍵和共價鍵;
(2)NaHSO4固體加熱熔融電離方程式為NaHSO4=Na++HSO4-,斷裂化學鍵為離子鍵,故答案為:NaHSO4=Na++HSO4-;離子鍵;
(3)從化學反應的實質的角度解釋原因是上述兩種變化只有舊化學鍵的斷裂,沒有新化學鍵的形成,故不是化學變化,故答案為:只有舊化學鍵的斷裂,沒有新化學鍵的形成;
(4)區別離子化合物和共價化合物的方法是加熱熔融進行導電性實驗,熔融狀態下能導電的化合物是離子化合物,不導電的化合物是共價化合物,
故答案為:加熱熔融進行導電性實驗,熔融狀態下能導電的化合物是離子化合物,不導電的化合物是共價化合物.
點評 本題考查較綜合,涉及化學鍵、電離及物質類別等,注重高頻考點及基礎知識點的考查,綜合性較強,題目難度不大,注意NaHSO4固體在溶于水及熔化狀態的區別.


 鷹派教輔銜接教材河北教育出版社系列答案
鷹派教輔銜接教材河北教育出版社系列答案 初中暑期銜接系列答案
初中暑期銜接系列答案科目:高中化學 來源: 題型:選擇題
| A. | 如圖所示 表示乙醇的比例模型 表示乙醇的比例模型 | |
| B. | 蔗糖、纖維素的水解過程都是高分子轉化為小分子的過程 | |
| C. | 甲烷、甲醛、甲酸都不存在同分異構體,則甲醚(CH3OCH3)也不存在同分異構體 | |
| D. | HOCH2COOH既可以發生取代反應又可以發生縮聚反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2O:0.002 mol•L-1 | B. | NO:0.001 mol•L-1 | ||
| C. | NH3:0.002 mol•L-1 | D. | O2:0.0025 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

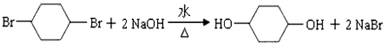 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸氫鈉和稀鹽酸反應:CO32-+2H+=H2O+CO2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | 三氯化鐵溶液中加入鐵粉:Fe3++Fe=2Fe2+ | |
| D. | FeCl2溶液跟氯氣反應:2Fe2++Cl2=2 Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單位時間內生成n molA2同時生成n mol AB3 | |
| B. | 容器內的總物質的量不隨時間變化 | |
| C. | 單位時間內生成2n mol AB3的同時生成n molB2 | |
| D. | 單位時間內生成n molA2的同時生成n molB2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | F2<Cl2<Br2<I2 | B. | CF4>CCl4>CBr4>CI4 | ||
| C. | HCl<HBr<HI<HF | D. | CH4<SiH4<GeH4<SnH4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com