
【題目】A、B、C、D, E、F、G、H是元素周期表前四周期常見元素,且原子序數依次增大,其相關信息如下表:
元素 | 相關信息 |
A | 原子核外有6種不同運動狀態的電子 |
C | 基態原子中s電子總數與p電子總數相等 |
D | 原子半徑在同周期元素中最大 |
E | 基態原子最外層電子排布式為3s23p1 |
F | 基態原子的最外層p軌道有兩個電子的自旋方向與其他電子的自旋方向相反 |
G | 基態原子核外有7個能級且能量最高的能級上有6個電子 |
H | 是我國使用最早的合金中的最主要元素 |
請用化學用語填空:
(1)A元素位于元素周期表第_______周期_______族;B元素和C元素的第一電離能比較,較大的是________,C元素和F元素的電負性比較,較小的是________。
(2)B元素與宇宙中含量最豐富的元素形成的最簡單化合物的分子模型為________,B元素所形成的單質分子![]() 鍵與π鍵數目之比為________。
鍵與π鍵數目之比為________。
(3)G元素的低價陽離子的離子結構示意圖是________,F元素原子的價電子的軌道表示式是________,H元素的基態原子核外電子排布式的________。
(4)G的高價陽離子的溶液與H單質反應的離子方程式為_________________;與E元素成對角線關系的某元素的最高價氧化物的水化物具有兩性,寫出該兩性物質與D元素的最高價氧化物的水化物反應的離子方程式:_________________。
【答案】二 ⅣA N Cl 三角錐 1∶2 ![]()
![]() 1s22s22p63s23p63d104s1或[Ar]3d104s1 2Fe3++3Cu=2Fe2++Cu2+ Be(OH)2+2NaOH=Na2BeO2+2H2O
1s22s22p63s23p63d104s1或[Ar]3d104s1 2Fe3++3Cu=2Fe2++Cu2+ Be(OH)2+2NaOH=Na2BeO2+2H2O
【解析】
A、B、C、D、E、F、G、H是元素周期表前四周期常見元素,且原子序數依次增大,A原子核外有6種不同運動狀態的電子,則A為碳元素;E基態原子最外層電子排布式為3s23p1,則E為Al元素;D原子半徑在同周期元素中最大,且原子序數小于Al,大于碳,故處于第三周期ⅠA族,則D為Na元素;C基態原子中s電子總數與p電子總數相等,原子序數小于Na,原子核外電子排布為1s22s22p4,則C為O元素;B的原子序數介于碳、氧之間,則B為N元素;G基態原子核外有7個能級且能量最高的能級上有6個電子,核外電子排布式為1s22s22p63s23p63d64s2,則G為Fe元素;F基態原子的最外層p軌道有兩個電子的自旋方向與其它電子的自旋方向相反,外圍電子排布為ns2np5,結合原子序數可知,F為Cl元素;H是我國使用最早的合金中的最主要元素,則H為Cu元素,據此分析解答。
根據上述分析,A為碳元素,B為N元素;C為O元素;D為Na元素;E為Al元素;F為Cl元素;G為Fe元素;H為Cu元素。
(1)A為碳元素,位于元素周期表第二周期ⅣA族,N元素原子2p軌道為半滿穩定狀態,能量較低,第一電離能高于O元素;O與Cl形成的化合物中O元素表現負價,對鍵合電子的吸引能力更強,故Cl的電負性較小,故答案為:二;ⅣA;N;Cl;
(2)N元素與宇宙中含量最豐富的元素形成的最簡單化合物為NH3,分子構型為三角錐形,N元素所形成的單質分子結構式為N≡N,分子σ鍵與π鍵數目之比為1∶2,故答案為:三角錐形;1∶2;
(3)G為Fe元素,其低價陽離子的離子結構示意圖是 ;F為Cl元素,其原子的價電子軌道表示式為
;F為Cl元素,其原子的價電子軌道表示式為![]() ;H為Cu元素,其基態原子核外電子排布式是1s22s22p63s23p63d104s1,故答案為:
;H為Cu元素,其基態原子核外電子排布式是1s22s22p63s23p63d104s1,故答案為: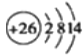 ;
;![]() ;1s22s22p63s23p63d104s1;
;1s22s22p63s23p63d104s1;
(4)鐵離子與Cu反應生成亞鐵離子與銅離子,反應的離子方程式為:2Fe3++Cu=2Fe2++Cu2+;與E(Al)元素成對角關系的某元素的最高價氧化物的水化物具有兩性,該元素為Be,其最高價氧化物為Be(OH)2,與氫氧化鈉反應方程式為:Be(OH)2+2NaOH=Na2BeO2+2H2O,故答案為:2Fe3++Cu=2Fe2++Cu2+;Be(OH)2+2NaOH=Na2BeO2+2H2O。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】常溫時,Ca(OH)2和CaWO4(鎢酸鈣)的沉淀溶解平衡曲線如圖所示。下列分析不正確的是
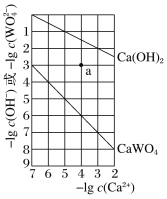
A. 常溫時Ksp[Ca(OH)2]>Ksp(CaWO4)
B. a點:無Ca(OH)2沉淀,有CaWO4沉淀
C. 加熱飽和Ca(OH)2溶液有白色沉淀生成
D. 常溫時這兩種飽和溶液中c(Ca2+)相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼鎂泥是一種工業廢料,主要成份是MgO(占40%,質量分數),還有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等雜質,以此為原料制取的硫酸鎂,可用于印染、造紙、醫藥等工業。從硼鎂泥中提取MgSO47H2O的工藝流程如下:
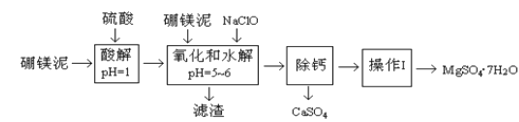
(1)實驗中需要1 mol/L的硫酸980 mL,若用 98% 的濃硫酸(ρ= 1.84 g/mL)來配制,量取濃硫酸需要使用量筒的規格為____(填寫選項字母)。
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可與Mn2+ 反應:Mn2+ + ClO + H2O = MnO2↓+ 2H+ + Cl ,在該步驟中還有一種離子也會被NaClO氧化,該反應的離子方程式為________。
(3)濾渣的主要成分除含有Fe(OH)3、Al(OH)3外,還含有______,____。
(4)在“除鈣”前,需檢驗濾液中Fe3+ 是否被除盡,簡述檢驗方法_____。(寫出操作、現象和結論)
(5)已知MgSO4、CaSO4 的溶解度(單位為 g/100 g 水)如下表:
溫度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除鈣”是將MgSO4和CaSO4混合溶液中的CaSO4除去,根據上表數據,簡要說明操作步驟_______。“操作Ⅰ”是將濾液繼續蒸發濃縮,冷卻結晶,______,便得到了MgSO47H2O。
(6)實驗中提供的硼鎂泥共100 g ,得到 MgSO47H2O 為196.8 g ,則MgSO47H2O 的產率為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(一)Na、Cu、O、Si、S、Cl是常見的六種元素.
(1)Na位于元素周期表第__周期第__族;S的基態原子核外有__個未成對電子;
Si的基態原子核外電子排布式為__.
(2)用“>”或“<”填空:
第一電離能 | 離子半徑 | 熔點 | 酸性 |
Si______S | O2-______Na+ | NaCl ______ Si | H2SO4 __________HClO4 |
(3)ClO2常用于水的凈化,工業上可用Cl2氧化NaClO2溶液制取.寫出該反應的離子方程式,并標出電子轉移的方向和數目___
(二).某元素的原子序數為33,請回答:
(1)該元素原子核外有_______個電子層,______個能級,______個原子軌道。
(2)它的最外層電子排布式為____________,它的電子排布式為________,軌道表示式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關反應的離子方程式正確的是( )
A.氯氣溶于水:Cl2+H2O=H++Cl-+HClO
B.Fe跟稀鹽酸反應:2Fe+6H+=2Fe3++3H2↑
C.將濃鹽酸與MnO2混合加熱:MnO2+2H++2Cl-![]() Mn2++Cl2↑+H2O
Mn2++Cl2↑+H2O
D.過氧化鈉投入水中:Na2O2+2H2O=O2↑+2OH-+2Na+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以氯酸鈉等為原料制備亞氯酸鈉的工藝流程如下,下列說法錯誤的是

A. NaClO3在發生器中作氧化劑
B. 吸收塔中1mol H2O2得到2mol電子
C. 吸收塔中溫度不宜過高,會導致H2O2的分解
D. 從“母液”中可回收的主要物質是Na2SO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據所學知識,回答下列問題:
I. 0.5L 1mol·l-1 氫氧化鈉溶液中所含溶質的質量為________g,加水將溶液稀釋到10L,其物質的量濃度是_________mol·l-1,取稀釋后的溶液 10mL,其溶質的物質的量濃度是________mol·L-1.
Ⅱ.標準狀況下,比較等物質的量 H2S、NH3、CH4 三種氣體,并完成下列填空。
(1)體積之比________
(2)質量之比為________
(3)原子數之比為________
(4)氫原子數之比為________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在0.2L由NaCl、MgCl2、BaCl2組成的混合溶液中,部分離子濃度大小如圖所示,對于該溶液成分。下列說法不正確的是( )

A. NaCl的物質的量為0.2mol
B. 溶質MgCl2的質量為9g
C. 該混合液中BaCl2的物質的量為0.1mol
D. 將該混合液加水稀釋至體積為1L,稀釋后溶液中Ba2+的物質的量濃度為0.1mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA為阿伏加德羅常數的數值,下列說法中正確的是( )
①0.5molO3與11.2LO2所含的分子數一定相等
②標準狀況下,22.4L氯氣與足量鋁充分反應,轉移的電子數為3NA
③通常狀況下,NA 個CO2分子占有的體積為22.4L
④常溫常壓下,92g的NO2和N2O4混合氣體含有的原子數為6NA
⑤常溫下,4.4g CO2和N2O(不反應)混合物中所含有的原子數為0.3 NA
⑥在反應KIO3+6HI===KI+3I2+3H2O中,每生成3molI2轉移的電子數為6NA
⑦標準狀況下,22.4 L SO3含有的分子數為NA
⑧在常溫常壓下,1 mol O2含有的原子數為2NA.
⑨物質的量濃度為0.5 mol·L-1 MgCl2溶液中,含有Cl-個數為NA
⑩將100 mL 0.1 mol·L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3膠粒數目為0.01NA
A. ①②④⑧B. ④⑤⑧C. ③⑥⑨⑩D. ④⑤⑧⑨
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com