
科學家一直致力于研究常溫、常壓下“人工固氮”的新方法。曾有實驗報道:在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生反應,生成的主要產物為NH3。進一步研究NH3生成量與溫度的關系,部分實驗數據見下表(光照、N2壓力1.0×105 Pa、反應時間3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
相應的熱化學方程式如下:
![]() N2(g)+3H2O(l) 2NH3(g)+
N2(g)+3H2O(l) 2NH3(g)+![]() O2(g)
O2(g)
ΔH=+765.2 kJ·mol-1
回答下列問題:![]()
![]()
![]()
![]()
![]()
![]()
![]()
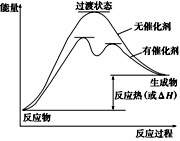
(1)請畫出上述反應在有催化劑與無催化劑兩種情況下反應過程中體系能量變化示意圖,并進行必要標注。
(2)與目前廣泛使用的工業合成氨方法相比,該方法中固氮反應速率慢。請提出可提高其反應速率且增大NH3生成量的建議: 。
![]() (3)工業合成氨的反應為N2(g)+3H2(g) 2NH3(g)。設在容積為2.0 L的密閉容器中充入
(3)工業合成氨的反應為N2(g)+3H2(g) 2NH3(g)。設在容積為2.0 L的密閉容器中充入
0.60 mol N2(g)和1.60 mol H2(g),反應在一定條件下達到平衡時,NH3的物質的量分數(NH3的物質的量與反應體系中總的物質的量之比)為![]() 。計算:
。計算:
①該條件下N2的平衡轉化率;
![]() ②該條件下反應2NH3(g) N2(g)+3H2(g)的平衡常數。
②該條件下反應2NH3(g) N2(g)+3H2(g)的平衡常數。
(1)![]()
![]()
(2)升溫、增大N2濃度、不斷移出生成物![]()
![]()
![]()
![]()
![]()
![]()
![]()
(3)①66.7% ②5.0×10-3mol2·L-2
(1)催化劑能降低反應的活化能,改變反應的歷程,使一個高能變過程變為幾個能量相對低的過程,使反應易發生。要點是有催化劑時能量低而過程階段多了。圖見答案。
(2)加快反應速率且增大NH3生成量的方法是升溫、增大N2濃度、不斷移出生成物。
(3)解:①設反應過程消耗xmolN2(g)。
![]() N2(g)+3H2(g) 2NH3(g)
N2(g)+3H2(g) 2NH3(g)
起始物質的量/mol 0.60 1.60 0
平衡物質的量/mol 0.60-x 1.60-3x 2x
平衡時反應體系總物質的量=[(0.60-x)+(1.60-3x)+2x]mol=(2.20-2x) mol
NH3(g)的物質的量分數=2x÷(2.20-2x)=4/7
x=0.40
N2的平衡轉化率=![]() ×100%=66.7%
×100%=66.7%
![]() ②設反應2NH3(g) N2(g)+3H2(g)的平衡常數為K。平衡時,c(NH3)=2×0.40 mol÷2.0 L=
②設反應2NH3(g) N2(g)+3H2(g)的平衡常數為K。平衡時,c(NH3)=2×0.40 mol÷2.0 L=
0.40 mol·L-1c(N2)=(0.60-0.40) mol÷2.0 L=0.10 mol·L-1
c(H2)=(1.60-3×0.40) mol÷2.0 L=0.20 mol·L-1
K=![]() =[(0.10 mol·L-1?)×(0.20 mol·L-1)3]÷(0.40 mol·L-1)2
=[(0.10 mol·L-1?)×(0.20 mol·L-1)3]÷(0.40 mol·L-1)2
=5.0×10-3mol2·L-2


 一線名師提優試卷系列答案
一線名師提優試卷系列答案科目:高中化學 來源: 題型:閱讀理解
| T/K | 303 | 313 | 323 |
| 平衡時NH3的生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
| ||
| ||


| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
 2NH3(g).設在容積為2.0L的密閉容器中充入0.60mol N2(g)和1.60molH2(g),反應在一定條件下達到平衡時,NH3的物質的量分數(NH3的物質的量與反應體系中總的物質的量之比)為
2NH3(g).設在容積為2.0L的密閉容器中充入0.60mol N2(g)和1.60molH2(g),反應在一定條件下達到平衡時,NH3的物質的量分數(NH3的物質的量與反應體系中總的物質的量之比)為| 4 |
| 7 |
 N2(g)+3H2(g)的平衡常數.
N2(g)+3H2(g)的平衡常數.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 自然界里氮的固定途徑之一是在閃電的作用下,N2與O2反應生成NO.
自然界里氮的固定途徑之一是在閃電的作用下,N2與O2反應生成NO.| 溫度/℃ | 1538 | 1760 | 2404 |
| 平衡常數K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
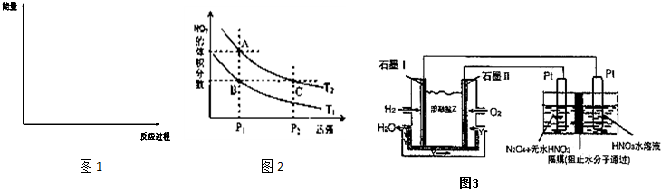
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
| 4 |
| 7 |
查看答案和解析>>
科目:高中化學 來源:2011-2012年安徽紅星中安工大附中高二下學期期中聯考理科化學試卷(帶解析) 題型:填空題
(6分)自然界里氮的固定途徑之一是在閃電的作用下,N2與O2反應生成NO。
(1)在不同溫度下,反應N2(g)+O2(g) 2NO(g) DH=a kJ·mol-1的平衡常數K如下表:
2NO(g) DH=a kJ·mol-1的平衡常數K如下表:
| 溫度/℃ | 1538 | 1760 | 2404 |
| 平衡常數K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
 2NO(g)達到平衡時N2的濃度為 。(此溫度下不考慮O2與NO的反應。計算結果保留兩位有效數字)
2NO(g)達到平衡時N2的濃度為 。(此溫度下不考慮O2與NO的反應。計算結果保留兩位有效數字)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com