
【題目】下列關于實驗室制取氨氣的說法不正確的是( )
A.可用濃鹽酸檢驗氨氣
B.可用濃硫酸干燥氨氣
C.可用向下排空氣法收集氨氣
D.可將濃氨水滴入盛有生石灰的燒瓶制取氨氣
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】Ⅰ.根據下列各題中所給出的數據,可分別求出其溶液的“溶質質量分數”或溶液的“物質的量濃度”,試求解。
(1)已知某氫氧化鈉溶液V L中含有N個氫氧根離子,可求出此溶液的物質的量濃度是________。
(2)已知某氫氧化鈉溶液中Na+與H2O的個數之比為1∶a,則可求出此溶液的溶質的質量分數為________。
Ⅱ.常溫下,10.0 mL 1.0 mol·L-1的H2SO4(aq),加水稀釋到500 mL,所得H2SO4(aq)的濃度為________mol·L-1;蒸發濃縮,使溶液的體積為2.40 mL,所得H2SO4(aq)的濃度為____mol·L-1。
Ⅲ.已知標準狀況下1體積水能溶解500體積的氯化氫,得到密度為1.19g/mL的鹽酸,則可求出標準狀況下氯化氫飽和溶液中溶質的質量分數為______,該鹽酸的濃度為_____(結果均保留一位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于化學鍵的說法正確的是
A. 構成單質分子的微粒一定含有共價鍵
B. 不同元素組成的多原子分子里的化學鍵一定都是極性鍵
C. 非極性鍵只存在于雙原子單質分子中
D. 全部由非金屬元素組成的化合物不一定是共價化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】立方氮化硼CBN( Cubic Boron Nitrde)的硬度僅次于金剛石而遠遠高于其它材料,因此它與金剛石統稱為超硬材料,具有優異的耐磨性。其晶體結構如下圖所示:
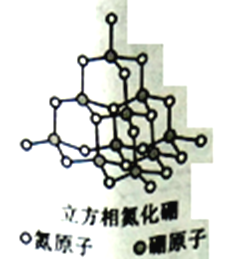
(1)基態氮原子的價電子層排布式是_____________,在氮和硼原子所在的周期中,第一電離能小于氮原子的有_____種元素的原子。
(2)氮原子和硼原子形成的化學鍵類型有_____________________。
(3)硼原子的雜化類型是_______,與硼原子緊相連的4個氮原子的空間構型是________,鍵角是_______ 。
(4)晶胞如圖所示,該晶體屬于______晶體。
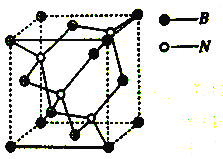
(5)晶體中所連接的最小環上是六元環,每個硼原子被_____個六元環共用,六元環最多有_____個原子在同一平面上。若晶胞邊長為apm,立方氮化硼的密度是ρg/cm3,則NA的表達式是____(用a和ρ表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表所示的體檢報告的部分項目中,表示總膽固醇指標的物理量是( )
送檢物:血液 檢驗目的:血常規 血型:O型 | 檢驗結果: 項目中文名稱結果單位參考值 ALT谷丙轉氨酶7U/L<40 ALB白蛋白43.9g/L35-55 TC總膽固醇4.27mmol/L3.6-5.18 |
A.溶解度B.質量分數C.密度D.物質的量濃度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】檸檬酸(用HR 表示)是一種高效除垢劑,現用一定濃度的檸檬酸溶液去除水垢,溶液中H3R、H2R-、HR2-、R3-的含量隨pH的變化如圖所示。下列說法正確的是

A. H3R的第二步電離常數Ka2(H3R)的數量級為10-4
B. pH=6時,c(R3-)=c(HR2-)>c(H+)>c(OH-)
C. Na2HR溶液中HR2-的水解程度大于電離程度
D. pH=4時,c(H+)=c(H2R-)+2c(HR2-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物M 是一種局部麻醉藥,實驗室由芳香烴A 合成M的一種路線如下:
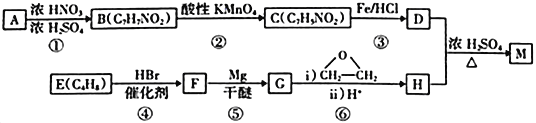
已知: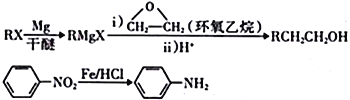
回答下列問題:
(1)A的化學名稱為______________,F中所含的官能團為____________。
(2)③的反應類型是____________,④的反應類型是_____________。
(3)B的苯環上有2種化學環境的氫原子,D在一定條件下發生縮聚反應生成的高分子產物的結構簡式為_______________________。
(4)F的核磁共振氫譜只有1組吸收峰,D和H生成M的化學方程式為__________________________。
(5)L是H的同分異構體,L不能與金屬鈉反應,核磁共振氫譜只有兩組峰,且峰面積比為6∶1,L的結構簡式為__________________________。
(6)參照上述合成路線,以乙烯和環氧乙烷為原料(無機試劑任選)制備1,6-己二醛[OHC(CH2)4CHO],設計合成路線______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從海水得到的粗食鹽水中常含Ca2+、Mg2+、SO42-,需要分離提純。現有含少量CaCl2、MgSO4的粗食鹽水,在除去懸浮物和泥沙之后,要用4種試劑:①鹽酸、②Na2CO3、③NaOH、④BaCl2來除去食鹽水中的Ca2+、Mg2+、SO42-。提純時的操作步驟和加入試劑的情況如圖。

圖中a、b、c、d分別表示上述4種試劑中的一種,請回答:
(1)沉淀A的名稱是________。
(2)試劑d是________;判斷試劑d已經足量的方法是__________________________。
(3)加入b、c后溶液中發生的化學反應的化學方程式有______________________(任寫兩個)。
(4)現有下列儀器,過濾出沉淀A、B、C時必須用到的是____(填序號),儀器③的名稱是_______。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】天然氣是一種重要的清潔能源和化工原料,其主要成分為甲烷。
(1)工業上可用煤制天然氣,生產過程中有多種途徑生成CH4。
寫出CO與H2反應生成CH4和H2O的熱化學方程式
已知: CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1
C(s)+2H2(g)![]() CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1
2CO(g)![]() C(s)+CO2(g) ΔH=-171kJ·mol-1
C(s)+CO2(g) ΔH=-171kJ·mol-1
(2)天然氣中的H2S雜質常用氨水吸收,產物為NH4HS。一定條件下向NH4HS溶液中
通入空氣,得到單質硫并使吸收液再生,寫出再生反應的化學方程式 。
(3)天然氣的一個重要用途是制取H2,其原理為:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)。在密閉容器中通入物質的量濃度均為0.1mol·L-1的CH4與CO2,在一定條件下發生反應,測得CH4的平衡轉化率與溫度及壓強的關系如下圖1所示,則壓強P1 P2(填“大于”或“小于”);壓強為P2時,在Y點:v(正) v(逆)(填“大于”、“小于”或“等于”)。 求Y點對應溫度下的該反應的平衡常數K= 。(計算結果保留兩位有效數字)
2CO(g)+2H2(g)。在密閉容器中通入物質的量濃度均為0.1mol·L-1的CH4與CO2,在一定條件下發生反應,測得CH4的平衡轉化率與溫度及壓強的關系如下圖1所示,則壓強P1 P2(填“大于”或“小于”);壓強為P2時,在Y點:v(正) v(逆)(填“大于”、“小于”或“等于”)。 求Y點對應溫度下的該反應的平衡常數K= 。(計算結果保留兩位有效數字)
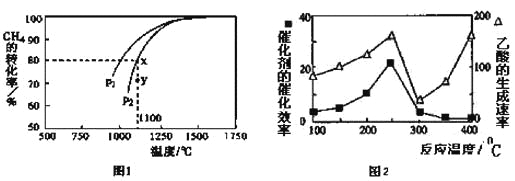
(4) 以二氧化鈦表面覆蓋CuAl2O4為催化劑,可以將CH4和CO2直接轉化成乙酸。
①在不同溫度下催化劑的催化效率與乙酸的生成速率如圖2所示。250~300℃時,溫度升高而乙酸的生成速率降低的原因是 。
②為了提高該反應中CH4的轉化率,可以采取的措施是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com