
有下列儀器:①漏斗;②錐形瓶;③蒸餾燒瓶;④天平;⑤分液漏斗;⑥量筒;⑦燃燒匙。其中常用于分離物質的儀器是
A.①③④ B.①②⑥ C.①③⑤ D.③④⑦
科目:高中化學 來源:2016屆浙江省溫州市高三上學期期中測試理綜化學試卷(解析版) 題型:填空題
某含氯化合物A由兩種短周期元素組成,常溫下該物質為氣態,測得該氣體對空氣的相對密度為3.0,A溶于水可得只含單一溶質B的弱酸性溶液,B溶液在放置過程中其酸性會增強.常溫下,氣體A與NH3反應生成離子晶體C、氣體單質D和常見液體E,D為空氣中含量最多的物質。氣體A可用某一氣體單質與潮濕的Na2CO3 反應制得,同時生成兩種鈉鹽。請回答下列問題:
(1)氣體A的化學式為 ,氣體單質D對應元素在周期表中的位置為 。
(2)寫出A溶于水生成弱酸B的化學方程式 。
(3)氣體A與NH3反應的化學方程式為 ,該反應體現氣體A具有 性。
(4)試寫出制取氣體A的化學方程式為 。
(5)設計實驗探究離子晶體C的成分為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年廣東省清遠市高二上學期10月月考化學試卷(解析版) 題型:選擇題
一定能使反應速率加快的因素是:①擴大容器的容積;②使用催化劑;③增加反應物的質量;④升高溫度;⑤縮小容積
A.②③ B.②③④ C.②③④⑤ D.④
查看答案和解析>>
科目:高中化學 來源:2016屆四川省高三上學期10月月考化學試卷(解析版) 題型:實驗題
酸性KMnO4溶液能與草酸(H2C2O4)溶液反應。某探究小組利用反應過程中溶液紫色消失快慢的方法來研究影響反應速率的因素。
Ⅰ.實驗前首先用濃度為0.1000mol•L-1酸性KMnO4標準溶液滴定未知濃度的草酸。
(1)寫出滴定過程中發生反應的離子方程式為 。
(2)滴定過程中操作滴定管的圖示正確的是 。
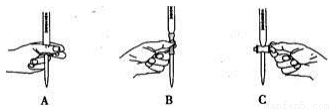
(3)若配制酸性KMnO4標準溶液時,俯視容量瓶的刻度線,會使測得的草酸溶液濃度 (填“偏高”、“偏低”、或“不變”)。
Ⅱ.通過滴定實驗得到草酸溶液的濃度為0.2000mol·L-1。用該草酸溶液按下表進行后續實驗(每次實驗草酸溶液的用量均為8mL)。
實驗編號 | 溫 度(℃) | 催化劑用量(g) | 酸性高錳酸鉀溶液 | 實驗目的 a.實驗1和2探究 b.實驗1 和3 探究反應物濃度對該反應速率的影響; c.實驗1 和4 探究催化劑對該反應速率的影響。 | |
體積(mL) | 濃度(mol•L-1) | ||||
1 | 25 | 0.5 | 4 | 0.1000 | |
2 | 50 | 0.5 | 4 | 0.1000 | |
3 | 25 | 0.5 | 4 | 0.0100 | |
4 | 25 | 0 | 4 | 0.1000 | |
(4)寫出表中a 對應的實驗目的 ;
(5)該小組同學對實驗1和3分別進行了三次實驗,測得以下實驗數據(從混合振蕩均勻開始計時):
實驗編號 | 溶液褪色所需時間(min) | ||
第1次 | 第2 次 | 第3 次 | |
1 | 14.0 | 13.0 | 11.0 |
3 | 6.5 | 6.7 | 6.8 |
分析上述數據后得出“當其它條件相同時,酸性高錳酸鉀溶液的濃度越小,褪色時間就越短,即反應速率就越快”的結論。某同學認為該小組“探究反應物濃度對速率影響”的實驗方案設計中存在問題,從而得到了錯誤的實驗結論,請簡述改進的實驗方案_________。
(6)該實驗中使用的催化劑應選擇MnSO4并非MnCl2,原因為(離子方程式表示) 為 。
查看答案和解析>>
科目:高中化學 來源:2016屆福建省晨曦、冷曦、正曦、岐濱四校高三第二次聯考理綜化學試卷(解析版) 題型:選擇題
NA表示阿伏加德羅常數,下列敘述正確的是
A.1 mol FeI2與足量氯氣反應時轉移的電子數為2NA
B.0.2 mol S在空氣中充分燃燒,轉移電子數為0.6NA
C.0.1molCl2與足量的水充分反應,轉移電子數為0.1NA
D.1.5 mol Na2O2與足量的二氧化碳充分反應,轉移電子數為1.5NA
查看答案和解析>>
科目:高中化學 來源:2016屆福建省高三上學期期中測試化學試卷(解析版) 題型:實驗題
(12分)某校課外小組為測定某碳酸鈉和碳酸氫鈉混合物中碳酸鈉的質量分數,甲、乙兩組同學分別進行了下列相關實驗.
方案Ⅰ.甲組同學用質量法,按如下圖所示的實驗流程進行實驗:

(1)實驗時,蒸發結晶操作中,除了酒精燈外,還要用到的儀器是
(2)有同學認為“加入適量鹽酸”不好操控,應改為“過量鹽酸”,便于操作且不影響測定的準確性,你認為對或錯 ,為什么
(3)若實驗中測得樣品質量為46.4g,固體質量為40.95g,則碳酸鈉的質量分數為 .(保留3位有效數字)
(4)蒸發結晶過程中若有固體飛濺,測得碳酸鈉的質量分數 (填偏大 偏小 無影響).
方案Ⅱ:乙組同學的主要實驗流程圖如下:
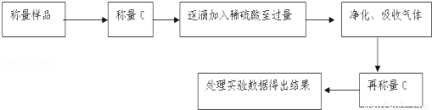
按如下圖所示裝置進行實驗:
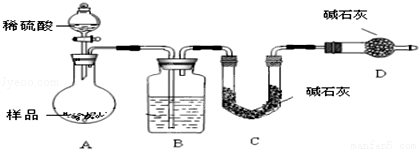
(5)在C中裝堿石灰來吸收凈化后的氣體.D裝置的作用是 .
(6)有的同學認為為了減少實驗誤差,在反應前后都通入N2,反應后通入N2的目的是 .
方案Ⅲ:氣體分析法
(7)把一定量樣品與足量稀硫酸反應后,用如圖裝置測量產生CO2氣體的體積,B溶液最好采用 (以下選項中選擇)使測量誤差較小.
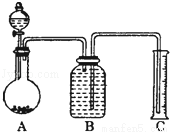
A.飽和碳酸鈉溶液 B.飽和碳酸氫鈉溶液
C.飽和氫氧化鈉溶液 D.飽和硫酸銅溶液
查看答案和解析>>
科目:高中化學 來源:2016屆河南省英文學校高三上學期期中測試化學試卷(解析版) 題型:選擇題
下列實驗過程中產生沉淀的物質的量(Y) 與加入試劑的量(X)之間的關系正確的是
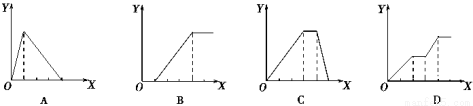
A.向AlCl3溶液中逐滴加入NaOH溶液至過量且邊滴邊振蕩
B.向NaAlO2溶液中滴加稀鹽酸至過量且邊滴邊振蕩
C.向NH4Al(SO4)2溶液中逐滴加入氫氧化鈉溶液直至過量
D.向NaOH、Ba(OH)2、NaA1O2的混合溶液中逐漸通入二氧化碳至過量
查看答案和解析>>
科目:高中化學 來源:2016屆江蘇省高三上學期第一次月考化學試卷(解析版) 題型:填空題
(14分)FeCl3 具有凈水作用,但腐蝕設備,而聚合氯化鐵是一種新型的絮凝劑,處理污水比FeCl3 高效,且腐蝕性小。請回答下列問題:
(1)FeCl3 凈水的原理是 。FeCl3 溶液腐蝕鋼鐵設備,除H+作用外,另一主要原因是(用離子方程式表示) 。
(2)為節約成本,工業上用NaClO3 氧化酸性FeCl2 廢液得到FeCl3 。
①若酸性FeCl2 廢液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,則該溶液的PH約為 。
②完成NaClO3 氧化FeCl2 的離子方程式:
 ClO3-+
ClO3-+ Fe2++
Fe2++  =
=  Cl-+
Cl-+  Fe3++
Fe3++  .
.
(3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反應的平衡常數K1、K2、K3由大到小的順序是 。
通過控制條件,以上水解產物聚合,生成聚合氧化鐵,離子方程式為:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移動可采用的方法是(填序號) 。
a.降溫 b.加水稀釋 c.加入NH4Cl d.加入NaHCO3
室溫下,使氯化鐵溶液轉化為高濃度聚合氯化鐵的關鍵條件是 。
(4)天津某污水處理廠用氯化鐵凈化污水的結果如下圖所示。由圖中數據得出每升污水中投放聚合氯化鐵[以Fe(mg·L-1)表示]的最佳范圍約為 mg·L-1。
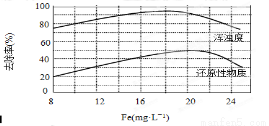
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省高三上學期期中測試化學試卷(解析版) 題型:選擇題
用試紙檢驗氣體性質是一種重要的實驗方法。如下表所示的實驗中(可加熱),下列試紙的選用、現象、對應結論都正確的一項是
選項 | 物質 | 試紙名稱 | 現象 | 性質 |
A | Na2SO3、硫酸 | 品紅試紙 | 褪色 | SO2具有漂白性 |
B | 濃氨水、生石灰 | 藍色石蕊溶液 | 變紅 | 氨氣為堿性氣體 |
C | 碘水 | 淀粉試紙 | 變藍 | 碘具有氧化性 |
D | Cu、濃硝酸 | KI淀粉試紙 | 變藍 | NO2為酸性氣體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com