
| A. | 1mol甲基所含有的電子數(shù)為10NA | |
| B. | 標準狀況下,11.2L氯仿(CHCl3)中含有C-Cl鍵的數(shù)目為1.5NA | |
| C. | 2.8 g乙烯和丙烯的混合氣體中所含碳原子數(shù)為0.2 NA | |
| D. | 6.0g冰醋酸與4.6g乙醇反應生成乙酸乙酯的分子數(shù)為0.1 NA |
分析 A.甲基中含有9個電子,1mol甲基中含有9mol電子;
B.標準狀況下氯仿的狀態(tài)不是氣體;
C.乙烯和丙烯的最簡式為CH2,根據(jù)最簡式計算出混合氣體的中含有的碳原子數(shù)目;
D.根據(jù)酯化反應是可逆反應進行判斷.
解答 解:A.甲基的電子式為: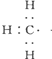 ,1mol甲基中含有9mol電子,含9NA個電子,故A錯誤;
,1mol甲基中含有9mol電子,含9NA個電子,故A錯誤;
B.在標準狀況下氯仿不是氣體,無法計算11.2L氯仿的物質(zhì)的量,故B錯誤;
C.2.8g乙烯和丙烯的混合物中含有0.2mol最簡式CH2,含有碳原子的物質(zhì)的量為0.2mol,所含碳原子數(shù)為0.2NA,故C正確;
D.6.0g冰醋酸與4.6g乙醇發(fā)生酯化反應,應為酯化反應為可逆反應,所以生成乙酸乙酯的分子數(shù)小于0.1NA,故D錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數(shù)的判斷及計算,題目難度中等,注意掌握阿伏伽德羅常數(shù)的概念,明確阿伏伽德羅常數(shù)與物質(zhì)的量、摩爾質(zhì)量等物理量之間的關系,明確標況下氣體摩爾體積的使用條件.


 文敬圖書課時先鋒系列答案
文敬圖書課時先鋒系列答案科目:高中化學 來源: 題型:選擇題
| A. | 2.4g金屬鎂變成鎂離子時失去的電子數(shù)為0.1NA | |
| B. | 標準狀況下,11.2LCCl4所含的分子數(shù)為0.5NA | |
| C. | 0.5mol/LAlCl3溶液中Cl-的數(shù)目為2NA | |
| D. | 17g氨氣中含有的電子數(shù)為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃,由水電離出的c(H+)=10-11mol/L的溶液:Na+、K+、Cl-、ClO- | |
| B. | 與Al反應能放出氫氣的溶液:Na+、Ba2+、NO3-、Cl- | |
| C. | 甲基橙變紅的溶液:Na+、Mg2+、SO42-、Cl- | |
| D. | 含Al3+的溶液:K+、Ca2+、Cl-、S2- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①③ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 圖1:石油分餾 | B. | 圖2:配制150mL 0.1mol/L鹽酸 | ||
| C. | 圖3:燒瓶內(nèi)溶液變藍色 | D. | 圖4:探究NaHCO3的熱穩(wěn)定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 溫度(℃) 平衡態(tài) | 260 | 270 | 280 | 290 | 300 | 310 |
| CO轉(zhuǎn)化率(%) | 92 | 87 | 82 | 80 | 72 | 62 |
| CH3OCH3產(chǎn)率(%) | 33 | 45 | 77 | 79 | 62 | 52 |
| A. | 反應①、②均為吸熱反應 | |
| B. | 290℃時反應②K值達到最大 | |
| C. | 平衡時,反應①與②中CH3OH的消耗速率一定相等 | |
| D. | 增大壓強能增大CH3OCH3產(chǎn)率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na$→_{點燃}^{O_{2}}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 | |
| B. | MgCO3$\stackrel{HCl}{→}$MgCl2溶液$\stackrel{電解}{→}$Mg | |
| C. | Fe$→_{點燃}^{O_{2}}$Fe2O3$\stackrel{H_{2}SO_{4}}{→}$Fe2(SO4)3 | |
| D. | SiO2$\stackrel{HCl}{→}$SiCl4$\stackrel{H_{2}}{→}$Si |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com