
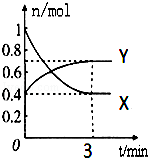
 在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應:2NO2(g)(紅棕色)?N2O4g)(無色),如圖所示.
在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應:2NO2(g)(紅棕色)?N2O4g)(無色),如圖所示.分析 (1)根據物質的量的變化量之比等于計量數之比分析;
(2)溫度降低,反應速率的減慢;
(3)根據反應速率之比等于化學計量數之比比較;
(4)根據v=$\frac{△c}{△t}$計算反應速率,結合圖象計算相關物理量;
(5)根據可逆反應處于平衡狀態時,正逆反應速率相等、組成不變等特征判斷.
解答 解:(1)由方程式2NO2 (g) (紅棕色)?N2O4g)(無色),可知反應中NO2 的物質的量變化較大,則X表示NO2的物質的量隨時間的變化曲線;
故答案為:X;
(2)溫度降低,正逆反應速率都減慢;
故答案為:減慢;減慢;
(3)(3)分別測得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),v(NO2)=2v(N2O4)=0.6mol•L-1•min-1=0.01mol/(L•s),則甲反應較快,
故答案為:甲;
(4)分析圖象可知在0到3min中內N2O4的物質的量從0.4mol變為0.7mol,則其反應速率v=$\frac{△c}{△t}$=
$\frac{(0.7mol-0.4mol)÷2L}{3min}$=0.05mol/(L•min);
故答案為;0.05mol/(L•min);
(5)A.v(NO2)=2v(N2O4),未體現正與逆的關系,故錯誤;
B.該反應是個體積變化的可逆反應,容器內壓強不再發生變化,說明達平衡狀態,故正確;
C.X的體積分數不再發生變化,說明達平衡狀態,故正確;
D.容器內氣體原子總數不再發生變化,根據質量守恒,從反應發生容器中原子總數就不變,所以不能作平衡狀態的標志,故錯誤;
E. 只要反應發生就符合相同時間內消耗n mol的Y的同時生成2n mol的X,所以不一定達平衡狀態,故錯誤;
F.相同時間內消耗n mol的Y對于X就是生成2n mol,同時又消耗2n mol的X,說明正逆反應速率相等,達平衡狀態,故正確;
故答案為:BCF.
點評 本題考查了化學平衡狀態的判斷,轉化率的計算,以及速率快慢的比較,較為綜合,題目難度中等,注意把握化學反應速率以及化學平衡的基本知識即可解答該題.


科目:高中化學 來源: 題型:選擇題
| A. | 將集有氨氣的試管倒扣于水槽中,液體迅速充滿試管,說明氨氣極易溶于水 | |
| B. | 將濕潤的紅色石蕊試紙放入集有氨氣的集氣瓶中,試紙由紅色變為藍色,說明氨水呈堿性 | |
| C. | 加熱NH4HCO3固體,觀察到固體逐漸減少,試管口有液滴產生,說明NH4HCO3受熱不穩定 | |
| D. | 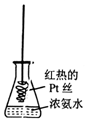 將紅熱的Pt絲伸入如圖所示的錐形瓶中,瓶口出現少量紅棕色氣體,說明氨氣的直接氧化產物為NO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5<pH<7.1 | B. | 7.1<pH<9 | C. | 3<pH<7.1 | D. | 7.1<pH<11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某溫度下,Ksp(AgCl)=1.8×10-10,Ksp (Ag2CrO4)=1.9×10-12,故Ag2CrO4更難溶 | |
| B. | 在CaCO3飽和溶液中,加入CaCl2固體,沉淀溶解平衡逆向移動,溶液中Ca2+濃度減小 | |
| C. | 溶度積常數Ksp與溫度有關,溫度越高,溶度積越大 | |
| D. | 在AgCl飽和溶液中,加入AgCl固體,平衡不移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 名稱 | 相對分子質量 | 性狀 | 熔點 | 沸點 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 無色液體易燃易揮發 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片狀或針狀晶體 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
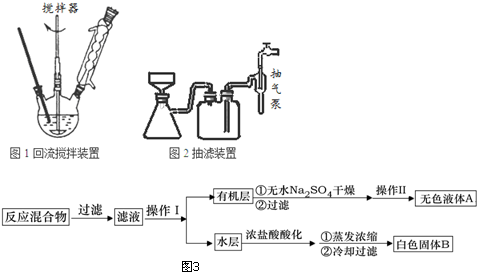
 ;操作Ⅱ為蒸餾.
;操作Ⅱ為蒸餾.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
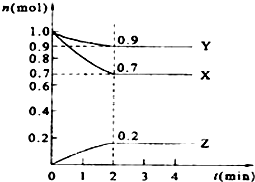 某溫度時,在2L的密閉容器中,X、Y、Z三種物質的量隨時間的變化曲線如圖所示.
某溫度時,在2L的密閉容器中,X、Y、Z三種物質的量隨時間的變化曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
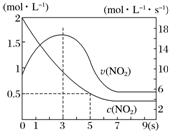 某絕熱恒容容器中充入2mol•L-1 NO2,發生反應2NO2(g)═N2O4(g)△H=-56.9kJ•mol-1.下列分析不正確的是( )
某絕熱恒容容器中充入2mol•L-1 NO2,發生反應2NO2(g)═N2O4(g)△H=-56.9kJ•mol-1.下列分析不正確的是( )| A. | 5s時NO2的轉化率為75% | |
| B. | 0~3 s時v(NO2)增大是由于體系溫度升高 | |
| C. | 3s時化學反應處于平衡狀態 | |
| D. | 9s時再充入N2O4,平衡后K較第一次平衡時大 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com