



科目:高中化學 來源: 題型:
 (2012?石家莊一模)常溫下,A為無色無味液體,B為淡黃色粉末,D、E、G、W為氣體,且G的相對分子質量比D大16,各物質間的轉化關系如圖所示:
(2012?石家莊一模)常溫下,A為無色無味液體,B為淡黃色粉末,D、E、G、W為氣體,且G的相對分子質量比D大16,各物質間的轉化關系如圖所示:| 9 |
| 4 |
| 物質 | A | D | G | W |
| 濃度/(mol?L-1) | 0.45 | 0.45 | 0.55 | 0.55 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、Z為0.35mol?L-1 | B、Y2為0.45mol?L-1 | C、X2為0.2 mol?L-1 | D、Z為0.4mol?L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、Z為0.3mol.L-1, | B、X2為0.2mol.L-1, | C、Y2為0.3mol.L-1, | D、Z為0.4mol.L-1, |
查看答案和解析>>
科目:高中化學 來源: 題型:
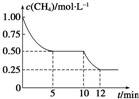 在密閉容器中進行反應CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,測得c(CH4)隨反應時間(t)的變化如圖所示.下列判斷不正確的是( )
在密閉容器中進行反應CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,測得c(CH4)隨反應時間(t)的變化如圖所示.下列判斷不正確的是( )| A、10min時,改變的外界條件可能是升高溫度 | B、0~10min內,v(H2)=0.15mol?L-1?min-1 | C、恒溫下,縮小容器體積,一段時間內v逆>v正 | D、12min時,反應達平衡的本質原因是氣體總質量不再變化 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com