
分析 (1)根據抗酸藥物有效成分能中和胃里過多的鹽酸分析;碳酸鎂和鹽酸反應生成氯化鎂和水、二氧化碳,氫氧化鋁和鹽酸反應生成氯化鋁和水;
(2)根據淀粉在人體內在酶的作用水解最終轉化成葡萄糖判斷;
(3)嚼碎后能增大固體表面積.
解答 解:(1)碳酸鎂、氫氧化鋁都能中和胃里過多的鹽酸;碳酸鎂與鹽酸反應生成氯化鎂、二氧化碳氣體和水,碳酸鎂需要保留化學式,反應的離子方程式為MgCO3+2HCl=MgCl2+H2O+CO2↑,氫氧化鋁和鹽酸反應生成氯化鋁和水,反應的離子方程式為:Al(OH)3+3HCl═AlCl3+3H2O,故答案為:MgCO3+2H+=Mg2++H2O+CO2↑;Al(OH)3+3H+═Al3++3H2O;
(2)淀粉在人體內在酶的作用水解最終轉化成葡萄糖,其分子式為:C6H12O6,故答案為:C6H12O6;
(3)嚼碎后能增大固體表面積,從而能加快與胃酸的反應速率.答:嚼碎后能增大固體表面積,加快反應速率.
點評 本題較為綜合,主要考查酸堿鹽之間的復分解反應及化學方程式的書寫等知識,注意利用化學知識來解決生活中的問題,注意化學方程式的書寫重要知識點,題目難度不大.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
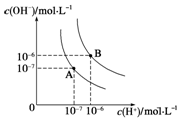 水的電離平衡曲線如圖所示,若A點、B點分別表示25℃和100℃時水的電離達平衡時的離子濃度.則表示25℃的是A (填“A”或“B”).100℃時,在1mol•L-1的NaOH溶液中,由水電離出的c(H+)=1×10-12mol•L-1.100℃時,5×10-5 mol•L-1的H2SO4溶液與pH=9的Ba(OH)2溶液混合后pH=7,則混合前H2SO4溶液與Ba(OH)2溶液的體積比為9:1.
水的電離平衡曲線如圖所示,若A點、B點分別表示25℃和100℃時水的電離達平衡時的離子濃度.則表示25℃的是A (填“A”或“B”).100℃時,在1mol•L-1的NaOH溶液中,由水電離出的c(H+)=1×10-12mol•L-1.100℃時,5×10-5 mol•L-1的H2SO4溶液與pH=9的Ba(OH)2溶液混合后pH=7,則混合前H2SO4溶液與Ba(OH)2溶液的體積比為9:1.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
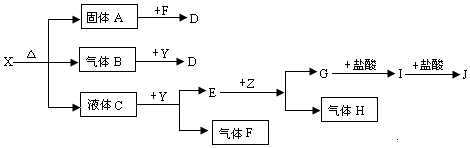
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 密度比4:11 | B. | 分子數之比為4:11 | ||
| C. | 體積比4:11 | D. | 物質的量之比為4:11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Mg2+、MnO4-、SO42- | B. | NH4+、Al3+、NO3-、Cl- | ||
| C. | K+、Na+、AlO2-、NO3- | D. | Mg2+、K+、HCO3-、OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在紫外線、飽和(NH4)2SO4溶液、CuSO4溶液、福爾馬林等作用下,蛋白質均會發(fā)生變性 | |
| B. | 用新制Cu(OH)2懸濁液可鑒別麥芽糖和蔗糖 | |
| C. | 為檢驗皂化反應進行程度,取幾滴反應液,滴入裝有熱水的試管中,震蕩,若有油滴浮在液面上,說明油脂已完全反應 | |
| D. | CH3CH2Br中滴加AgNO3溶液觀察是否有淺黃色沉淀,判斷鹵代烴的類型 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
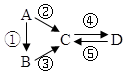
| A. | 若A是大氣中含量最多的氣體,C、D是氧化物且會造成光化學污染.則D轉化成C的反應化學方程為3NO2+H2O=2HNO3+2NO | |
| B. | 若A、B、C分別為C(s)、CO(g)和CO2(g),且通過與O2(g)反應實現圖示的轉化.在同溫同壓且消耗含碳物質均為1mol時,反應①、②、③的焓變依次為△H1、△H 2、△H 3,則它們之間的關系為△H 2=△H1+△H 3 | |
| C. | 若C為一元強堿且陰、陽離子所含的電子數相同,D為日常生活中常用的調味品,工業(yè)上用D制備A的化學方程式2Na2O(熔融)$\frac{\underline{\;通電\;}}{\;}$4Na+O2↑ | |
| D. | 若A是應用最廣泛的金屬.④反應用到A,②、⑤反應均用到同一種氣態(tài)非金屬單質實驗室保存D溶液的方法是加入適量鐵粉與適量鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在0.2 mol•L-1的Na2CO3溶液中含有Na+的數目為0.4NA | |
| B. | 0.1 mol Fe參加氧化還原反應,轉移的電子數目一定是0.3 NA | |
| C. | 15.6 g Na2O2 與過量CO2反應時,轉移的電子數為0.4NA | |
| D. | 標準狀況下22.4 L CH4和C2H4的混合氣體所含氫原子數為4NA |
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com