
【題目】下列化工生產過程中,未涉及氧化還原反應的是( )
A.海帶提碘
B.氯堿工業
C.煅燒石灰石制取生石灰
D.海水提溴
科目:高中化學 來源: 題型:
【題目】將足量的KHCO3溶液不斷滴入含等物質的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物質的量與滴入的KHCO3溶液體積的關系可表示為
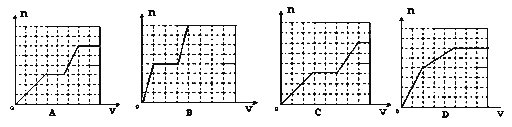
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦、鉻、鐵、鎳、銅等金屬及其化合物在工業上有重要用途。
(1)鈦鐵合金是鈦系儲氫合金的代表,該合金具有放氫溫度低、價格適中等優點。
①Ti的基態原子價電子排布式為________________。
②Fe的基態原子共有________種不同能級的電子。
(2)制備CrO2Cl2的反應為K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化學方程式中非金屬元素電負性由大到小的順序是______________(用元素符號表示)。
②COCl2分子中所有原子均滿足8電子構型,COCl2分子中σ鍵和π鍵的個數比為____________,中心原子的雜化方式為____________。
(3)NiO、FeO的晶體結構均與氯化鈉的晶體結構相同,其中Ni2+和Fe2+的離子半徑分別為6.9×10-2 nm和7.8×10-2 nm。則熔點:NiO____________(填“>”、“<”或“=”)FeO。
(4)Ni和La的合金是目前使用廣泛的儲氫材料,具有大容量、高壽命、耐低溫等特點,在日本和中國已實現了產業化。該合金的晶胞結構如圖所示。
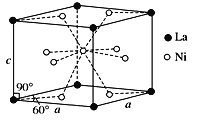
①該晶體的化學式為________________。
②已知該晶胞的摩爾質量為M g·mol-1,密度為d g·cm-3。設NA為阿伏加德羅常數的值,則該晶胞的體積是____________cm3(用含M、d、NA的代數式表示)。
[化學—選修5:有機化學基礎]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活息息相關。下列敘述正確的是( )
A.鮮榨橙汁遇到碘水會變藍 B.饅頭越嚼越甜
C.油脂經水解可變成葡萄糖 D.土豆中的淀粉經水解可變成酒(乙醇)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在反應X+2Y=R+2M中,已知R和M的摩爾質量之比為22:9,當1.6gX與Y完全反應后,生成4.4gR。則在此反應中Y和M的質量之比為
A.16:9 B.23:9 C.32:9 D. 46:9
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于淀粉和纖維素的敘述,正確的是( )
A.因為都屬于糖,所以都具有甜味
B.人體內有催化淀粉和纖維素水解的酶
C.兩者都能在一定條件下水解生成葡萄糖
D.因為二者都是由多個單糖分子按照一定的方式在分子間脫水結合而成,所以都用(C6H10O5)n表示,因此它們是同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制一定體積一定濃度的NaOH溶液時,下列操作導致結果偏高的是
A.稱量NaOH固體時動作緩慢 B.定容時俯視刻度線
C.定容后振蕩發現液面低于刻度線 D.未洗滌燒杯和玻璃棒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下存在反應:CO(g)+H2O(g)![]() CO2(g)+H2(g),ΔH<0。現有三個相同的2L恒
CO2(g)+H2(g),ΔH<0。現有三個相同的2L恒
容絕熱(與外界沒有熱量交換) 密閉容器I、II、III,在I中充入1 mol CO和1 mol H2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO 和2 mol H2O,700℃條件下開始反應。達到平衡時,下列說法正確的是( )
A. 容器I、II中正反應速率相同
B. 容器I中CO 的物質的量比容器II中的多
C. 容器I、III中反應的平衡常數相同
D. 容器I中CO 的轉化率與容器II中CO2的轉化率之和等于1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳、氮及其化合物在工農業生產生活中有著重要作用,請回答下列問題:
(1)用CH4催化還原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
若2 molCH4還原NO2至N2,整個過程中放出的熱量為1734 kJ,則△H2=_________;
(2)據報道,科學家在一定條件下利用Fe2O3與甲烷反應可制取“納米級”的金屬鐵,其反應如下:Fe2O3(s)+3CH4(g)===2Fe(s)+3CO(g)+6H2(g) △H>0
① 若反應在5 L的密閉容器中進行,1 min后達到平衡,測得Fe2O3在反應中質量減少3.2g。則該段時間內CO的平均反應速率為__________mol/(L·s)
② 若該反應在恒溫恒壓容器中進行,能表明該反應達到平衡狀態的是__________(選填序號)
A.CH4的轉化率等于CO的產率
B.混合氣體的平均相對分子質量不變
c.v(CO)與v(H2)的比值不變
D.固體的總質量不變
③該反應達到平衡時某物理量隨溫度變化如圖所示,當溫度由T1升高到T2時,平衡常數KA________KB(填“>”、“<”或“=”),縱坐標表示的物理量可能是__________(填字母)。
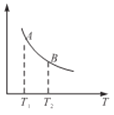
A.H2的逆反應速率
B.CH4的的體枳分數
C.混合氣體的平均相對分子質量
D.CO的體積分數
(3)而一些科學家采用高質子導電性的SCY陶瓷(能傳遞H+)實現氨的電化學合成,從而大大提高了氮氣和氫氣的轉化率。電化學合成氨過程的總反應式為N2+3H2![]() 2NH3,該過程中還原反應的方程式為________________。
2NH3,該過程中還原反應的方程式為________________。
(4)若往20 mL0.01mol/L的弱酸HNO2溶液中逐滴加入一定濃度的燒堿溶液,測得混合溶液的溫度變化如下圖所示,下列有關說法正確的是_____________(填標號)
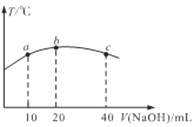
①該燒堿溶液的濃度為0.02mol/L
②該燒堿溶液的濃度為0.01mol/L
③HNO2的電離平衡常數:b點>a點
④從b點到c點,混合溶液中一直存在:c(Na+)> c(NO2-) >c(OH-)> c(H+)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com