
| A. | .①②③ | B. | ②③ | C. | ① | D. | 全部 |
分析 金屬元素的化合價一定是正價,因而其原子只有還原性,但其離子不一定只有氧化性,如Fe2+就有還原性,金屬元素難以得到電子,在化學反應中只能失去電子,金屬性越強的元素相應的離子氧化性越弱,在金屬和非金屬分界線附近的金屬一般具有金屬性和非金屬性.
解答 解:①對于多價金屬離子來說,較低價態的金屬離子既有氧化性又有還原性,例Fe2+,Fe2++Zn=Fe+Zn2+,2Fe2++Cl2═2Fe3++2Cl-,故①錯誤;
②因為金屬元素的原子只具有還原性,故在化合物中只顯正價,故②正確;
③金屬性越強的元素越易失去電子,單質的還原性越強,對應的離子越難以得電子,氧化性越弱,故③正確;
④金屬性強弱和失電子能力有關,與失電子數多少無關,如Na失去一個電子形成鈉離子,Al失去3個電子形成鋁離子,鈉金屬性強,所以失電子數越多,元素的金屬性不一定越強,故④錯誤.
故選B.
點評 本題考查金屬的性質,題目難度中等,注意對于此類結論性判斷,只要能舉出相反的例子,即可證明敘述錯誤.


 智能訓練練測考系列答案
智能訓練練測考系列答案科目:高中化學 來源: 題型:選擇題
 北京奧運會期間對大量盆栽鮮花施用了S-誘抗素制劑,以保持鮮花盛開.S-誘抗素的分子結構如圖,下列關于該分子說法不正確的是( )
北京奧運會期間對大量盆栽鮮花施用了S-誘抗素制劑,以保持鮮花盛開.S-誘抗素的分子結構如圖,下列關于該分子說法不正確的是( )| A. | 1mol該有機物可與2mol鈉反應 | |
| B. | 該有機物可以發生酯化、加成、醇催化氧化 | |
| C. | 1mol碳酸鈉可與2mol該物質反應產生1mol二氧化碳 | |
| D. | 該有機物中含有碳碳雙鍵、羥基、羧基等官能團 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(NH4+)>c(SO42-),c(OH-)>c(H+) | B. | c(NH4+)=c(SO42-),c(OH-)=c(H+) | ||
| C. | c(NH4+)>c(SO42-),c(H+)>c(OH-) | D. | c(SO42-)>c(NH4+),c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ; (2)鋁離子的結構示意圖:
; (2)鋁離子的結構示意圖: ;
;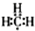
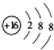 ; (6)NH4Cl的電子式:
; (6)NH4Cl的電子式: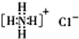 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
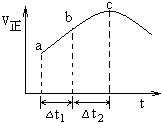 向絕熱恒容密閉容器中通入SO2和NO2,在一定條件下使反應SO2(g)+NO2(g)═SO3(g)+NO(g)達到平衡,正反應速率隨時間變化的示意圖如圖所示.由圖可得出的正確結論是( )
向絕熱恒容密閉容器中通入SO2和NO2,在一定條件下使反應SO2(g)+NO2(g)═SO3(g)+NO(g)達到平衡,正反應速率隨時間變化的示意圖如圖所示.由圖可得出的正確結論是( )| A. | 該反應為放熱反應 | |
| B. | 反應物濃度:c>b>a | |
| C. | a、b均未建立平衡,c點恰好達到平衡 | |
| D. | 若在恒溫恒容容器中,以相同的投料進行該反應,平衡后轉化率小于絕熱恒容容器中的轉化率 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,氯化鈣
,氯化鈣 ,硫化氫 結構式:H-S-H.以上三種物質中其中屬于共價化合物的是H2S,晶體類型為分子晶體.
,硫化氫 結構式:H-S-H.以上三種物質中其中屬于共價化合物的是H2S,晶體類型為分子晶體.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
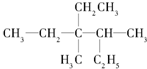 用系統命名法命名:3,4-二甲基-3-乙基己烷
用系統命名法命名:3,4-二甲基-3-乙基己烷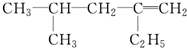
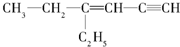 ,分子中飽和碳原子數為4,可能在同一平面上的碳原子數最多為8
,分子中飽和碳原子數為4,可能在同一平面上的碳原子數最多為8查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2CO3、NaHCO3、NaCl、HCl | B. | Na2CO3、NaHCO3、HCl、NaCl | ||
| C. | (NH4)2SO4、NH4Cl、NaNO3、Na2CO3 | D. | NH4Cl、(NH4)2SO4、Na2CO3、NaNO3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com