
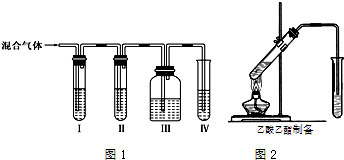
| 濃硫酸 |
| △ |
| 濃硫酸 |
| △ |


 期末1卷素質教育評估卷系列答案
期末1卷素質教育評估卷系列答案科目:高中化學 來源: 題型:
| A、離子半徑:Na+>Mg2+>Al3+>Cl-;原子半徑:Na>Mg>Al>Cl |
| B、穩定性:HF>H2O>NH3>CH4; 還原性:HF<H2O<NH3<CH4 |
| C、堿性:CsOH>KOH>Mg(OH)2>NaOH; 金屬性:Cs>K>Mg>Na |
| D、酸性:HClO>H2SO4>H2CO3;非金屬性Cl>S>C |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
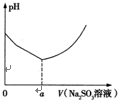 銅合金及銅的氯化物在生產生活中有著廣泛的應用.請回答下列問題:
銅合金及銅的氯化物在生產生活中有著廣泛的應用.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com