
【題目】金是一種用途廣泛的貴重金屬。某化工廠利用氰化法從一種含金礦石中提取金的工藝流程如下:
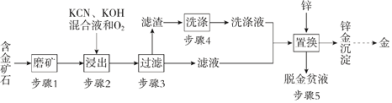
資料:
① Zn + ![]() O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2
② Zn2+(aq) ![]() Zn(CN)2(s)
Zn(CN)2(s) ![]() Zn(CN)42-(aq)
Zn(CN)42-(aq)
(1)步驟2中發生的反應有:
① 2Au(s) + 4CN-(aq) + 2H2O(l) + O2(g) = 2Au(CN)2-(aq) + 2OH-(aq) + H2O2(aq) H = -197.61 kJ·mol-1
② 2Au(s) + 4CN-(aq)+ H2O2(aq) = 2Au(CN)2-(aq) + 2OH-(aq) H = -386.93 kJ·mol-1
則2Au(s)+ 4CN-(aq)+ H2O(l) + 1/2O2(g) = 2Au(CN)2-(aq) + 2OH-(aq)的H =_______。
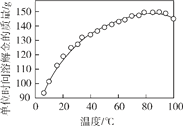
(2)下圖是步驟2中金的溶解速率與溫度的關系。80℃以后溶解速率降低的原因是___________。
(3)步驟4的目的是_________________。
(4)步驟5置換的總反應是:
2Au(CN)2- + 3Zn + 4CN- + 2H2O = 2Au + 2Zn(CN)42- + ZnO22- + 2H2↑
則以下說法正確的是________(填字母序號)。
A 步驟5進行時要先脫氧,否則會增加鋅的用量
B 若溶液中c(CN-)過小,會生成Zn(CN)2,減緩置換速率
C 實際生產中加入適量Pb(NO3)2的目的是形成原電池加快置換速率
(5)脫金貧液(主要含有CN-)會破壞環境,影響人類健康,可通過化學方法轉化為無毒廢水凈化排放。堿性條件下,用Cl2將貧液中的CN-氧化成無毒的CO2和N2,該反應的離子方程式為_______________。
【答案】-292.27kJ·mol-1 溫度太高會減小O2的溶解度,使c(O2)減小,[或溫度太高會使H2O2分解,c(H2O2)減小],金的溶解速率降低 提高金的浸出率(或提高金的產率,或減小金的損失,合理即可) ABC 2CN- + 5Cl2 + 8OH- === 2CO2↑ + N2↑ + 10Cl- + 4H2O
【解析】
含金礦石經磨礦粉碎后加入KCN、KOH混合液,并通入氧氣,反應生成Au(CN)2-,過濾,將濾渣洗滌,在濾液中加入Zn置換,可生成Zn、Au沉淀,加入酸除去鋅,可得到金,以此解答該題。
(1)根據蓋斯定律分析解答;
(5)根據題意寫出反應物和生成物,結合氧化還原反應方程式的配平方法書寫方程式。。
(1)①2Au(s)+4CN-(aq)+2H2O(l)+O2(g)═2Au(CN)2-(aq)+2OH-(aq)+H2O2(aq) △H=-197.61kJmol-1,②2Au(s)+4CN-(aq)+H2O2(aq)═2Au(CN)2-(aq)+2OH-(aq) △H=-386.93kJmol-1,根據蓋斯定律,將![]() 可得2Au(s)+4CN-(aq)+H2O(l)+
可得2Au(s)+4CN-(aq)+H2O(l)+![]() O2(g)═2Au(CN)2-(aq)+2OH-(aq) △H=-292.27 kJmol-1,故答案為:-292.27kJmol-1;
O2(g)═2Au(CN)2-(aq)+2OH-(aq) △H=-292.27 kJmol-1,故答案為:-292.27kJmol-1;
(2)溫度越高,氣體在水中的溶解度越小。溫度較高時,導致氧氣的溶解度減小,同時也導致過氧化氫分解,使過氧化氫的濃度降低,金的溶解速率降低,故答案為:溫度太高會減小O2的溶解度,使c(O2)減小[或溫度太高會使H2O2分解,c(H2O2)減小],金的溶解速率降低;
(3)步驟4是洗滌沉淀,可提高金的浸出率(或提高金的產率,或減小金的損失),故答案為:提高金的浸出率(或提高金的產率,或減小金的損失);
(4)A.氧氣可氧化鋅,則步驟5進行時要先脫氧,否則會增加鋅的用量,故A正確;B.若溶液中c(CN-)過小,會生成Zn(CN)2,Zn(CN)2為固體,難溶于水,會減緩置換速率,故B正確;C.實際生產中加入適量Pb(NO3)2,鋅置換出Pb,可形成原電池,加快置換速率,故C正確;故答案為:ABC;
(5)堿性條件下,用Cl2將脫金貧液(主要含有CN-)中的CN-氧化成無毒的CO2和N2,該反應的離子方程式為2CN-+5Cl2+8OH-═2CO2↑+N2↑+10Cl-+4H2O,故答案為:2CN-+5Cl2+8OH-═2CO2↑+N2↑+10Cl-+4H2O。


科目:高中化學 來源: 題型:
【題目】磷化氫(PH3)是一種劇毒氣體,是最常用的高效熏蒸殺蟲劑,也是一種電子工業原料。
(1)PH3的電子式為______________。
(2)在密閉糧倉放置的磷化鋁(AlP)片劑,遇水蒸氣放出PH3氣體,該反應的化學方程式為:_____。
(3)PH3的一種工業制法涉及的物質轉化關系如下圖所示:

①次磷酸屬于____元酸,亞磷酸屬于____元酸;
②當反應I生成的n(NaH2PO2):n(Na2HPO3) =3:1時,參加反應的n(P4):n(NaOH)= ____。
(4)一種用于處理PH3廢氣的吸收劑成分為次氯酸鈣80%、鋸木屑(疏松劑)15%、活性炭 2.5%、滑石粉(防結塊)2.5%。
①次氯酸鈣將PH3氧化為H3PO4的化學方程式為_______________________________;
②空氣中的水蒸氣可加快PH3的氧化過程,其原因可能是_______________________。
(5)從(4)中的吸收殘留物中回收磷酸氫鈣(CaHPO4)的方法如下:

①試劑x為_________填化學式);
②已知25℃時,H3 PO4的Kal=7.5×10-3、Ka2=6.3×10-8、Ka3 =4.4×10-13。加入Y時,應控制懸濁液pH____7(填“>”、“=”或“<”),通過計算說明理由:________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z為原子序數依次增大的前四周期元素,元素W是宇宙中最豐富的元素,元素X的原子最外層電子數是其內層的3倍,元素Z的基態原子核外電子有24種運動狀態,Y、X、Z不在同一周期,且Y原子核外p電子比s電子多5個。
(1)Z基態原子的核外電子排布式為__________。
(2)Z的氧化物是石油化工中重要的催化劑之一,如催化異丙苯(![]() )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1mol丙烯分子中含有σ鍵與π鍵數目之比為_______。
②苯分子中碳原子軌道的雜化類型為__________。
③Z的一種氧化物ZO5中,Z的化合價為+6,則其中過氧鍵的數目為_______個。
(3)W、X、Y三種元素的電負性由小到大順序為__________。(請用元素符號回答)
(4)ZY3熔點為1152℃,熔融狀態下能夠導電,據此可判斷ZY3晶體屬于__________(填晶體類型)。
(5)ZX2晶體的晶胞結構如圖,每個Z原子周圍最近的X 原子數目為__________。若該化合物的相對分子質量為M,晶胞邊長為acm,阿伏加德羅常數為NA,則該晶體的密度為_________g/cm3。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鹽酸普魯卡因 ( 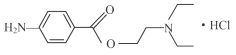 ) 是一種良好的局部麻醉藥, 具有毒性小, 無成癮性等特點。其合成路線如下圖所示:
) 是一種良好的局部麻醉藥, 具有毒性小, 無成癮性等特點。其合成路線如下圖所示:

回答下列問題:
(1) 3molA可以合成1molB, 且B是平面正六邊形結構, 則B的結構簡式為_________。
(2) 有機物C的名稱為____________, B→C的反應類型為_____________。
(3) 反應C→D的化學方程式為________________________________________。
(4) F和E發生酯化反應生成G, 則F的結構簡式為___________________。
(5) H的分子式為____。
(6) 分子式為C9H12且是C的同系物的同分異構體共有__________種。
(7) 請結合上述流程信息, 設計由苯、 乙炔為原料合成 的路線_______________ 。(其他無機試劑任選)
的路線_______________ 。(其他無機試劑任選)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數,下列敘述正確的是( )
A. 64 g SO2含有氧原子數為1NA
B. 物質的量濃度為0.5 mol·L-1的MgCl2溶液,含有Cl-數為1 NA
C. 標準狀況下,22.4 L H2O的分子數為1NA
D. 常溫常壓下,14 g N2含有分子數為0.5 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Mg–AgCl電池是一種以海水為電解質溶液的水激活電池。如圖用該水激活電池為電源電解NaCl溶液的實驗中,X電極上有無色氣體逸出。下列有關分析正確的是

A. II為正極,其反應式為Ag+ + e– =Ag
B. 水激活電池內Cl–由正極向負極遷移
C. 每轉移1 mole-,U型管中消耗0. 5mol H2O
D. 開始時U型管中Y極附近pH逐漸增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用AG表示溶液酸度:![]() 。在室溫下,用 0.1molL-1的NaOH溶液滴定20.00mL 0.1molL-1的CH3 COOH溶液,滴定結果如圖所示。下列分析正確的是
。在室溫下,用 0.1molL-1的NaOH溶液滴定20.00mL 0.1molL-1的CH3 COOH溶液,滴定結果如圖所示。下列分析正確的是

A. 0.1molL-1的CH3 COOH溶液的pH=3.4
B. A點加入的NaOH溶液的體積為20.00mL
C. 滴定過程中,c(CH3COO-)/c(H+)逐漸減小
D. B點溶液中可能存在c(Na+)>c(CH3COO-)> c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用下列實驗裝置能達到實驗目的的是
A.  分離CH3COOH和CH3COOC2H5混合液
分離CH3COOH和CH3COOC2H5混合液
B.  驗證NH4NO3晶體溶于水的熱效應
驗證NH4NO3晶體溶于水的熱效應
C.  蒸發FeCl3溶液得到FeCl3固體
蒸發FeCl3溶液得到FeCl3固體
D. 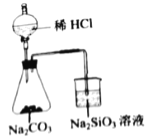 驗證C、Cl、Si的非金屬性強弱
驗證C、Cl、Si的非金屬性強弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解合成 1 , 2-二氯乙烷的實驗裝置如圖所示。下列說法中正確的是

A. 該裝置工作時,化學能轉變為電能
B. CuCl2能將C2H4還原為 l , 2-二氯乙烷
C. X、Y依次為陽離子交換膜、陰離子交換膜
D. 該裝置總反應為CH2CH2 + 2H2O + 2NaCl![]() H2 + 2NaOH + ClCH2CH2Cl
H2 + 2NaOH + ClCH2CH2Cl
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com