
| A. | 3.4g H2O2中含有的共用電子對數為0.1NA | |
| B. | 25℃,pH=13的NaOH溶液中,含有OH-的數目為0.1NA | |
| C. | 標準狀況下,2.24L氯氣溶于水發生反應,轉移的電子數目為0.1 NA | |
| D. | 標況下,11.2 L由CH4和C2H4組成的混合氣體中含有氫原子的數目為2 NA |
分析 A、求出雙氧水的物質的量,然后根據1mol雙氧水中含3mol共用電子對來分析;
B、溶液體積不明確;
C、氯氣和水的反應為可逆反應;
D、求出混合氣體的物質的量,然后根據甲烷和乙烯中均含4個氫原子來分析.
解答 解:A、3.4g雙氧水的物質的量為n=$\frac{3.4g}{34g/mol}$=0.1mol,而1mol雙氧水中含3mol共用電子對,故0.1mol雙氧水中含0.3NA對共用電子對,故A錯誤;
B、溶液體積不明確,故溶液中的氫氧根的個數無法計算,故B錯誤;
C、氯氣和水的反應為可逆反應,不能進行徹底,故轉移的電子數小于0.1NA個,故C錯誤;
D、標況下11.2L混合氣體的物質的量為0.5mol,而甲烷和乙烯中均含4個氫原子,故0.5mol混合物中含2NA個氫原子,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:高中化學 來源: 題型:解答題
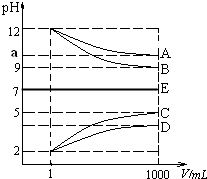 物質A~E都是由NH4+、H+、Na+、OH-、CH3COO-、Cl-中離子兩兩組成(離子可重復,如NaCl、HCl).常溫下將各物質的溶液從1mL稀釋到1000mL,pH的變化如甲圖所示.請回答:
物質A~E都是由NH4+、H+、Na+、OH-、CH3COO-、Cl-中離子兩兩組成(離子可重復,如NaCl、HCl).常溫下將各物質的溶液從1mL稀釋到1000mL,pH的變化如甲圖所示.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(Cl-)=c(NH3•H2O)+c(NH4+) | |
| B. | c(Cl-)>c(NH4+)>c(Na+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| C. | c(Cl-)+c(OH-)=c(Na+)+c(NH4+)+c(H+) | |
| D. | c(NH3•H2O)+c(OH-)=c(Na+)+c(NH4+)+c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

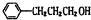 $?_{△}^{濃硫酸}$
$?_{△}^{濃硫酸}$ +H2O;該反應的反應類型為酯化反應或取代反應
+H2O;該反應的反應類型為酯化反應或取代反應 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵和酸反應,放出標準狀況下的22.4L氣體,轉移的電子數必為2NA | |
| B. | 將標準狀況下,11.2LN2和33.6LH2混合,在一定條件下充分反應,產生的NH3的分子數為2NA | |
| C. | 常溫常壓下,6g乙酸所含共價鍵數目為0.7NA | |
| D. | 1L 0.1mol•L-1碳酸鈉溶液中,陰離子數目大于0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| F | Cl | Br | I | |
| 第一電離能((kJ•mol-1)) | 1681 | 1251 | 1140 | 1008 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
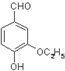 是食品添加劑的增香原料,其香味比香草醛更濃郁.寫出乙基香草醛分子中兩種含氧官能團的名稱醛基、羥基,核磁共振氫譜顯示該分子中有7種不同類型的氫原子.
是食品添加劑的增香原料,其香味比香草醛更濃郁.寫出乙基香草醛分子中兩種含氧官能團的名稱醛基、羥基,核磁共振氫譜顯示該分子中有7種不同類型的氫原子.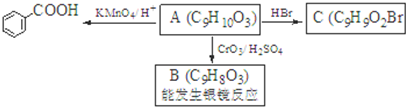
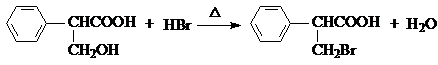 ,屬于取代反應(填反應類型).
,屬于取代反應(填反應類型). .
. .
. )是一種醫藥中間體,請設計合理方案用茴香醛(
)是一種醫藥中間體,請設計合理方案用茴香醛(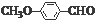 )合成D.(其他原料自選,用反應流程圖表示并注明必要的反應條件).
)合成D.(其他原料自選,用反應流程圖表示并注明必要的反應條件).

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com