
下列有關說法正確的是
A.為保護海輪的船殼,常在船殼上鑲入鋅塊
B.明礬溶于水可以使水凈化,是因為明礬中的Al3+水解顯酸性
C.己知工業合成氨氣∆H<0,達平衡后,升高溫度,正反應速率減小,逆反應 速率增大
速率增大
D.NH3(g) + HCl(g)=NH4Cl(s)是熵減小的反應,較低溫度下能自發進行,說明該反應的∆H>0
 快捷英語周周練系列答案
快捷英語周周練系列答案科目:高中化學 來源:2016-2017學年河北省高一12月月考化學卷(解析版) 題型:選擇題
甲、乙、丙三種物質均含有鋁元素,在溶液中的轉化關系如圖所示。下列說法正確的是
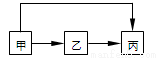
A.若甲是Al,丙是Al(NO3)3,則乙一定是NaAlO2
B.若甲是Al2O3,丙是NaAlO2,則乙一定是Al(NO3)3
C.若甲是Al(NO3)3,丙是NaAlO2,則乙一定是Al(OH)3
D.若甲是Al(OH)3,丙是Al(NO3)3,則乙一定是NaAlO2
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市部分區高一上學期期末化學試卷(解析版) 題型:選擇題
氮化鋁(化學式為AlN)廣泛應用于電子、陶瓷等工業領域。在一定條件下,AlN可通過反應Al2O3+N2+3C  2AlN+3CO合成。下列敘述正確的是
2AlN+3CO合成。下列敘述正確的是
A.上述反應中,N2是還原劑,Al2O3是氧化劑
B.上述反應中,每生成1 mol AlN需轉移3 mol e-
C.AlN中氮元素的化合價為+3
D.AlN的摩爾質量為41 g
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市部分區高二上學期期末化學試卷(解析版) 題型:填空題
電化學與我們的生活有著密切的聯系,請結合電化學知識回答下列有關問題。
(1)炒過菜的鐵鍋未及時洗凈(殘液中含有NaCl),不久便會因 腐蝕而出現紅棕色銹斑。試回答:
腐蝕而出現紅棕色銹斑。試回答:
鐵鍋的銹蝕應 屬于________________(填“析氫腐蝕”或“吸氧腐蝕”),鐵鍋銹蝕的負極反應式為:__________________;正負極反應產物會繼續發生反應,最終生成的紅棕色銹斑的主要成分是________________(填化學式)。
屬于________________(填“析氫腐蝕”或“吸氧腐蝕”),鐵鍋銹蝕的負極反應式為:__________________;正負極反應產物會繼續發生反應,最終生成的紅棕色銹斑的主要成分是________________(填化學式)。
(2)下圖是一個電化學過程的示意圖。
已知甲池的總反應式為:2CH3OH+3O2+4KOH 2K2CO3+6H2O
①甲池是_______裝置,通O2一極的電極反應式為____________________。
②乙池中反應的化學方程式為_____________________________。如果開始加入的CuSO4溶液足量,當乙池中A(Fe)極的質量增加3.2 g時,甲池中消耗O2_________mL(標準狀況下)。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市部分區高二上學期期末化學試卷(解析版) 題型:選擇題
熔融狀態下,Na的單質和FeCl2能組成可充電電池(裝置示意圖如下),反應原理為:2Na+FeCl2 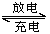 Fe+2NaCl 。下列判斷不正確的是
Fe+2NaCl 。下列判斷不正確的是
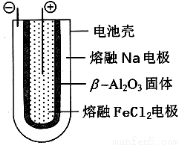
A.放電時,電池的正極反應式為Fe2++2e-=Fe
B.充電時,鈉電極接電源的正極
C.該電池的電解質為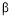 -Al2O3
-Al2O3
D.電池在使用時,外電路中電子由負極流向正極
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市部分區高二上學期期末化學試卷(解析版) 題型:選擇題
MnCl2溶液中常含有Cu2+離子,通過添加過量難溶電解質MnS,可使Cu2+離子形成CuS沉淀,經過濾除去包括MnS在內的沉淀,再經蒸發、結晶,可得純凈的MnCl2。根據上述實驗事實,可推知MnS具有的相關性質是
A.具有吸附性 B.溶解度與CuS相同
C.溶解度大于CuS D.溶解度小于CuS
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省資陽市高一上學期期末化學試卷(解析版) 題型:計算題
3.84 g Fe和Fe2O3的混合物溶于100 mL某濃度的鹽酸中,恰好使混合物溶解,生成0.03 mol H2,向反應后的溶液中加入KSCN檢驗,溶液無明顯現象,設HCl無揮發,反應后溶液的體積不變。(已知:氧化性Fe3+>H+,還原性Fe>Cl-)
(1)求標準狀況下生成氫氣的體積?
(2)求反應后Cl-的物質的量濃度?
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省資陽市高一上學期期末化學試卷(解析版) 題型:選擇題
下列鑒別物質或離子的方法能達到目的的是
A.用氨水鑒別MgCl2溶液和AlCl3溶液
B.用澄清石灰水鑒別Na2CO3溶液和NaHCO3溶液
C.用AgNO3鑒別Na2CO3溶液和NaCl溶液
D.用足量的鹽酸和BaCl2溶液鑒別溶液中是否含SO42-
查看答案和解析>>
科目:高中化學 來源:2016-2017學年廣東省惠州市高一上學期期末化學試卷(解析版) 題型:實驗題
硫酸銅的制備實驗是化學實驗教學中一個必做實驗,某學習小組設計了如下兩個實驗方案:
實驗一:
因銅不能與稀硫酸反應,實驗中用銅和濃硫酸加熱使之完全反應,將溶液通過蒸發、結晶等操作得到硫酸銅晶體。
(1)根據上述實驗和反應,比較濃硫酸與稀硫酸的性質,濃硫酸具有 。
(2)該反應的化學方程式為 。
實驗二:
以空氣為氧化劑的一步氧化法,將空氣或氧氣直接通入到銅粉與稀硫酸的混合物中,其反應原理為2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反應速率太慢,當升高溫度到80~90℃,反應仍然緩慢。如在銅粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,則速率明顯加快。
(3)Fe2(SO4)3的作用是 。
(4)得到的混合液可以用下列四種物質中的 調節溶液的pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH B. CuO C. CuCO3 D.Fe
(5)請根據以上內容,對這兩個實驗方案進行評價,填下表:
實 驗 (一) | 實 驗 (二) | |
主要優點 | 操作簡便 | (1)原料充分轉化為產品 (2)沒有有害氣體排放 |
主要缺點 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com