
| A. | 一定溫度下的可逆反應,只有達到平衡時才具有平衡常數 | |
| B. | 化學平衡移動時,平衡常數一定改變 | |
| C. | 對于一個確定的反應來說,平衡常數的數值越大,反應限度越大 | |
| D. | 化學平衡常數大的可逆反應,所有反應物的轉化率一定大 |
分析 化學平衡常數是用生成物濃度系數次冪之積除以反應物濃度系數次冪之積,化學平衡常數的大小只受溫度的影響,反應中的固體或者純液體的濃度看作是1,平衡常數不變,平衡可能發生移動,據此答題
解答 解:化學平衡常數是用生成物濃度系數次冪之積除以反應物濃度系數次冪之積,化學平衡常數的大小只受溫度的影響,
A、一定溫度下的可逆反應,本身就具有平衡常數,這是對可逆反應的限度的一種衡量,與反應是否處于的狀態時無關,故A錯誤;
B、化學平衡常數只受溫度的影響,其它條件改變,平衡移動,而平衡常數不變,故B錯誤;
C、平衡常數就反映了反應限度大小的一個量,它是用生成物濃度系數次冪之積除以反應物濃度系數次冪之積,所以對于一個確定的反應來說,平衡常數的數值越大,反應限度越大,故C正確;
D、反應物的轉化率與反應物起始的量和轉化的量有關,例如當有兩種反應物時,如果一種反應物過量較多,則這種反應物就是在平衡常數較大的情況下,轉化率也較小,故D錯誤;
故選C.
點評 本題主要考查了化學平衡常數的概念,難度不大,解題時要注意化學平衡常數的概念的理解及影響因素.


科目:高中化學 來源: 題型:選擇題
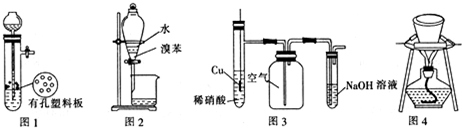
| A. | 圖1裝置用于Cu和濃H2SO4反應制取少量的SO2氣體 | |
| B. | 圖2裝置用于分離水和溴苯的混合物 | |
| C. | 圖3裝置用于制備并收集NO氣體 | |
| D. | 圖4裝置用于除去碳酸氫鈉固體中的少量碳酸鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl-、SO42-、Mg2+、Al3+ | B. | Na+、K+、Cl-、SO42- | ||
| C. | Na+、K+、Cl-、CO32- | D. | Na+、Fe3+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ,回答下列問題:
,回答下列問題: $\stackrel{一定條件下}{→}$
$\stackrel{一定條件下}{→}$ +2H2O.
+2H2O. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  Mg作負極,電子流向:Mg一→稀硫酸一→A1 | |
| B. |  Al作負極,電極反應式6H2O+6e-═6OH-+3H2↑ | |
| C. |  Cu作負極,電極反應式Cu-2e-═Cu2+ | |
| D. |  Cu作正極,電極反應式:2H++2e═H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al2(SO4)3溶液滴加氨水產生白色膠狀沉淀:Al3++3OH-═Al(OH)3↓ | |
| B. | 碳酸鈉溶液滴入酚酞變紅:CO32-+2H2O?H2CO3+2OH- | |
| C. | 向氫氧化鋇溶液中逐滴加入少量碳酸氫鈉溶液:Ba2++2OH-+2HCO3-═BaCO3↓+2H2O+CO32- | |
| D. | 硝酸鐵溶液中滴加足量HI溶液:Fe3++3NO3-+12H++10I-═Fe2++5I2+3NO↑+6H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com