
【題目】下列有關電解質溶液的說法正確的是
A.向0.1mol/LCH3COOH溶液中加入少量水,溶液中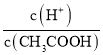 減小
減小
B.將CH3COONa溶液從20℃升溫至30℃,溶液中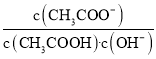 增大
增大
C.向鹽酸中加入氨水至中性,溶液中c(NH4+):c(Cl-)>1
D.向AgCl、AgBr的飽和溶液中加入少量AgNO3,溶液中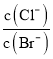 不變
不變
【答案】D
【解析】
A.加水促進弱電解質的電離,因此溶液n(H+)增大,n(CH3COOH)減小;
B.從20℃升溫至30℃,促進水解,Kh增大;
C.向鹽酸中加入氨水至中性,則c(H+)=c(OH-),結合電荷守恒分析;
D.向AgCl、AgBr的飽和溶液中加入少量AgNO3,c(Ag+)相同,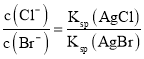 。
。
A.Ka=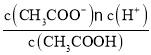 ,加水雖然促進電離,n(CH3COO-)增大,但c(CH3COO-)減小,Ka保持不變,則溶液中
,加水雖然促進電離,n(CH3COO-)增大,但c(CH3COO-)減小,Ka保持不變,則溶液中 增大,A錯誤;
增大,A錯誤;
B.從20℃升溫至30℃,促進水解,Kh增大,則溶液中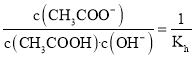 減小,B錯誤;
減小,B錯誤;
C.向鹽酸中加入氨水至中性,則c(H+)=c(OH-),根據溶液中電荷守恒可知,溶液中c(NH4+)=c(Cl-),所以c(NH4+):c(Cl-)=1,C錯誤;
D.向AgCl、AgBr的飽和溶液中加入少量AgNO3,c(Ag+)相同,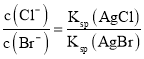 ,Ksp只與溫度有關,溫度不變,因此溶液中
,Ksp只與溫度有關,溫度不變,因此溶液中 不變,D正確;
不變,D正確;
故合理選項是D。


 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源: 題型:
【題目】有下列6組物質:①![]() 與
與![]() ;②N4與N2;③H2O2與H2O;④冰與水;⑤
;②N4與N2;③H2O2與H2O;④冰與水;⑤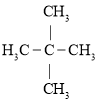 與
與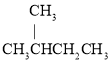 ;⑥C2H2與C2H4。請用序號填寫下列空白:
;⑥C2H2與C2H4。請用序號填寫下列空白:
互為同位素的是______;互為同素異形體的是______;互為同分異構體的是______;屬于同一種化合物的是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 都是元素周期表中前20號主族元素,原子序數依次增大,
都是元素周期表中前20號主族元素,原子序數依次增大,![]() 是地殼中含量最高的元素,
是地殼中含量最高的元素,![]() 、
、![]() 、
、![]() 同周期,
同周期,![]() 和其他元素既不在同一周期也不在同一主族,
和其他元素既不在同一周期也不在同一主族,![]() 的氫化物及其最高價氧化物對應的水化物均為強酸,且
的氫化物及其最高價氧化物對應的水化物均為強酸,且![]() 、
、![]() 、
、![]() 的最高價氧化物對應的水化物兩兩混合均能發生反應生成鹽和水。據此回答下列問題:
的最高價氧化物對應的水化物兩兩混合均能發生反應生成鹽和水。據此回答下列問題:
(1)![]() 四種元素中,原子半徑最大的是______(填元素符號);
四種元素中,原子半徑最大的是______(填元素符號);![]() 和
和![]() 的簡單氫化物中,沸點較低的是______(填化學式)。
的簡單氫化物中,沸點較低的是______(填化學式)。
(2)元素![]() 在元素周期表中的位置是______,
在元素周期表中的位置是______,![]() 、
、![]() 的最高價氧化物對應的水化物之間發生反應的化學方程式為____________________________________________________________。
的最高價氧化物對應的水化物之間發生反應的化學方程式為____________________________________________________________。
(3)![]() 、
、![]() 、
、![]() 可以形成多種鹽,其中一種鹽中
可以形成多種鹽,其中一種鹽中![]() 、
、![]() 、
、![]() 三種元素的原子個數比為
三種元素的原子個數比為![]() ,該鹽的化學名稱為______。它的水溶液與
,該鹽的化學名稱為______。它的水溶液與![]() 的氫化物的水溶液反應可生成
的氫化物的水溶液反應可生成![]() 的單質,該反應的離子方程式______________________________,反應生成
的單質,該反應的離子方程式______________________________,反應生成![]() 的單質時,轉移電子______
的單質時,轉移電子______![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸錳在電解錳、染料、造紙以及陶瓷等工業生產中有廣泛的應用。利用軟錳礦(主要成分為MnO2,含鐵的化合物等雜質)和閃鋅礦(主要成分ZnS)制得硫酸錳的流程如下:
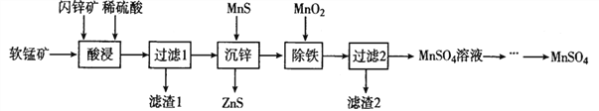
(1)“酸浸”時,為了縮短浸取時間,常加入少量FeSO4溶液,FeSO4的作用可能是___________________;MnO2、ZnS及硫酸反應轉變為兩種硫酸鹽的化學方程式為______________________。
(2)常溫下,Ksp(ZuS)=1.2×l0-24、Ksp(MnS)=1.5×10-15,“沉鋅”反應為:Zn2+(aq)+MnS![]() ZnS+Mn2+(aq),該反應的平衡常數K=__________________。
ZnS+Mn2+(aq),該反應的平衡常數K=__________________。
(3)在強酸性條件下加入MnO2氧化Fe2+的離子方程式為___________________。
(4)“除鐵”時需要調節pH約為3~4,過濾所得的濾渣2中除MnO2以外的另一種物質是________________。(寫化學式)
(5)該工藝流程中可以循環利用的物質是____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z是四種常見的短周期主族元素,其原子半徑隨原子序數的變化趨勢如圖所示。已知W的一種核素的質量數為18,中子數為10;X是短周期中金屬性最強的元素;Y的單質是一種常見的半導體材料;Z的非金屬性在同周期主族元素中最強。下列說法正確的是( )
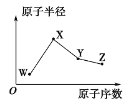
A.對應氣態氫化物的穩定性:Y > W
B.對應簡單離子的半徑:W>Z
C.化合物XZW中既含離子鍵又含共價鍵
D.Y的氧化物能與Z的最高價氧化物對應的水化物反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表的形式多種多樣,如下圖所示是扇形元素周期表的一部分(1~36號元素),對比中學常見元素周期表,思考扇形元素周期表的填充規律,下列說法不正確的是

A. 簡單離子半徑:②>⑧>⑨
B. 簡單氫化物的穩定性:⑤>⑧
C. 最高價氧化物對應的水化物的酸性:⑨>⑧>⑦
D. ①與⑤可形成既含極性鍵又含非極性鍵的化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是![]()
![]()
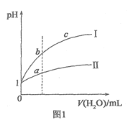

A.圖1表示相同溫度下![]() 的鹽酸和醋酸溶液分別加水稀釋時pH的變化曲線,其中曲線Ⅱ為鹽酸,且b點溶液的導電性比a點強
的鹽酸和醋酸溶液分別加水稀釋時pH的變化曲線,其中曲線Ⅱ為鹽酸,且b點溶液的導電性比a點強
B.圖2中在b點對應溫度下,將![]() 的
的![]() 與
與![]() 的NaOH溶液等體積混合后,溶液顯中性
的NaOH溶液等體積混合后,溶液顯中性
C.圖1中,b點酸的總濃度大于a點酸的總濃度
D.圖2中純水僅升高溫度,就可以從a點變到c點
查看答案和解析>>
科目:高中化學 來源: 題型:
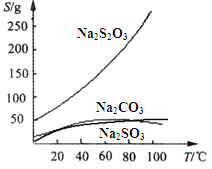
【題目】硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得:Na2SO3+S = Na2S2O3 。常溫下溶液中析出晶體為Na2S2O35H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有關物質的溶解度曲線如下左圖所示。
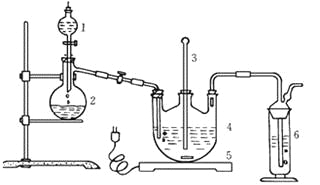
Ⅰ.現按如下方法制備Na2S2O3·5H2O:
將硫化鈉和碳酸鈉按反應要求比例一并放入三頸燒瓶中,注入150mL蒸餾水使其溶解,在分液漏斗中,注入濃鹽酸,在裝置2中加入亞硫酸鈉固體,并按上右圖安裝好裝置。
(1)儀器2的名稱為______________,裝置6中可放入___________。
A.BaCl2溶液 | B.濃H2SO4 | C.酸性KMnO4溶液 | D.NaOH溶液 |
(2)打開分液漏斗活塞,注入濃鹽酸使反應產生的二氧化硫氣體較均勻的通入Na2S和Na2CO3的混合溶液中,并用磁力攪拌器攪動并加熱,反應原理為:
① Na2CO3+SO2=Na2SO3+CO2②Na2S+SO2+H2O=Na2SO3+H2S
③ 2H2S+SO2=3S↓+2H2O ④ Na2SO3+S![]() Na2S2O3
Na2S2O3
隨著SO2氣體的通入,看到溶液中有大量淺黃色固體析出,繼續通SO2氣體,反應約半小時。當溶液中pH接近或不小于7時,即可停止通氣和加熱。溶液pH要控制不小于7的理由是:_____________(用文字和相關離子方程式表示)。
Ⅱ.分離Na2S2O3·5H2O并測定含量:
![]()
(3)為減少產品的損失,操作①為__________,操作②是過濾洗滌干燥,其中洗滌操作是用________(填試劑)作洗滌劑。
(4)蒸發濃縮濾液直至溶液呈微黃色渾濁為止,蒸發時為什么要控制溫度不宜過高_____________。
(5)制得的粗晶體中往往含有少量雜質。為了測定粗產品中Na2S2O3·5H2O的含量,一般采用在酸性條件下用KMnO4標準液滴定的方法(假定粗產品中雜質與酸性KMnO4溶液不反應)。
稱取1.28 g的粗樣品溶于水,用0.40mol/L KMnO4溶液(加入適量硫酸酸化)滴定,當溶液中S2O32—全部被氧化時,消耗KMnO4溶液體積20.00 mL。(5S2O32—+8MnO4—+14H+ =8Mn2++10SO42—+7H2O)
試回答:
①KMnO4溶液置于__________(填“酸式”或“堿式”)滴定管中。
②滴定終點時的顏色變化:_____________________。
③產品中Na2S2O3·5H2O的質量分數為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,0.1 mol·L-1Na2S溶液中存在著水解平衡:S2-+H2O![]() HS-+OH-。下列說法正確的是( )
HS-+OH-。下列說法正確的是( )
A.加水稀釋后恢復至常溫,水解平衡正向移動,水解平衡常數增大
B.通入NH3,平衡正向移動
C.滴加少量AgNO3溶液,平衡逆向移動
D.升高溫度,c(HS-)/c(S2-)減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com