
| A. | 反應速率:乙>甲 | |
| B. | 平衡混合物中SO2的體積分數:乙>甲 | |
| C. | SO2的轉化率:乙>甲 | |
| D. | 平衡時O2的體積分數:甲>乙 |
分析 在相同溫度下(T=500K),有相同體積的甲、乙兩容器,且保持體積不變,加入二氧化硫和氧氣發生的反應為:2SO2+O2?2SO3,反應是氣體體積減小的放熱反應,甲容器中和乙容器中相比,乙容器中壓強大于甲,反應速率快,增大壓強,平衡正向移動,二氧化硫轉化率增大.
解答 解:在相同溫度下(T=500K),有相同體積的甲、乙兩容器,且保持體積不變,加入二氧化硫和氧氣發生的反應為:2SO2+O2?2SO3,反應是氣體體積減小的放熱反應,甲容器中和乙容器中相比,乙容器中壓強大于甲,反應速率快,增大壓強,平衡正向移動,二氧化硫轉化率增大.
A.乙中物質濃度大于甲,化學反應速率:乙>甲,故A正確;
B.乙容器中壓強大于甲,增大壓強,平衡正向移動,SO2的體積分數減小,因此平衡混合物中SO2的體積分數:乙<甲,故B錯誤;
C.乙容器中壓強大于甲,增大壓強,平衡正向移動,SO2的轉化率增大,因此SO2的轉化率:乙>甲,故C正確;
D.乙容器中壓強大于甲,增大壓強,平衡正向移動,O2的體積分數減小,因此平衡時O2的體積分數:甲>乙,故D正確;
故選B.
點評 本題考查了化學平衡影響因素分析判斷,注意恒溫容器中平衡的分析判斷,掌握外界條件對化學反應速率和化學平衡的影響是關鍵,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1Na2CO3溶液中,c(OH)-=c(H+)+c(HCO3-)+c(H2CO3) | |
| B. | 相同物質的量濃度的NaCN和NaClO相比,NaCN溶液的pH較大,則對于同溫、同體積、同pH的HCN和HClO分別與Na0H恰好完全反應時,消耗NaOH的物質的量:HClO<HCN | |
| C. | 向醋酸鈉溶液中加入適量醋酸,得到酸性的混合溶液:c(Na+)>c(CH3COO-)>C(H+)>c(OH-) | |
| D. | 向硝酸鈉溶液中滴加稀鹽酸得到pH=5的混合溶液:c(Na+)=c(NO3-)+c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
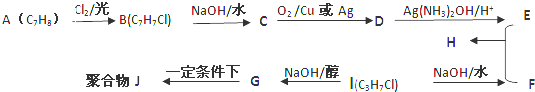
 ,D的官能團名稱醛基.
,D的官能團名稱醛基. +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. +CH3CH(OH)CH3$→_{△}^{濃硫酸}$
+CH3CH(OH)CH3$→_{△}^{濃硫酸}$ +H2O.
+H2O.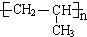 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不能發生消去反應 | B. | 不能發生取代反應 | ||
| C. | 能溶于水,不溶于乙醇 | D. | 能氧化為醛 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3mol NF3(F元素為-1價)與水完全反應生成HF、HNO3和NO,轉移電子數2NA | |
| B. | 22.4L CO2與過量的Na2O2反應,轉移的電子數為NA | |
| C. | 物質的量濃度為0.3mol/L的BaCl2溶液中,含有Cl- 個數為0.6 NA | |
| D. | 常溫下,5.6g鐵釘與足量濃硝酸反應,轉移的電子數為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Na+、MnO4-、SO42- | |
| B. | I-、Na+、NO3-、ClO- | |
| C. | Mg2+、Na+、NO3-、SO42- | |
| D. | 加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com