
分析 依據化學反應速率之比等于化學方程式中計量數之比,把四種情況下的反應速率化為一種物質表示的反應速率減小比較,溫度越高反應速率越大.
解答 解:將四個反應速率甲:ν(A)=3mol/(L•min);乙:ν(B)=4.5mol/(L•min);丙:ν(C)=4mol/(L•min);丁:ν(A)=0.75mol/(L•s),都統一到用A表示的反應速率值分別為甲:ν(A)=3mol/(L•min);乙:ν(A)=$\frac{1}{3}$V(B)=$\frac{1}{3}$×4.5mol/L•min=1.5mol/(L•min);丙:ν(A)=$\frac{1}{2}$V(C)=$\frac{1}{2}$×4mol/(L•min)=2mol/L•min;丁:ν(A)=0.75mol/(L•s)=45mol/L•min,所以化學反應速率是丁>甲>丙>乙,溫度越高,化學反應速率越快,溫度由低到高的順序是:乙<丙<甲<丁;
故答案為:乙<丙<甲<丁.
點評 本題考查化學反應速率的計算以及影響因素,為高頻考點,側重于學生的分析能力的考查,注意把握化學反應速率與計量數的關系,難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;檢驗元素X、Y、Z以質量比為1:7:12形成的化合物中所含陽離子的離子反應方程式是:
;檢驗元素X、Y、Z以質量比為1:7:12形成的化合物中所含陽離子的離子反應方程式是:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子數為2 NA | |
| B. | 密閉容器中2 mol NO與1 mol O2充分反應,產物的分子數為2 NA | |
| C. | 過氧化鈉與水反應時,生成0.1 mol 氧氣轉移的電子數為0.2 NA | |
| D. | 標準狀況下,33.6 L氟化氫中含有氟原子的數目為1.5 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子總數為NA的NO2和CO2混合氣體中含有的氧原子數為2NA | |
| B. | 28g乙烯(C2H4)和環丁烷(C4H8)的混合氣體中含有的碳原子數為2NA | |
| C. | 常溫常壓下,92g的NO2和N2O4混合氣體含有的原子總數為6NA | |
| D. | 17gOH-中含有的質子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
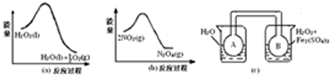
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 陳述Ⅰ | 陳述Ⅱ |
| A | 氫氟酸具有酸性 | 氫氟酸可用于雕刻玻璃 |
| B | 氯水顯酸性 | 可用pH試紙測氯水的pH |
| C | NH3極易溶于水 | NH3可用作制冷劑 |
| D | ClO2具有強氧化性 | ClO2可用于自來水的殺菌消毒 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com