
| A. | 整個反應過程中:c(H+)+c(Na+)+c(NH4+)=c(OH-)+c(SO42-) | |
| B. | 當滴入30mL NaOH溶液時(pH>7):c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| C. | 當滴入20mL NaOH溶液時:2c(SO42-)═c(NH3•H2O)+c(NH4+) | |
| D. | 當溶液呈中性時:c(NH4+)>c(SO42-)>c(Na+)>c(H+)=c(OH-) |
分析 A.任何電解質溶液中都存在電荷守恒,根據電荷守恒判斷;
B.滴入30mLNaOH溶液時,反應后的溶液中含有0.001mol一水合氨、0.0005mol硫酸銨,溶液的pH>7,說明一水合氨的電離程度大于銨根離子的水解程度;
C.根據混合液中的物料守恒判斷;
D.當加入20mL氫氧化鈉溶液時,二者反應生成硫酸銨、硫酸鈉,由于銨根離子部分水解,溶液顯示酸性,若為中性,則加入的氫氧化鈉溶液稍大于20mL,據此進行判斷.
解答 解:A.溶液中一定滿足電荷守恒:c(H+)+c(Na+ )+c(NH4+)=c(OH-)+2c(SO42-),故A錯誤;
B.滴入30mLNaOH溶液時(pH>7),其中20mLNaOH溶液與NH4HSO4中的氫離子發生中和反應,剩余的10mLNaOH溶液與銨根離子反應,則反應后的溶液中含有0.001mol一水合氨、0.0005mol硫酸銨,溶液的pH>7,說明一水合氨的電離程度大于銨根離子的水解程度,則:c(NH4+)>c(NH3•H2O)、c(OH-)>c(H+),則溶液中離子濃度大小為:c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+),故B正確;
C.當滴入20mLNaOH溶液時,根據物料守恒可得:c(SO42-)=c(NH4+)+c(NH3•H2O),故C錯誤;
D.根據物料守恒可得:c(SO42-)=c(NH4+)+c(NH3•H2O),則c(SO42-)>c(NH4+);由于溶液為中性,則c(H+)=c(OH-),根據電荷守恒可得:c(H+)+c(Na+ )+c(NH4+)=c(OH-)+2c(SO42-),所以c(Na+ )+c(NH4+)=2c(SO42-),結合c(SO42-)>c(NH4+)可知:c(Na+ )>c(SO42-),所以溶液中離子濃度大小為:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-),故D錯誤;
故選B.
點評 本題考查了離子濃度大小比較、酸堿混合的定性判斷等知識,題目難度中等,明確反應后溶質組成為解答關鍵,注意掌握電荷守恒、物料守恒、鹽的水解原理在判斷離子濃度大小中的應用方法,注意氫離子和銨根離子反應先后順序,為易錯點.


 同步學典一課多練系列答案
同步學典一課多練系列答案 經典密卷系列答案
經典密卷系列答案 金牌課堂練系列答案
金牌課堂練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.3 mol/L Na2SO4溶液中含有Na+和SO42-總物質的量為0.9mol | |
| B. | 當1L水吸收22.4LNH3時所得氨水的濃度不是1 mol/L,只有當22.4L NH3溶于水制得1L氨水時,其濃度才是1 mol/L | |
| C. | 10℃時0.5 mol/L的稀鹽酸100mL,蒸發掉5g水,冷卻到10℃時,其體積小于100mL,它的物質的量濃度大于0.5 mol/L | |
| D. | 10℃時0.5 mol/L的KCl飽和溶液100mL,蒸發掉5g水,冷卻到10℃時,其體積小于100 mL,它的物質的量濃度仍為0.5 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol Cl2在反應中得到電子數不一定為NA | |
| B. | 1mol O2在反應中得到電子數一定為4NA | |
| C. | 1molNa2O2與足量H2O反應,轉移了NA個電子 | |
| D. | 在2KClO3+4HCl(濃)═2KCl+2ClO2↑+Cl2↑+2H2O中,氯氣既是氧化產物又是還原產物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol A+0.5mol B+1.5mol C+0.1mol D | |
| B. | 3mol C+0.5mol D | |
| C. | 2mol A+1mol B+1molD | |
| D. | 0.5mol A+0.25mol B+2.25mol C |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化鋁溶液中加入過量氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | 澄清石灰水與過量蘇打溶液反應:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 碳酸鈣溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 碘化亞鐵中通入氯氣:2I-+Cl2═I2+2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
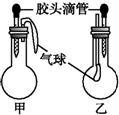 | 甲 | 乙 | |||
| 滴管中 | 燒瓶中 | 滴管中 | 燒瓶中 | ||
| A | 水 | 過氧化鈉 | 飽和碳酸氫鈉溶液 | CO2 | |
| B | NaOH溶液 | 鋁 | 硫酸鈉溶液 | CO2 | |
| C | NaOH溶液 | 碳酸氫鈉 | 澄清石灰水 | 碳酸氫鈉 | |
| D | 稀鹽酸 | 碳酸氫鈉 | NaOH溶液 | CO2 | |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可以利用電泳現象區分溶液和膠體 | |
| B. | 可以利用膠體的丁達爾效應區分溶液和膠體 | |
| C. | 可以用過濾的方法分離溶液和膠體 | |
| D. | 溶液呈電中性,膠體是帶電的 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com