
(16分)寫出下列反應的化學方程式或離子方程式。
(1)漂白粉溶液中通入過量的二氧化碳的化學方程式 ___________________________
(2)足量的氯氣通入到溴化亞鐵溶液中的離子方程式_________________________________
(3)硫酸工業生產中在接觸室中發生的反應的化學方程式_____________________________
(4)碳和濃硫酸反應的化學方程式__________________________________
(1) Ca(ClO)2 + 2CO2 + 2H2O = 2HClO + Ca(HCO3)2
(2)3Cl2 + 2Fe2+ + 4Br- = 6Cl- + 2Fe3+ + 2Br2
(3)4FeS2 +11O2 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
(4)SO2 + Br2 + 2H2O = 2HBr + H2SO4
解析試題分析:
(1)這里是碳酸酸性強于次氯酸,先Ca(ClO)2 + CO2 + H2O =" 2HClO" + CaCO3↓,后是過量的二氧化碳:CO2 + H2O + CaCO3 = Ca(HCO3)2,兩式疊加去掉碳酸鈣即可。
(2)氯氣能氧化二價鐵和溴離子,先寫出方程式:3Cl2+2FeBr2=2FeCl3+2Br2,然后改成離子方程式。
(3)制硫酸用的是黃鐵礦即FeS2先鍛燒后生成二氧化硫,再進一步氧化成三氧化硫,再用濃硫酸吸收生成的三氧化硫,在接觸中則發生4FeS2+11O2=(高溫)2Fe2O3+8SO2,配平時要注意其有兩種元素變價。
(4)溴是鹵族元素,很容易想到具有強氧化性,被還原成Br-,根據氧化還原反應的特點,二氧硫當體現還原性,在溶液中往往以SO42-的形式存在,先寫出Br2+SO2→2Br-+ SO42-,剩余的部分通過原子守恒補足。
考點: 氧化還原反應及優先反應原理;化學方程式的書寫。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:單選題
對于反應14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列說法正確的是( )
| A.只有硫酸銅作氧化劑 |
| B.SO42-既不是氧化產物又不是還原產物 |
| C.被氧化的硫與被還原的硫的質量比為3:7 |
| D.1mol硫酸銅可以氧化5/7mol的硫 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
Cu2S與一定濃度的HNO3反應,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,當NO2和NO的物質的量之比為2:1時,實際參加反應的Cu2S與HNO3的物質的量之比為
| A.1:10 | B.1:8 | C.1:6 | D.1:5 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)無論是從在國民經濟中的地位來看,還是從科學發展的角度來看,硅都發揮著重要的作用。
(1)人類使用硅酸鹽產品(陶瓷等)的歷史已經快一萬年了,但在1823年才獲得單質硅,瑞典化學家貝采尼烏斯用金屬鉀還原SiF4獲得單質硅,寫出化學方程式_______________ 。
(2)由于制取方法和條件的不同,得到的單質硅形態不同,其性質也不同。
①用鋁熱法還原氟硅酸鉀制得較純凈的晶體硅:4Al+3K2SiF6高溫3Si+2KAlF4+2K2AlF5,關于該反應的說法正確的是________(填序號)。
| A.Al是還原劑 | B.氧化產物只有KAlF4 |
| C.每轉移6NA電子,得到42 g Si | D.Al元素在KAlF4和K2AlF5中化合價不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(本題16分)無水AlCl3可用作有機合成的催化劑、食品膨松劑等。工業制備無水AlCl3的流程如下: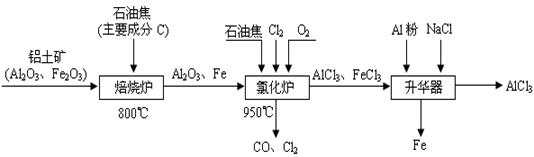
(1)氯化爐中通入O2的目的是 _________。
(2)氯化爐中Al2O3、C12和C反應的化學方程式是____________________________。
(3)氯化爐中導出的氣體,通常用亞硫酸鈉溶液來吸收,請寫出用Na2SO3溶液處理尾氣時發生反應的離子方程式___________________________________________________。
(4)在升華器中加入鋁粉的目的是_________________________________________。
(5)用氯化鋁晶體(AlCl3·6H2O)在HCl氣中加熱也能進行無水氯化鋁的制備。但若實驗條件控制不當,最終得到的物質是堿式氯化鋁[化學式為Al2(OH)nCl(6-n)],且質量是原氯化鋁晶體(AlCl3·6H2O)的40%,則可推算n的值為 。
(6)鍍鋁電解池中,金屬鋁為陽極,熔融鹽電鍍液中鋁元素主要以AlCl4-形式存在,則陽極的電極反應式為___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)某經濟開發區將鈦冶煉廠與氯堿廠、甲醇廠組成了一個產業鏈(如圖所示),大大地提高了資源利用率,減少了環境污染。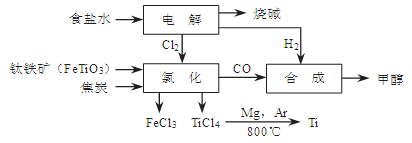
請填寫下列空白:
(1)寫出鈦鐵礦經氯化得到四氯化鈦的化學方程式: 。
(2)由CO和H2合成甲醇是放熱的,方程式是:CO(g)+2H2(g)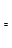 CH3OH(g)。
CH3OH(g)。
①已知該反應在300℃時的化學平衡常數為0.27,該溫度下將2 mol CO、3 mol H2和2 mol CH3OH充入容積為2 L的密閉容器中,此時反應將 (填“向正反應方向進行”、“向逆反應方向進行”或“處于平衡狀態”)。
②下圖表示合成甲醇反應達到平衡后,每次只改變溫度、壓強、催化劑中的某一條件,反應速率υ與時間t的關系。其中表示平衡混合物中的甲醇的含量最高的一段時間是 。圖中t3時改變的條件可能是 。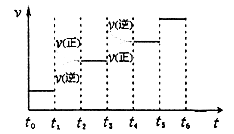
(3)某同學設計了一個甲醇燃料電池,并用該電池電解200mL—定濃度NaCl與CuSO4混合溶液,其裝置如圖: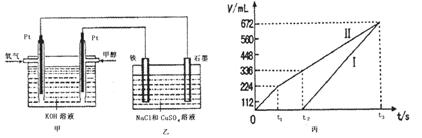
①寫出甲中通入甲醇這一極的電極反應式 。
②理論上乙中兩極所得氣體的體積隨時間變化的關系如丙圖所示(氣體體積已換算成標準狀況下的體積),寫出在t1后,石墨電極上的電極反應式 ,原混合溶液中NaCl的物質的量濃度為 mol/L。(假設溶液體積不變)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
銅單質及其化合物是應用極其廣泛的物質。
(1)銅是氫后金屬,不能與鹽酸發生置換反應,但將單質銅置于濃氫碘酸中,會有可燃性氣體及白色沉淀生成,又知氧化性:Cu2+>I2,則銅與氫碘酸反應的化學方程式為__________________________________
(2)已知Cu2O能溶于醋酸溶液或鹽酸中,同時得到藍色溶液和紅色固體,則Cu2O與稀硫酸反應的離子方程式為____________________________________;
Cu2O與稀硝酸反應的離子方程式為_____________________________;
只用稀硫酸來確定某紅色固體是 Cu2O與Cu組成的混合物的方法:稱取m g該紅色固體置于足量稀硫酸中,充分反應后過濾,然后___________________。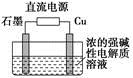
(3)Cu2O是一種半導體材料,基于綠色化學理念設計的制取Cu2O的電解裝置如圖所示,電解總反應:2Cu+H2O Cu2O+H2↑,則石墨應與電源的________極相連,銅電極上的電極反應式為________;電解過程中,陰極區周圍溶液pH________(填“變大”、“變小”或“不變”)。
Cu2O+H2↑,則石墨應與電源的________極相連,銅電極上的電極反應式為________;電解過程中,陰極區周圍溶液pH________(填“變大”、“變小”或“不變”)。
(4)現向Cu、Cu2O、CuO組成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同時收集到2 240 mL NO(標準狀況)。若將上述混合物用足量的氫氣還原,所得固體的質量為________;若混合物中含有0.1 mol Cu,將該混合物與稀硫酸充分反應,至少消耗硫酸的物質的量為________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
向FeI2溶液中不斷通入Cl2,溶液中I-、I2、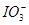 、Fe2+、Fe3+等粒子的物質的量隨n(Cl2)∶n(FeI2)變化的曲線如圖所示。
、Fe2+、Fe3+等粒子的物質的量隨n(Cl2)∶n(FeI2)變化的曲線如圖所示。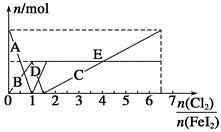
已知:2Fe3++2I-=I2+2Fe2+。
請回答下列問題:
(1)指出圖中折線E和線段C所表示的意義:折線E表示 ;線段C表示 。
(2)寫出線段D所表示的反應的離子方程式: 。
(3)當n(Cl2)∶n(FeI2)=6.5時,溶液中n(Cl-)∶n(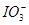 )= 。
)= 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
溴的氧化性介于氯和碘之間,利用這一性質解決下面的問題。
(1)你認為:將含有下列哪種分子或離子的試劑加入到含有Br-的溶液中,可以將Br-氧化為Br2__________。
| A.I2 | B.I | C.Cl2 | D.Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com