
X、Y、Z、Q、R是五種短周期元素,原子序數依次增大。X、Y兩元素最高正價與最低負價之和均為0;Q與X同主族;Z、R分別是地殼中含量最高的非金屬元素和金屬元素。
請回答下列問題:
(1)五種元素原子半徑由大到小的順序是(寫元素符號)________________。
(2)X與Y能形成多種化合物,其中既含極性鍵又含非極性鍵,且相對分子質量最小的物質是(寫分子式)____________。
(3)由以上某些元素組成的化合物A、B、C、D有如下轉化關系:
A B(在水溶液中進行)
B(在水溶液中進行)
其中,C是溶于水顯酸性的氣體;D是淡黃色固體。寫出C的結構式:________;D的電子式:________。
①如果A、B均由三種元素組成,B為兩性不溶物,則A的化學式為________;由A轉化為B的離子方程式為______________________________。
②如果A由三種元素組成,B由四種元素組成,A、B溶液均顯堿性。用離子方程式表示A溶液顯堿性的原因:______________________。A、B濃度均為0.1 mol·L-1的混合溶液中,離子濃度由大到小的順序是________;常溫下,在該溶液中滴加稀鹽酸至中性時,溶質的主要成分有______________________。
(1)Na>Al>C>O>H (2)C2H2
(3)O=C=O 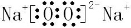
①NaAlO2 AlO2—+2H2O+CO2=Al(OH)3↓+HCO3—[或2AlO2—+3H2O+CO2=2Al(OH)3↓+CO32—]
②CO32—+H2O HCO3—+OH-
HCO3—+OH-
c(Na+)>c(HCO3—)>c(CO32—)>c(OH-)>c(H+)
NaCl、NaHCO3、CO2(或H2CO3)
【解析】依據題干提供的信息,判定元素種類,解決具體問題。X、Y兩元素最高正價與最低負價之和均為0,結合它們都是短周期初步判斷是ⅠA族的H和ⅣA族的C。Q與X同主族,則Q為Na。Z、R分別是地殼中含量最高的非金屬元素和金屬元素,可以判斷是O和Al。所以X、Y、Z、Q、R分別是H、C、O、Na、Al。(1)H、C、O、Na、Al原子半徑的大小順序是Na>Al>C>O>H。(2)H和C形成的化合物中既含極性鍵又含非極性鍵,且相對分子質量最小的物質是C2H2。(3)由A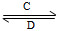 B轉化及C是溶于水顯酸性的氣體,可知C是CO2,D是淡黃色固體,則D是Na2O2。CO2的結構式為O=C=O;Na2O2的電子式是
B轉化及C是溶于水顯酸性的氣體,可知C是CO2,D是淡黃色固體,則D是Na2O2。CO2的結構式為O=C=O;Na2O2的電子式是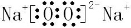 。①A、B均由三種元素組成,B為兩性不溶物,則B為Al(OH)3,A為NaAlO2。NaAlO2轉化為Al(OH)3的離子方程式為AlO2—+2H2O+CO2=Al(OH)3↓+HCO3—或2AlO2—+3H2O+CO2=2Al(OH)3↓+CO32—。②由上述五種元素組成的化合物,其溶液顯堿性的有Na2CO3、NaHCO3和NaOH等。B由四種元素組成,所以B是NaHCO3。結合A
。①A、B均由三種元素組成,B為兩性不溶物,則B為Al(OH)3,A為NaAlO2。NaAlO2轉化為Al(OH)3的離子方程式為AlO2—+2H2O+CO2=Al(OH)3↓+HCO3—或2AlO2—+3H2O+CO2=2Al(OH)3↓+CO32—。②由上述五種元素組成的化合物,其溶液顯堿性的有Na2CO3、NaHCO3和NaOH等。B由四種元素組成,所以B是NaHCO3。結合A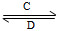 B的轉化可以確定A是Na2CO3。Na2CO3溶液顯堿性的原因是CO32—+H2O
B的轉化可以確定A是Na2CO3。Na2CO3溶液顯堿性的原因是CO32—+H2O HCO3—+OH-。Na2CO3和NaHCO3濃度均為0.1 mol·L-1的混合溶液中,由于CO32—的水解程度大于HCO3—,所以離子濃度大小關系是c(Na+)>c(HCO3—)>c(CO32—)>c(OH-)>c(H+)。向Na2CO3和NaHCO3的混合溶液中滴加稀鹽酸,Na2CO3先和HCl反應生成NaHCO3,然后NaHCO3與鹽酸反應生成CO2,生成的CO2部分溶解在溶液中,溶有CO2的飽和溶液的pH為5.6,所以當溶液呈中性時,還會有少量NaHCO3存在,此時溶質的主要成分為NaCl、NaHCO3、CO2。
HCO3—+OH-。Na2CO3和NaHCO3濃度均為0.1 mol·L-1的混合溶液中,由于CO32—的水解程度大于HCO3—,所以離子濃度大小關系是c(Na+)>c(HCO3—)>c(CO32—)>c(OH-)>c(H+)。向Na2CO3和NaHCO3的混合溶液中滴加稀鹽酸,Na2CO3先和HCl反應生成NaHCO3,然后NaHCO3與鹽酸反應生成CO2,生成的CO2部分溶解在溶液中,溶有CO2的飽和溶液的pH為5.6,所以當溶液呈中性時,還會有少量NaHCO3存在,此時溶質的主要成分為NaCl、NaHCO3、CO2。
點撥:知識:元素推斷、電子式、結構式、原子半徑大小比較、離子反應方程式書寫、鹽類的水解以及電荷守恒。能力:考查學生對元素的推斷、物質轉化的推理能力及對鹽類水解的應用能力。試題難度:中等。


 靈星計算小達人系列答案
靈星計算小達人系列答案 孟建平錯題本系列答案
孟建平錯題本系列答案科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 綜合實驗設計與評價練習卷(解析版) 題型:實驗題
醇脫水是合成烯烴的常用方法,實驗室合成環己烯的反應和實驗裝置如下:


可能用到的有關數據如下:
| 相對分子質量 | 密度 g/cm3 | 沸點/℃ | 溶解性 |
環己醇 | 100 | 0.9618 | 161 | 微溶于水 |
環己烯 | 82 | 0.8102 | 83 | 難溶于水 |
合成反應:
在a中加入20 g環己醇和2小片碎瓷片,冷卻攪動下慢慢加入1 mL濃硫酸。b中通入冷卻水后,開始緩慢加熱a,控制餾出物的溫度不超過90℃。
分離提純:
反應粗產物倒入分液漏斗中分別用少量5%碳酸鈉溶液和水洗滌,分離后加入無水氯化鈣顆粒,靜置一段時間后棄去氯化鈣。最終通過蒸餾得到純凈環己烯10 g。
回答下列問題:
(1)裝置b的名稱是________。
(2)加入碎瓷片的作用是________;如果加熱一段時間后發現忘記加瓷片,應該采取的正確操作是________(填正確答案標號)。
A.立即補加 B.冷卻后補加 C.不需補加 D.重新配料
(3)本實驗中最容易產生的副產物的結構簡式為________。
(4)分液漏斗在使用前須清洗干凈并________;在本實驗分離過程中,產物應該從分液漏斗的________(填“上口倒出”或“下口放出”)。
(5)分離提純過程中加入無水氯化鈣的目的是________。
(6)在環己烯粗產物蒸餾過程中,不可能用到的儀器有________(填正確答案標號)。
A.圓底燒瓶 B.溫度計 C.吸濾瓶 D.球形冷凝管
E.接收器
(7)本實驗所得到的環己烯產率是________(填正確答案標號)。
A.41% B.50% C.61% D.70%
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 電解質溶液練習卷(解析版) 題型:選擇題
25℃時,用濃度為0.1000 mol·L-1的NaOH溶液滴定20.00 mL濃度均為0.1000 mol·L-1的三種酸HX、HY、HZ,滴定曲線如下圖所示。下列說法正確的是( )

A.在相同溫度下,同濃度的三種酸溶液的導電能力順序:HZ<HY<HX
B.根據滴定曲線,可得Ka(HY)≈10-5
C.將上述HX、HY溶液等體積混合后,用NaOH溶液滴定至HX恰好完全反應時:c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY與HZ混合,達到平衡時:c(H+)= +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 物質結構與性質練習卷(解析版) 題型:填空題
太陽能電池的發展已經進入了第三代。第三代就是銅銦鎵硒CIGS等化合物薄膜太陽能電池以及薄膜Si系太陽能電池。完成下列填空:
(1)亞銅離子(Cu+)基態時的電子排布式為________;
(2)硒為第四周期元素,相鄰的元素有砷和溴,則3種元素的第一電離能從大到小順序為________(用元素符號表示),用原子結構觀點加以解釋:________。
(3)與鎵元素處于同一主族的硼元素具有缺電子性(價電子數少于價層軌道數),其化合物可與具有孤對電子的分子或離子生成加合物,如BF3能與NH3反應生成BF3·NH3。BF3·NH3中B原子的雜化軌道類型為________,B與N之間形成________鍵。
(4)單晶硅的結構與金剛石結構相似,若將金剛石晶體中一半的C原子換成Si原子且同種原子不成鍵,則得如圖所示的金剛砂(SiC)結構;在SiC中,每個C原子周圍最近的C原子數目為________。

查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 物質結構與性質練習卷(解析版) 題型:選擇題
兩種元素原子的核外電子層數之比與最外層電子數之比相等,則在周期表前10號元素中,滿足上述關系的元素共有( )
A.1對 B.2對 C.3對 D.4對
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 物質結構、元素周期律練習卷(解析版) 題型:選擇題
下列排序正確的是( )
A.酸性:H2CO3<C6H5OH<CH3COOH B.堿性:Ba(OH)2<Ca(OH)2<KOH
C.熔點:MgBr2<SiCl4<BN D.沸點:PH3<NH3<H2O
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 物質結構、元素周期律練習卷(解析版) 題型:選擇題
X、Y、Z是原子序數依次遞增的短周期元素,3種元素的原子核外電子數之和與Ca2+的核外電子數相等,X、Z分別得到1個電子后均形成稀有氣體原子的穩定電子層結構。下列說法正確的是( )
A.原子半徑:Z>Y>X
B.Z與X形成化合物的沸點高于Z的同族元素與X形成化合物的沸點
C.Na2Y2與水發生氧化還原反應時,Na2Y2只做氧化劑
D.CaX2、CaY2和CaZ2等3種化合物中,陽離子與陰離子個數比均為1:2
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 物質的組成性質分類及化學用語練習卷(解析版) 題型:選擇題
下列有關物質的性質或結構的說法正確的是( )
A.L層上的電子數為奇數的原子一定是主族元素的原子
B.周期表中的堿金屬元素從上到下,其單質的還原性逐漸增強,熔沸點逐漸升高
C.化學鍵的形成一定伴隨著電子的轉移和能量變化
D.元素周期表中,位于金屬和非金屬分界線附近的元素屬于過渡元素
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化工生產流程、無機物的判斷練習卷(解析版) 題型:選擇題
已知:A、B為單質,C為化合物, 。能實現該轉化關系的是( )
。能實現該轉化關系的是( )
①若C溶于水后得到強堿性溶液,則A可能是Na
②若C的溶液遇Na2CO3放出CO2氣體,則A可能是H2
③若C的溶液中滴加KSCN溶液顯紅色,則B可能為Fe
④若C的溶液中滴加NaOH溶液有藍色沉淀生成,則B可能為Cu
A.①② B.②④ C.①③ D.③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com