
化學上存在許多的遞變關系,下列遞變關系完全正確的是( )
A.離子半徑:Na+>Mg2+>Al3+>Cl— ;原子半徑:Na>Mg>Al>Cl
B.穩定性:HF>H2O>NH3>CH4 ; 還原性: HF < H2O < NH3< CH4
C.堿性:CsOH>KOH>Mg(OH)2>NaOH ; 金屬性:Cs>K>Mg>Na
D.酸性:HClO>H2SO4>H2CO3;非金屬性Cl>S>C
科目:高中化學 來源: 題型:
由碳的氧化物直接合成乙醇燃料已進入大規模生產。下圖是由二氧化碳合成乙醇的技術流程:

吸收池中盛有飽和碳酸鉀溶液,把含有二氧化碳的空氣吹入吸收池中,吸收池中反應液進入分解池后,向分解池中通入高溫水蒸汽,把二氧化碳從溶液中提取出來,在合成塔中和氫氣經化學反應使之變為可再生燃料乙醇。回答下列問題:
(1)寫出吸收池中反應的離子方程式 。
(2)從分解池中循環使用的物質是 。
|
|
| 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
提高氫碳n(H2)/n(CO2)比,對生成乙醇 (選填“不利”、“有利”或“無影響”)。
| Q | R | ||
| T | W |
查看答案和解析>>
科目:高中化學 來源: 題型:
研究人員最近發現了一種“水”電池,這種電池能利用淡水與海水之間含鹽量差別進行發電,在海水中電池總反應可表示為:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水” 電池在海水中放電時的有關說法正確的是:
A.正極反應式:Ag+Cl--e-=AgCl
B.每生成1 mol Na2Mn5O10轉移2 mol電子
C.Na+不斷向“水”電池的負極移動
D. AgCl是還原產物
查看答案和解析>>
科目:高中化學 來源: 題型:
銅是人類認識并應用最早的金屬之一,我國是最早使用銅器的國家之一。鐵與人類生活密切相關,幾乎無處不在,是地殼中含量僅次于鋁的金屬。某研究性學習小組為了證明鐵的金屬活動性比銅強,設計了如下實驗方案:
(1)將鐵片置于硫酸銅溶液中有銅析出
(2)鐵、銅和氯氣反應分別生成FeCl3和CuCl2
(3)足量的鐵粉和銅粉與濃硫酸在加熱條件下反應分別生成FeSO4和CuSO4
(4)將銅片置于FeCl3溶液中銅片逐漸溶解
(5)把鐵片和銅片置于盛有稀硫酸的燒杯中,并用導線連接,鐵片上無氣泡產生,而銅片上有氣泡產生
(6)把鐵片和銅片置于盛有濃硝酸的燒杯中,并用導線連接,鐵片上有氣泡產生,而銅片上無氣泡產生
以上實驗方案設計合理的有( )
A.兩種 B.三種
C.四種 D.五種
查看答案和解析>>
科目:高中化學 來源: 題型:
肼(H2NNH2)是一種高能燃料,有關化學反應的能量變化如圖所示,已知斷裂1mol化學鍵所需的能量(kJ):N≡N為942、O=O為500、N-N為154,則斷裂1molN-H鍵所需的能量(KJ)是
A.194 B.391 C.526.7 D.658

查看答案和解析>>
科目:高中化學 來源: 題型:
一定量的甲烷燃燒后得到的產物為CO、CO2和水蒸氣, 此混合氣體質量為49.6g, 當
其緩慢經過無水CaCl2時, CaCl2增重25.2g。原混合氣中CO2的質量為
A.12.5g B.13.2g C.19.7g D.24.4g
查看答案和解析>>
科目:高中化學 來源: 題型:
【化學——選修2:化學與技術】(15分)
化學是人類進步的關鍵,化學為人類的生產、生活提供了物質保證。
(1)電鍍時,用鍍層金屬作陽極的作用是 .
為了使鍍層厚度均勻、光滑致密、與鍍件的附著力強,除控制溶液中離子濃度外,
通常還可以采取的措施有 。
(2)鹵水中蘊含著豐富的鎂資源,經轉化后可獲得MgCl2粗產品。從鹵水中提取鎂的
步驟為:
a.將海邊大量存在的貝殼煅燒成石灰,并將石灰制成石灰乳;
b.將石灰乳加入到海水沉淀池中經過濾得到Mg(OH)2沉淀;
c.在Mg(OH)2沉淀中加入鹽酸得到MgCl2溶液,再經蒸發結晶得到MgCl2·6H2O;
d.將MgCl2·6H2O在一定條件下加熱得到無水MgCl2;
e.電解熔融的氯化鎂可得到Mg。
①步驟d中的“一定條件”指的是 ,目的是 。
上述提取鎂的流程中,為了降低成本.減少污染,可以采取很多措施,請寫出其中一點
②有同學認為:步驟b后可加熱Mg(OH)2得到MgO,再電解熔融的MgO制金屬鎂,這樣可簡化實驗步驟,你同意該同學的想法嗎?為什么?
(3)鈾是核反應最重要的燃料,已經研制成功一種螫合型離子交換樹脂,它專門吸附海水中 的U4+,而不吸附其他元素。其反應原理為 (樹脂用HR代替),發生離子交換后的離子交換膜用酸處理還可再生并得到含鈾的溶液,其反應原理為: 。
(4)阿司匹林(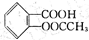 )在潮濕空氣中可分解成水楊酸和醋酸而略帶酸臭味,故密封保存,用化學方程式表示阿司匹林必須貯藏于密閉、干燥處的原因:
)在潮濕空氣中可分解成水楊酸和醋酸而略帶酸臭味,故密封保存,用化學方程式表示阿司匹林必須貯藏于密閉、干燥處的原因:
,此反應的類型屬于 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com