
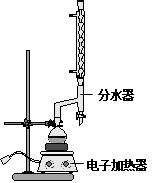
 (改編)苯甲酸乙酯(C9H10O2)稍有水果氣味,用于配制香水香精和人造精油,大量用于食品工業中,也可用作有機合成中間體、溶劑等.其制備方法為:
(改編)苯甲酸乙酯(C9H10O2)稍有水果氣味,用于配制香水香精和人造精油,大量用于食品工業中,也可用作有機合成中間體、溶劑等.其制備方法為:
| 顏色、狀態 | 沸點(℃) | 密度(g•cm-3) | |
| 苯甲酸* | 無色、片狀晶體 | 249 | 1.2659 |
| 苯甲酸乙酯 | 無色澄清液體 | 212.6 | 1.05 |
| 乙醇 | 無色澄清液體 | 78.3 | 0.7893 |
| 環己烷 | 無色澄清液體 | 80.8 | 0.7318 |
分析 (1)減少生成物能促進平衡向正反應方向移動;
(2)根據分水器中水位判斷;
(3)溫度低于苯甲酸乙酯的沸點時,苯甲酸乙酯不被蒸餾出,要使苯甲酸乙酯不被蒸餾出,則溫度應低于苯甲酸乙酯的沸點,所以溫度應低于212.6℃,但要使乙醇和環己烷蒸餾出,所以溫度應高于乙醇和環己烷的沸點;
(4)白煙是固體小顆粒,因為苯甲酸在100℃會迅速升華,所以可能是苯甲酸乙酯中混有未除凈的苯甲酸;
(5)分流漏斗的使用方法,必須將水溶液中加入乙醚,轉移至分液漏斗中,塞上玻璃塞.將分液漏斗倒轉過來,用力振搖,而且放出液體時,需將玻璃塞上的凹槽對準漏斗口上的小孔,只有這樣液體才能順利流下;
(6)蒸餾時所用的玻璃儀器有酒精燈、冷凝管、接收器、錐形瓶、蒸餾燒瓶、溫度計,由此分析解答;
(7)實驗的產率=$\frac{實際產量}{理論產量}$.
解答 解:(1)分離器分離出生成的水,減少生成物從而使該反應向正反應方向移動,提高轉化率,
故答案為:分離產生的水,使平衡向正反應方向移動,提高轉化率;
(2)當該反應完成后,就不再生成水,則加熱回流至分水器中水位不再上升,故答案為:分水器中的水層不再增加時,視為反應的終點;
(3)溫度低于苯甲酸乙酯的沸點時,苯甲酸乙酯不被蒸餾出,要使苯甲酸乙酯不被蒸餾出,則溫度應低于苯甲酸乙酯的沸點,所以溫度應低于212.6℃,但要使乙醇和環己烷蒸餾出,所以溫度應高于乙醇和環己烷的沸點80.8,故答案為:C;
(4)白煙是固體小顆粒,因為苯甲酸在100℃會迅速升華,所以可能是苯甲酸乙酯中混有未除凈的苯甲酸,加熱升華產生白煙,
故答案為:苯甲酸乙酯中混有未除凈的苯甲酸,在受熱至100℃時發生升華;
(5)分流漏斗的使用方法,必須將水溶液中加入乙醚,轉移至分液漏斗中,塞上玻璃塞.將分液漏斗倒轉過來,用力振搖,而且放出液體時,需將玻璃塞上的凹槽對準漏斗口上的小孔,只有這樣液體才能順利流下,故選:A D;
(6)蒸餾時所用的玻璃儀器有酒精燈、冷凝管、接收器、錐形瓶、蒸餾燒瓶、溫度計,故答案為:蒸餾燒瓶,溫度計;
(7)12.20g苯甲酸的物質的量為:$\frac{12.20g}{122g/mol}$=0.1mol,而生成苯甲酸乙酯的質量為:12.86mL×1.05g•ml-1=13.503g,物質的量為:$\frac{13.503g}{122g/mol}$=0.11mol,所以實驗的產率=$\frac{實際產量}{理論產量}$=$\frac{0.1}{0.11}$×100%=90%,故答案為:90%.
點評 本題考查物質制備,為高頻考點,涉及計算、儀器的選取、物質分離和提純等知識點,明確實驗原理是解本題關鍵,注意反應結束的判斷標志,題目較新穎,為易錯題.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②④ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 60% | B. | 75% | C. | 80% | D. | 85% |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
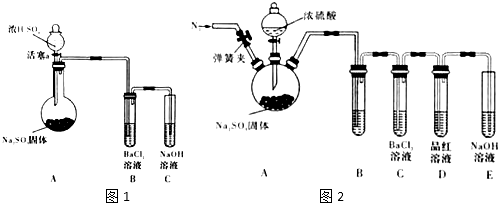
 溴乙烷是有機合成中的重要原料,實驗室合成溴乙烷的裝置示意圖、相關原理和數據如下:
溴乙烷是有機合成中的重要原料,實驗室合成溴乙烷的裝置示意圖、相關原理和數據如下:| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 溶解度 | |
| 乙 醇 | 46 | 0.789 | 78.3 | 易溶 |
| 溴乙烷 | 109 | 1.46 | 38.2 | 難溶 |
| 濃硫酸(H2SO4) | 98 | 1.84 | 338.0 | 易溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
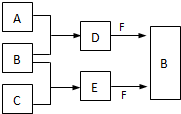 A、B、C是三種常見短周期元素的單質.常溫下D為無色液體,E是一種常見的溫室氣體.其轉化關系如圖(反應條件和部分產物略去).試回答:
A、B、C是三種常見短周期元素的單質.常溫下D為無色液體,E是一種常見的溫室氣體.其轉化關系如圖(反應條件和部分產物略去).試回答:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
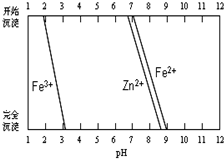 鐵酸鋅(ZnFe2O4)是對可見光敏感的半導體催化劑,其實驗室制備原理為:
鐵酸鋅(ZnFe2O4)是對可見光敏感的半導體催化劑,其實驗室制備原理為:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業廢水經處理達標后再排放 | B. | 農業生產中農藥、化肥正確使用 | ||
| C. | 禁止使用化肥、農藥 | D. | 城市垃圾妥善處理 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com