
| 物質 | pH (開始沉淀) | pH④ (完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
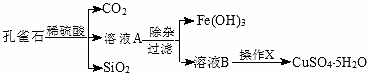
分析 孔雀石的主要成分為Cu2(OH)2CO3,還含少量FeO、Fe2O3、SiO2,加入稀硫酸反應后生成二氧化碳氣體,得到溶液A,主要成分為硫酸銅、硫酸亞鐵、硫酸鐵,過濾得到二氧化硅固體;然后將Fe2+氧化成Fe3+,再加入CuO固體調節溶液pH沉淀鐵離子過濾得到濾液為硫酸銅溶液,通過蒸發濃縮,冷卻結晶,過濾洗滌得到膽礬晶體,據此解答.
解答 解:孔雀石的主要成分為Cu2(OH)2CO3,還含少量FeO、Fe2O3、SiO2,加入稀硫酸反應后生成二氧化碳氣體,得到溶液A,主要成分為硫酸銅、硫酸亞鐵、硫酸鐵,過濾得到二氧化硅固體;然后將Fe2+氧化成Fe3+,再加入CuO固體調節溶液pH沉淀鐵離子過濾得到濾液為硫酸銅溶液,通過蒸發濃縮,冷卻結晶,過濾洗滌得到膽礬晶體,
(1)溶液A中的金屬陽離子有:Cu2+、Fe2+、Fe3+;由表中數據可知:溶液pH=9.0 時Cu2+也會沉淀;
故答案為:Cu2+、Fe2+、Fe3+;Cu2+也會沉淀;
(2)溶液A中的金屬陽離子有:Cu2+、Fe2+、Fe3+,亞鐵離子沉淀時銅離子也會沉淀,而鐵離子沉淀時銅離子不會沉淀,故應將亞鐵離子氧化為鐵離子再除去,則需要加氧化劑,雙氧水能氧化亞鐵離子且不會引入新雜質,由表中數據可知,鐵離子沉淀完全的pH為3.2,而銅離子開始沉淀的pH為4.7,調節溶液pH的范圍至3.2~4.7之間,CuO固體能中和溶液中H+使溶液的pH升高(1分),促進Fe3+水解生成Fe(OH)3沉淀;
故答案為:將Fe2+氧化成Fe3+; 3.2<pH<4.7 (或3.2~4.7之間);中和溶液中H+使溶液的pH升高,促進Fe3+水解生成Fe(OH)3沉淀 (或調節pH至Fe3+的沉淀范圍);
(3)硫酸銅溶液通過蒸發濃縮,冷卻結晶,過濾洗滌得到膽礬晶體,銅離子在水溶液中會水解,應適當酸化抑制其水解;
故答案為:蒸發濃縮;冷卻結晶;抑制Cu2+的水解.
點評 本題考查常見金屬的單質及其化合物的應用和硫酸銅結晶水含量的測定,掌握物質的制取和提純、離子的檢驗等實驗操作,分析信息是完成本題目的關鍵,題目較為綜合,難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水煤氣只能用作燃料 | |
| B. | 水煤氣是一種二級能源,比煤直接燃燒污染小 | |
| C. | 等質量的CO和H2完全燃燒時,前者放熱多 | |
| D. | 由③反應可以確定H2的燃燒熱為241.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3.01×1023個雙氫青蒿素的質量為142 g•mol-1 | |
| B. | 雙氫青蒿素中的C、H、O三種元素的質量比45:6:20 | |
| C. | 7.1 g雙氫青蒿素中含有的氫原子總數為1.2NA | |
| D. | 含有NA個碳原子的雙氫青蒿素的物質的量為1 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12.5% | B. | 14.3% | C. | 48.2% | D. | 87.5% |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 有丁達爾現象 | B. | 渾濁不透明 | ||
| C. | 能透過濾紙 | D. | 所得分散系不穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 某課外小組分別用如圖所示裝置對原電池和電解原理進行實驗探究.
某課外小組分別用如圖所示裝置對原電池和電解原理進行實驗探究.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | N4和N2是氮元素的兩種不同單質 | |
| B. | ${\;}_{7}^{14}{N}_{4}$、${\;}_{7}^{15}{N}_{2}$互為同位素 | |
| C. | 相同質量的N4和N2所含原子個數比為1:2 | |
| D. | ${\;}_{7}^{14}{N}_{4}$的摩爾質量是56g/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
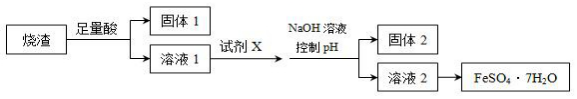
| A. | 溶解燒渣選用足量硫酸,試劑X選用鐵粉 | |
| B. | 固體1中一定含有SiO2,控制pH為使Al3+轉化為Al(OH)3,進入固體2 | |
| C. | 從溶液2得到FeSO4•7H2O產品的過程中,須控制條件防止其氧化 | |
| D. | 若改變方案,在溶液1中直接加NaOH至過量,得到的沉淀用硫酸溶解,其溶液經結晶分離也可得到FeSO4•7H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com