
國家標準(GB27602011)規定葡萄酒中SO2最大使用量為0.25 g·L-1。某興趣小組用題圖1裝置(夾持裝置略)收集某葡萄酒中SO2,并對含量 進行測定。
進行測定。
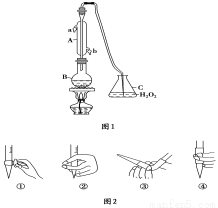
(1)圖2中①的儀器名稱 。
(2)B中加入300.00 mL葡萄酒和適量鹽酸,加熱使SO2全部逸出并與C中H2O2完全反應,其化學方程式為 。
(3)除去C中過量的H2O2,然后用0.090 0 mol·L-1 的NaOH標準溶液進行滴定,滴定前排氣泡時,應選擇圖2中的________;若滴定終點時溶液的pH=8.8,則選擇的指示劑為________;滴定的終點現象 ;若用50 mL滴定管進行實驗,當滴定管中的液面在刻度“10”處,則管內液體的體積 (填序號)___________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至終點時,消耗NaOH溶液25.00 mL,該葡萄酒中SO2含量為:___________g·L-1。
(5)該測定結果比實際值偏高,分析原因并利用現有裝置提出改進措施______________________。
 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源:2016屆黑龍江、吉林省兩省六校高三上學期期中聯考化學試卷(解析版) 題型:選擇題
以NA表示阿伏加德羅常數的值, 下列說法正確的是( )
下列說法正確的是( )
A.0.1 mol Fe與足量鹽酸反應,轉移的電子數為0.3 NA
B.0.1 mol/L氫氧化鈉溶液中所含Na+數為0.1NA
C.1 mol Na2O2與水完全反應時轉移電子數為2NA
D.46g NO 2和N2O4的混合氣體中含有的原子個數為3NA
2和N2O4的混合氣體中含有的原子個數為3NA
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市寶坻區高二11月聯考化學試卷(解析版) 題型:填空題
反應aA(s)+bB(g  cC(g)+dD(g)達到平衡時,B%跟壓強P和溫度T(T2>T1)之間的關系如圖所示(填“增大”“減小”“吸”“放”“正”“逆”)
cC(g)+dD(g)達到平衡時,B%跟壓強P和溫度T(T2>T1)之間的關系如圖所示(填“增大”“減小”“吸”“放”“正”“逆”)
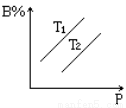
①當壓強不變時,升高溫度,B%變______,其反應為_______熱反應。
②當溫度不變,增大壓強時,B%變_______,平衡向______方向移動,方程式中系數間關系是_____。
③當溫度不變,增大壓強時,若B%不變,則方程式中系數關系是____ _。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市寶坻區高二11月聯考化學試卷(解析版) 題型:選擇題
在1100℃,一定容積的密閉容器中發生反應:FeO(s)+CO(g) Fe(s)+CO2(g) ?△H=a kJ/mol(a >0),該溫度下K=0.263,下列有關該反應的說法正確的是( )
Fe(s)+CO2(g) ?△H=a kJ/mol(a >0),該溫度下K=0.263,下列有關該反應的說法正確的是( )
A.若生成1 mol Fe,則吸收的熱量小于a kJ
B.若升高溫度,正反應速率加快,逆反應速率減慢,則化學平衡正向移動
C.若容器內壓強不隨時間變化,則可以判斷該反應已達到化學平衡狀態
D.達到化學平衡狀態時,若c(CO)=0.100 mol/L,則c(CO2)=0.0263 mol/L
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市寶坻區高二11月聯考化學試卷(解析版) 題型:選擇題
在2升的密閉容器中,發生以下反應:2A(g)+ B(g) 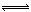 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒鐘A的平均反應速度為0.12 mol/(L·s),則10秒鐘時,容器中B的物質的量是 ( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒鐘A的平均反應速度為0.12 mol/(L·s),則10秒鐘時,容器中B的物質的量是 ( )
A.1.6 mol B.2.8 mol C.2.4 mol D.1.2 mol
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二12月月考化學試卷(解析版) 題型:選擇題
下列有關電解質溶液的說法正確的是 ( )
A、向0.1mol/L的CH3COOH溶液中加少量水,溶液中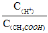 減小
減小
B、將CH3COONa溶液從20℃升溫至30℃,溶液中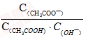 增大
增大
C、向鹽酸中加入氨水至中性,溶液中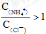
D、向AgCl、AgBr的飽和溶液中加入少量AgNO3,溶液 中
中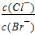 不變
不變
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省高三新考試大綱適應性考試化學卷(解析版) 題型:填空題
捕碳技術(主要指捕獲CO2)在降低溫室氣體排放中具有重要的作用。
在海洋碳循環中,通過右圖所示的途徑固碳。
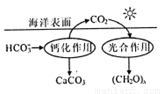
①寫出鈣化作用的離子方程式:______ ______________。
②同位素示蹤法證實光合作用釋放出的O2只來自于H2O。 用18O標記光合作用的化學方程式如下,將其補充完整。
__________+__________ (CH2O)x+x18O2+ xH2O)
(CH2O)x+x18O2+ xH2O)
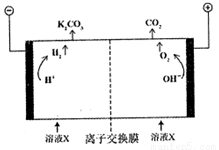
(2)工業上常用高濃度K2CO3溶液吸收CO2得到溶液X,再利用電解法使K2CO3溶液再生,并將CO2富集,其裝置如下圖。在陽極區發生的反應包括_________和H++HCO3-=H2O+CO2↑。簡述CO32-在陰極區再生的原理:______________。
(3)將上述富集的CO2和甲烷重整制合成氣(CO和H2)是CO2資源化利用的有效途徑。合成氣用干制備甲醇的反應為:2H2(g) +CO (g)  CH3OH(g) △H=-90.l kJ/mol
CH3OH(g) △H=-90.l kJ/mol
在T℃時,容積相同的甲、乙、丙三個恒容密閉容器中,按不同方式投入反應物,測得反應達到平衡時的有關數據如下表。

根據上表信息填空(填寫“>”“< ”或“=”):
2c1_________c3;②|x|+|y|___________90.1;
③2p2_________p3;④α1+α2_________1
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上第三次階段測化學試卷(解析版) 題型:選擇題
以 H2、O2、熔融鹽 Na2CO3 組成燃料電池,采用電解法制備 Fe(OH)2,裝置如下圖所示,其中 P端通入CO2。通電一段時間后,右側玻璃管中產生大量的白色沉淀,且較長時間不變色。則下列說法中正確的是
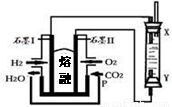
A.X、Y 兩端都必須用鐵作電極
B.不可以用 NaOH 溶液作為電解液
C.陰極發生的反應是:2H2O+2e-=H2↑+ 2OH-
D.X 端為電解池的陽極
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省高二上月考五化學卷(解析版) 題型:選擇題
工業上電解法處理含鎳酸性廢水并得到單質Ni的原理如圖所示.下列說法不正確的是
已知:
①Ni2+在弱酸性溶液中發生水解
②氧化性:Ni2+(高濃度)>H+>Ni2+(低濃度)
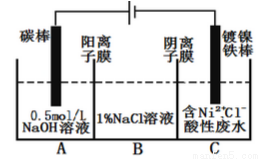
A.碳棒上 發生的電極反應:4OH﹣﹣4e﹣═O2↑+2H2O
發生的電極反應:4OH﹣﹣4e﹣═O2↑+2H2O
B.電解過程中,B中NaCl溶液的物質的量濃度將不斷減少
C.為了提高Ni的產率,電解過程中需要控制廢水pH
D.若將圖中陽離子膜去掉,將A、B兩室合并,則電解反應總方程式發生改變
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com