
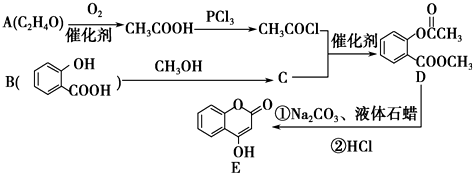
 +2NaOH $\stackrel{△}{→}$
+2NaOH $\stackrel{△}{→}$  +H2O.
+H2O. 是一種重要的有機合成中間體.
是一種重要的有機合成中間體. ;②光照時,甲苯與Cl2側鏈取代.
;②光照時,甲苯與Cl2側鏈取代.分析 (1)A的分子式為C2H4O,含有發生有機反應,含有醛基,催化氧化得到乙酸,則A為CH3CHO;
(2)由B的結構簡式可知,含有的官能團為羧基、羥基,B與甲醇發生酯化反應生成C為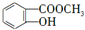 ;
;
(3)D中苯環與氫氣發生加成反應;
(4)E中酯基所得得到的羧基、酚羥基均與氫氧化鈉反應;
(5)同時滿足下列條件的B的同分異構體:①能發生銀鏡反應,說明含有醛基;②遇FeCl3發生顯色反應,說明含有酚羥基; ③1mol該物質最多可消耗2mol NaOH,結合B的結構簡式可知,含有2個-OH、1個-CHO,④核磁共振氫譜顯示其只有4種不同環境的氫原子,三個側鏈處于間位,或鄰位且-CHO處于2個-OH之間;
(6)甲苯與氯氣在光照條件下得到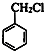 ,在氫氧化鈉水溶液、加熱條件下水解得到
,在氫氧化鈉水溶液、加熱條件下水解得到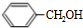 ,甲苯被酸性高錳酸鉀溶液氧化得到
,甲苯被酸性高錳酸鉀溶液氧化得到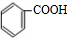 ,苯甲酸與苯甲醇在濃硫酸、加熱條件下發生轉化反應得到苯甲酸苯甲酯.
,苯甲酸與苯甲醇在濃硫酸、加熱條件下發生轉化反應得到苯甲酸苯甲酯.
解答 解:A的分子式為C2H4O,含有發生有機反應,含有醛基,催化氧化得到乙酸,則A為CH3CHO,乙酸分子羧酸中-OH被-Cl取代生成CH3COCl,B與甲醇發生酯化反應生成C為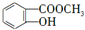 ,C與CH3COCl發生取代反應生成D,D轉化得到E.
,C與CH3COCl發生取代反應生成D,D轉化得到E.
(1)A為CH3CHO,發生銀鏡反應的化學方程式為:CH3CHO+2Ag(NH3)2OH $\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O,
故答案為:CH3CHO+2Ag(NH3)2OH $\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O;
(2)B中含氧官能團為:羧基、羥基,B與甲醇發生酯化反應生成C為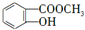 ,屬于取代反應,
,屬于取代反應,
故答案為:羧基、羥基;取代反應;
(3)D中苯環與氫氣發生加成反應,1mol D最多可與3mol H2加成,
故答案為:3;
(4)E與足量NaOH溶液完全反應的化學方程式: +2NaOH $\stackrel{△}{→}$
+2NaOH $\stackrel{△}{→}$  +H2O,
+H2O,
故答案為: +2NaOH $\stackrel{△}{→}$
+2NaOH $\stackrel{△}{→}$  +H2O;
+H2O;
(5)同時滿足下列條件的B的同分異構體:①能發生銀鏡反應,說明含有醛基;②遇FeCl3發生顯色反應,說明含有酚羥基; ③1mol該物質最多可消耗2mol NaOH,結合B的結構簡式可知,含有2個-OH、1個-CHO,④核磁共振氫譜顯示其只有4種不同環境的氫原子,為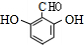 、
、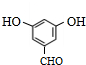 ,
,
故答案為:2;
(6)甲苯與氯氣在光照條件下得到 ,在氫氧化鈉水溶液、加熱條件下水解得到
,在氫氧化鈉水溶液、加熱條件下水解得到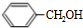 ,甲苯被酸性高錳酸鉀溶液氧化得到
,甲苯被酸性高錳酸鉀溶液氧化得到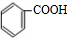 ,苯甲酸與苯甲醇在濃硫酸、加熱條件下發生轉化反應得到苯甲酸苯甲酯,合成路線流程圖為:
,苯甲酸與苯甲醇在濃硫酸、加熱條件下發生轉化反應得到苯甲酸苯甲酯,合成路線流程圖為: ,
,
故答案為: .
.
點評 本題考查有機物的推斷與合成、官能團結構與性質、性質條件同分異構體書寫等,注意掌握有機物官能團的性質和轉化,結合反應條件與有機物結構進行分析,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 甲、乙提高相同溫度 | B. | 甲中加入1molHe,乙不變 | ||
| C. | 甲降低溫度,乙不變 | D. | 甲增加1molH2,乙增加1molI2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合反應一定是氧化還原反應 | B. | 非金屬氧化物一定是酸性氧化物 | ||
| C. | 金屬氧化物一定是堿性氧化物 | D. | 堿性氧化物一定是金屬氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
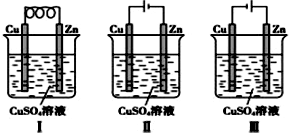
| A. | Ⅰ是原電池,Ⅱ是電鍍裝置 | |
| B. | Ⅰ、Ⅱ裝置中鋅極上均發生氧化反應 | |
| C. | Ⅱ、Ⅲ裝置中,銅極均發生氧化反應而溶解 | |
| D. | Ⅱ、Ⅲ裝置中Cu2+濃度基本不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
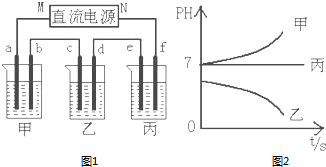 A、B、C三種強電解質,它們在水中電離出的離子如下表所示:
A、B、C三種強電解質,它們在水中電離出的離子如下表所示:| 陽離子 | Ag+ Na+ |
| 陰離子 | NO3- SO42- Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe在少量Cl2中燃燒生成FeCl2 | |
| B. | 石油的裂解、煤的干餾都是化學變化 | |
| C. | 化學反應的焓變與反應的途徑有關 | |
| D. | 等質量的銅按a、b兩種途徑完全轉化為硝酸銅,途徑a、b消耗的硝酸一樣多 途徑a:Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀硝酸}{→}$Cu(NO3)2;途徑b:Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
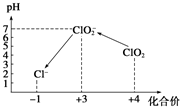 Cl2、ClO2等氣體可作為水處理等方面有廣泛應用的高效安全消毒劑.我國從2 000年起逐步用ClO2代替氯氣對飲用水進行消毒.
Cl2、ClO2等氣體可作為水處理等方面有廣泛應用的高效安全消毒劑.我國從2 000年起逐步用ClO2代替氯氣對飲用水進行消毒.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時,Mo3S4發生氧化反應 | |
| B. | 放電時,負極反應式:Mo3S4+2xe-→Mo3S42x- | |
| C. | 充電時,Mg2+向陰極遷移 | |
| D. | 充電時,陽極反應式:xMg2++2xe-→xMg |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al3+與SO42-的物質的量濃度之比為2:3 | |
| B. | 1L溶液中SO42-的物質的量為1.5mol | |
| C. | 準確稱取17.1g的Al2(SO4)3用100 mL蒸餾水溶解可配制得到該濃度的溶液 | |
| D. | 從1L 0.5 mol•L-1Al2(SO4)3溶液中取出100mL,Al3+濃度仍為1 mol•L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com