
分析 左室中氮氣的物質的量不變,令開始氮氣的物質的量為1mol,左右兩室壓強相同,體積之比等于物質的量之比,據此計算開始右室中氫氣與氧氣的物質的量,反應后左右體積相等,則右室剩余氣體的物質的量為1mol,該氣體可能是氧氣或氫氣,根據差量法計算,原混合氣體中氫氣、氧氣的物質的量,進而計算體積比.
解答 解:左室中氮氣的物質的量不變,令開始氮氣的物質的量為1mol,左右兩室壓強相同,體積之比等于物質的量之比,故開始右室中氫氣與氧氣的物質的量為1mol×$\frac{\frac{3}{4}}{\frac{1}{4}}$=3mol,反應后左右體積相等,則右室剩余氣體的物質的量為1mol,則:
2H2+O2=2H2O 氣體物質的量減少△n
2 1 3
$\frac{4}{3}$mol $\frac{2}{3}$mol 3mol-1mol=2mol
若剩余氣體為氫氣,則原混合氣體中氧氣為$\frac{2}{3}$mol,則氫氣為3mol-$\frac{2}{3}$mol=$\frac{7}{3}$mol,H2和O2的體積比為$\frac{7}{3}$mol:$\frac{2}{3}$mol=7:2,
若剩余氣體是氧氣,則原混合氣體中氫氣為$\frac{4}{3}$mol,則氫氣為3mol-$\frac{4}{3}$mol=$\frac{5}{3}$mol,H2和O2的體積比為$\frac{4}{3}$mol:$\frac{5}{3}$mol=4:5,
故答案為:4:5、7:2.
點評 本題考查化學計算、阿伏伽德羅定律等,難度中等,根據左室氮氣的物質的量利用體積判斷右室氣體的物質的量是關鍵.


 華東師大版一課一練系列答案
華東師大版一課一練系列答案科目:高中化學 來源: 題型:選擇題
| A. | v(B)=0.03mol•L-1•s-1 | B. | v(B)=0.045mol•L-1•s-1 | ||
| C. | v(C)=0.03mol•L-1•s-1 | D. | v(C)=0.06mol•L-1•s-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 軟脂酸和油酸互為同系物 | |
| B. |  的命名為:3-甲基-2-丁醇 的命名為:3-甲基-2-丁醇 | |
| C. | 苯酚能與溴水反應,苯不能與溴水反應,說明羥基對苯環有影響 | |
| D. | 與 互為同分異構體的芳香族化合物有4種 互為同分異構體的芳香族化合物有4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 名稱 | 托盤天平(帶砝碼) | 小燒杯 | 坩堝鉗 | 玻璃棒 | 藥匙 | 量筒 |
| 儀器 |  |  |  |  |  |  |
| 序號 | a | b | c | d | e | f |
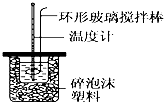
| 溫度 實驗次數 | 起始溫度t1/℃ | 終止溫 度t2/℃ | 平均溫度差 (t2-t1)/℃ | ||
| H2SO4溶液 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 請填寫(4.0℃ ) |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | x:y等于等質量的甲和乙的分子個數之比 | |
| B. | x:y等于同溫同壓下甲和乙的密度之比 | |
| C. | x:y等于甲與乙的相對分子質量之比 | |
| D. | x:y等于同溫同體積下等質量的甲和乙的壓強之比 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com