
【題目】中藥麻黃成分中含有生物堿、黃酮、鞣質、揮發油、有機酚、多糖等許多成分,其中一種有機酚的結構簡式如圖。下列說法正確的是( )
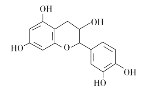
A.分子中所有碳原子可以處于同一平面
B.分子中含有2個手性原子
C.1mol該有機物跟足量濃溴水反應,最多消耗5molBr2
D.1mol該有機物與NaOH溶液反應最多消耗5molNaOH
 一諾書業暑假作業快樂假期云南美術出版社系列答案
一諾書業暑假作業快樂假期云南美術出版社系列答案科目:高中化學 來源: 題型:
【題目】如圖是部分短周期元素化合價與原子序數的關系圖,下列說法正確的是( )

A.原子半徑:Z>Y>X
B.氣態氫化物的熱穩定性:W>R
C.WX3和水反應生成的化合物是離子化合物
D.X元素在自然界中存在同素異形現象
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:氧化鋰(Li2O)晶體形成過程中的能量變化如圖所示
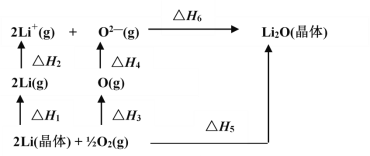
下列說法正確的是
A. △H1< 0,△H2>0B. -△H5 +△H1 +△H1 +△H3+△H4 +△H6 =0
C. △H3<0,△H4 < 0D. △H1+ △H2+△H3 +△H4 =△H5+△H6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向某濃度的二元弱酸H2C2O4溶液中逐滴加入NaOH溶液,pC與溶液pH的變化關系如圖所示(pC=-lgx,x表示溶液中溶質微粒的物質的量濃度)。下列說法正確的是
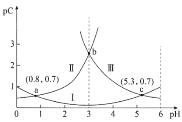
A.常溫下,H2C2O4的Ka1=100.8
B.pH=3時,溶液中![]()
C.pH由0.8增大到5.3的過程中,水的電離程度逐漸增大
D.常溫下,隨著pH的增大,![]() 的值先增大后減小
的值先增大后減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物苯:常常作為工農業生產中的良好溶劑。
(1)若將苯倒入盛有碘水的試管中,振蕩后靜置,現象是__________________________,說明苯的密度比水_________,且________________。
(2)若將乒乓球碎片、食鹽固體分別加入盛有苯的試管中,振蕩后靜置,現象是___________________,說明苯是很好的_____________________________。
(3)將盛有苯的兩支試管分別插入100℃的沸水和0℃的冰水的現象是________________________,說明苯的沸點_________________,熔點_________。
人們對苯的認識有一個不斷深化的過程。
(4)由于苯的含碳量與乙炔相同,人們認為它是一種不飽和烴,寫出分子式為C6H6的一種含兩個三鍵且無支鏈的鏈烴的結構簡式_____________________________________。
(5)已知分子式為C6H6的有機物有多種,其中的兩種為:
(I)![]() (II)
(II)![]() 這兩種結構的區別表現在以下兩方面:
這兩種結構的區別表現在以下兩方面:
①定性方面(即化學性質方面):(II)能___________(填字母),而(I)不能。
a. 被高錳酸鉀酸性溶液氧化 b. 與溴水發生取代反應
c. 與溴發生取代反應 d. 與氫氣發生加成反應
②定量方面(即消耗反應物的量的方面):1molC6H6與H2加成時:(I)需要H2______mol,而(II)需要H2_____mol。
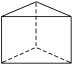
(6)今發現C6H6還可能有另一種如右圖所示的立體結構,該結構的一氯代物有_________種;現代化學認為苯分子中碳碳之間的鍵是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈹銅是廣泛應用于制造高級彈性元件的良好合金。某科研小組從某舊鈹銅元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收鈹和銅兩種金屬的工藝流程如圖:

已知:Ⅰ.鈹、鋁元素的化學性質相似,單質鈹與氫氧化鈉溶液反應生成可溶于水的Na2BeO2
Ⅱ.常溫下部分難溶物的溶度積常數如下表:
難溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
溶度積常數(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)濾液A的主要成分除NaOH外,還有___(填化學式),寫出反應I中含鈹化合物與過量鹽酸反應的離子方程式:___。
(2)濾液C中含NaCl、BeCl2和少量HCl,為提純BeCl2,最合理的實驗步驟順序為___(填字母)。
a.加入過量的氨水
b.通入過量的CO2
c.加入過量的NaOH
d.加入適量的HCl
e.洗滌
f.過濾
(3)①MnO2能將金屬硫化物中的硫元素氧化為硫單質。寫出反應Ⅱ中CuS發生反應的化學方程式:___。
②若用濃HNO3溶解金屬硫化物,缺點是___(任寫一條)。
(4)濾液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水調節pH可將其依次分離,首先沉淀的是___(填離子符號),為使銅離子開始沉淀,常溫下應調節溶液的pH大于___。
(5)電解NaCl-BeCl2混合熔鹽可制備金屬鈹,如圖是電解裝置圖。
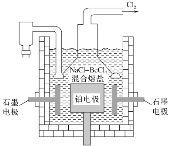
①石墨電極上的電極反應式為___。
②電解得到的Be蒸氣中約含1%的Na蒸氣,除去Be中少量Na的方法為___。
已知部分物質的熔、沸點如下表:
物質 | 熔點(K) | 沸點(K) |
Be | 1551 | 3243 |
Na | 370 | 1156 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸鎳是電鍍工業必不可少的化工原料。從不銹鋼廢渣(主要含Fe42.35%、Cr9.67%、Ni5.1%、C4.7%、Si3.39%等)中制取硫酸鎳晶體的工藝流程如圖:
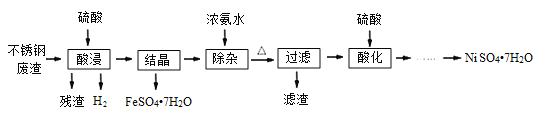 已知:①Cr3+與氨水反應時有少量Cr3+生成[Cr(NH3)6]3+,但加熱時該絡合物易分解。Ni2+與氨水反應生成[Ni(NH3)6]2+,該絡合物加熱時穩定,用硫酸酸化時生成相應的硫酸鹽。
已知:①Cr3+與氨水反應時有少量Cr3+生成[Cr(NH3)6]3+,但加熱時該絡合物易分解。Ni2+與氨水反應生成[Ni(NH3)6]2+,該絡合物加熱時穩定,用硫酸酸化時生成相應的硫酸鹽。
②Na2CrO4溶液中加酸調節pH為3.5時,CrO42-轉化為Cr2O72-。
③相關物質在不同溫度時溶解度如下表:
溫度 溶解度/g 物質 | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 90℃ |
Na2SO4 | 19.5 | 40.8 | 48.8 | 45.3 | 43.7 | 42.7 |
Na2Cr2O7 | 183 | 198 | 215 | 269 | 376 | 405 |
(1)“酸浸”后得到的溶液中主要含有FeSO4、NiSO4、Cr2(SO4)3,生成NiSO4的化學方程式為___。“酸浸”時需控制溫度為90℃左右,可以采用的加熱方式是___。
(2)“過濾”前,適當加熱的目的是___。
(3)對“過濾”所得的濾渣進行洗滌,檢驗濾渣已洗滌干凈的方法是___。
(4)“過濾”時產生的濾渣可用于制備Na2Cr2O7晶體。
①濾渣經干燥后與Na2CO3混合在空氣中煅燒生成Na2CrO4和CO2,此反應的化學方程式為___。
②請補充完整上述煅燒后混合物制備Na2Cr2O7晶體(橙紅色)的實驗方案:水浸,過濾,___,烘干得Na2Cr2O7晶體(必須使用的試劑有:硫酸,蒸餾水)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對可逆反應4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列敘述中正確的是( )
4NO(g)+6H2O(g),下列敘述中正確的是( )
A.達到化學平衡時4υ正(O2)=5υ逆(NO)
B.若單位時間內生成xmolNO的同時,消耗xmolNH3,則反應達平衡狀態
C.達到化學平衡時,若升高溫度,則正反應速率減小,逆反應速率增大
D.平衡時混合物中可能各物質的濃度相等,且保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物P是合成抗腫瘤藥物的中間體,其合成路線如下:
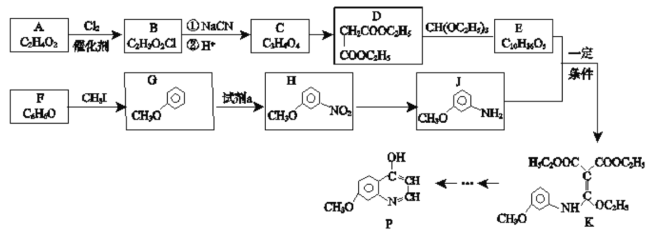
已知:RCl![]() RCOOH
RCOOH
(1)H的官能團名稱___________。寫出E的結構簡式___________。
(2)B→C中①的化學方程式___________。
(3)檢驗F中官能團的試劑及現象_________。
(4)D的同分異構體有多種,其中滿足以下條件的有________種。
①1mol D能與足量 NaHCO3反應放出2mol CO2
②核磁共振氫譜顯示有四組峰
(5)H→J的反應類型___________。
(6)已知: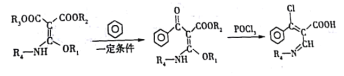
K經過多步反應最終得到產物P:
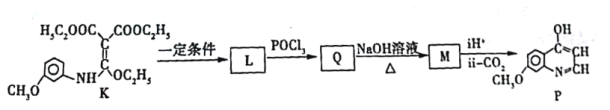
①K→L的化學方程式___________。
②寫出M的結構簡式___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com