
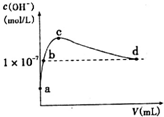
 常溫下,向l L pH=l0的NaOH溶液中持續通入CO2.通入CO2的體積(y)與溶液中水電離出的c(OH-)的關系如圖所示.下列敘述錯誤的是( )
常溫下,向l L pH=l0的NaOH溶液中持續通入CO2.通入CO2的體積(y)與溶液中水電離出的c(OH-)的關系如圖所示.下列敘述錯誤的是( )| A. | a點溶液中:水電離出的c(H+)=1×10-10mol•L-1 | |
| B. | b點溶液中:c(H+)=1×10-7mol•L-1 | |
| C. | c點溶液中:c(Na+)>c(HCO3-)>c(CO32-) | |
| D. | d點溶液中:c(Na+)=2c(CO32-)+c(HCO3-) |
分析 A.a點溶液中的溶質是NaOH,水電離出的c(H+)=10-pH;
B.常溫下,c(OH-)=1×10-7mol/L,溶液呈中性;
C.c點溶液中,當水電離出的OH-離子濃度最大時,說明此時的溶液是碳酸鈉溶液,碳酸根離子水解生成碳酸氫根離子但程度較小;
D.d點溶液中,溶液呈中性,溶液中存在電荷守恒,根據電荷守恒判斷.
解答 解:A.a點溶液中的溶質是NaOH,水電離出的c(H+)=10-pH=1×10-10mol•L-1,故A正確;
B.常溫下,c(OH-)=1×10-7mol/L,溶液呈中性,則c(OH-)=c(H+),所以c(H+)=1×10-7mol•L-1,故B正確;
C.c點溶液中,當水電離出的OH-離子濃度最大時,說明此時的溶液是碳酸鈉溶液,碳酸根離子水解生成碳酸氫根離子但程度較小,所以離子濃度大小順序是c(Na+)>c(CO32-)>c(HCO3-),故C錯誤;
D.d點溶液中,溶液呈中性,則c(OH-)=c(H+),溶液中存在電荷守恒,根據電荷守恒得c(Na+)=2c(CO32-)+c(HCO3-),故D正確;
故選C.
點評 本題考查離子濃度大小比較,為高頻考點,明確溶液中的溶質及其性質是解本題關鍵,結合電荷守恒進行解答,注意計算堿性溶液中水電離出氫離子和氫氧根離子的方法.


科目:高中化學 來源: 題型:解答題
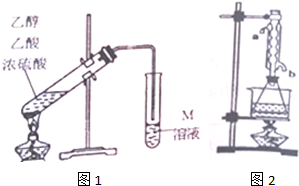
| 相對分子質量 | 沸點(℃) | |
| 乙醇 | 46 | 78.5 |
| 乙酸 | 60 | 117.9 |
| 乙酸乙酯 | 88 | 77.1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
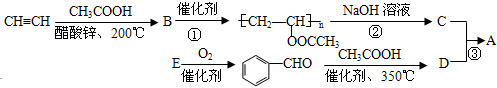
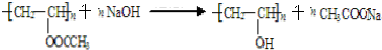 ;反應類型是取代反應.
;反應類型是取代反應. .
.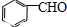 能發生銀鏡反應,該反應的化學方程式是
能發生銀鏡反應,該反應的化學方程式是 .
.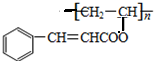 ,關于A的性質下列說法正確的是acd(填字母).
,關于A的性質下列說法正確的是acd(填字母).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
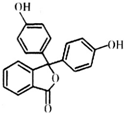 酚酞醫藥名為果桃,可治療消化系統疾病,其有效成分的結構簡式如圖所示.下列對該有效成分的說法正確的是( )
酚酞醫藥名為果桃,可治療消化系統疾病,其有效成分的結構簡式如圖所示.下列對該有效成分的說法正確的是( )| A. | 所有原子可能共平面 | |
| B. | 能發生加聚反應生成高分子化合物 | |
| C. | 酚酞的水解產物中含有醇羥基 | |
| D. | 1 mol該物質最多能與含4 mol NaOH的燒堿溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{8}^{18}$O2是${\;}_{8}^{16}$O2的同分異構體 | |
| B. | ${\;}_{8}^{18}$O2是O3的一種同素異形體 | |
| C. | ${\;}_{8}^{18}$O2與${\;}_{8}^{16}$O2互為同位素 | |
| D. | 1mol ${\;}_{8}^{18}$O2分子中含有20mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
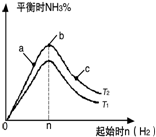 在某溫度時按n(N2):n(H2)=1:3的比例將混合氣體投入密閉容器中反應:N2(g)+3H2(g)═2NH3(g)△H<0;
在某溫度時按n(N2):n(H2)=1:3的比例將混合氣體投入密閉容器中反應:N2(g)+3H2(g)═2NH3(g)△H<0;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “地溝油”可以生產“生物燃料”,生物燃料本質上能量來源于太陽能 | |
| B. | 消除水體中的HgCl2污染可利用微生物使其轉化為有機汞CH3HgCl | |
| C. | 人體內沒有能使纖維素水解成葡萄糖的酶,但可以加強胃腸蠕動,有助于消化,因此纖維素是人類的營養食物 | |
| D. | 半導體行業中有一句話:“從沙灘到用戶”,計算機芯片的材料是經提純的二氧化硅 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
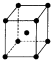 前四周期原子序數依次增大的六種元素A,B,D,X,Y,Z,基態時核外電子排布具有以下特征:A的電子層數和最外層電子數相等,非金屬元素B的已成對電子數是未成對電子數的2倍,且A和B位于不同周期;D和X的價電子層中未成對電子均只有1個,并且D-和X+的電子相差為8;Y、Z與X位于同一周期,它們價電子層中的未成對電子數分別為4和2,且原子序數相差為2.回答下列問題:
前四周期原子序數依次增大的六種元素A,B,D,X,Y,Z,基態時核外電子排布具有以下特征:A的電子層數和最外層電子數相等,非金屬元素B的已成對電子數是未成對電子數的2倍,且A和B位于不同周期;D和X的價電子層中未成對電子均只有1個,并且D-和X+的電子相差為8;Y、Z與X位于同一周期,它們價電子層中的未成對電子數分別為4和2,且原子序數相差為2.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com