
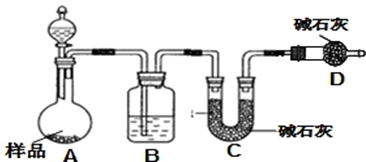
分析 (1)方案一原理為在加熱的條件下Na2CO3能夠穩定存在,而NaHCO3較易發生如下的分解反應2NaHCO3=Na2CO3+CO2↑+H2O,從而可根據其反應產生的CO2和水蒸汽H2O的量或殘留的固體的量推算出小蘇打樣品中純堿的質量分數;
(2)方案二原理為一定量混合樣品與足量的稀硫酸分別發生如下反應Na2CO3+H2SO4=Na2SO4+CO2↑+H2O,2 NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O↑,根據所產生的CO2的質量,可以分別求得樣品中Na2CO3和NaHCO3的質量從而得出純堿的質量分數.該方案關鍵是要獲得產生的CO2的質量,自然在實驗前要檢查裝置的氣密性,要將裝置中的CO2全部被堿石灰所吸收,要稱量堿石灰在吸收CO2前后的質量;
①制備氣體實驗,實驗前應先檢驗裝置氣密性;
②鹽酸具有揮發性,會影響實驗結果,D干燥管中的堿石灰吸收空氣中的水蒸氣、二氧化碳,防止進入C;
③實驗根據C裝置前后質量變化判斷生成二氧化碳的質量;
(3)方案三原理為在樣品中加入BaCl2溶液,其中Na2CO3可與BaCl2發生反應Na2CO3+BaCl2=BaCO3↓+2NaCl,而NaHCO3與BaCl2則不反應.從而根擗產生的沉淀量,得出純堿的質量分數,方案關鍵是測定BaCO3沉淀的質量,自然要保證沉淀完全,要正確過濾好,
①根據過濾具體操作判斷所需儀器;
②試驗中判斷沉淀是否完全的方法是:取少量濾液,再滴加BaCl2溶液少許,如無白色沉淀出現,說明沉淀完全;
③在一定量樣品中加入足量Na2CO3可與BaCl2發生反應Na2CO3+BaCl2=BaCO3↓+2NaCl,而NaHCO3與BaCl2則不反應,根據BaCO3沉淀的量,就可得出純堿的質量分數.
解答 解:(1)實驗中加熱時碳酸氫鈉發生分解,反應的方程式為2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
故答案為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(2)①該方案是要獲得產生的CO2的質量,在實驗前要檢查裝置的氣密性,
故答案為:檢查裝置的氣密性;
②鹽酸具有揮發性,會影響實驗結果,所以選擇稀硫酸;D干燥管中的堿石灰吸收空氣中的水蒸氣、二氧化碳,防止進入C被吸收,減少誤差,
故答案為:吸收空氣中的水蒸氣、二氧化碳,防止進入C被吸收;
③根據所產生的CO2的質量及樣品質量,分別求得樣品中Na2CO3和NaHCO3的質量從而得出純堿的質量分數,所以需稱量C裝置前后質量變化判斷生成二氧化碳的質量.
故答案為:C;
(3)①過濾操作中,除了燒杯外還用到漏斗、玻璃棒,
故答案為:漏斗、玻璃棒;
②試驗中判斷沉淀是否完全的方法是:取少量濾液,再滴加BaCl2溶液少許,如無白色沉淀出現,說明沉淀完全,
故答案為:取少量濾液,再滴加BaCl2溶液少許,如無白色沉淀出現,說明沉淀完全;
③在一定量樣品中加入足量Na2CO3可與BaCl2發生反應Na2CO3+BaCl2=BaCO3↓+2NaCl,而NaHCO3與BaCl2則不反應,根據題意可知,BaCO3沉淀的質量為19.7g,即為0.1mol,所以碳酸鈉的物質的量為0.1mol,即質量為10.6g,所以純堿的質量分數為$\frac{10.6g}{20g}$×100%=53%,
故答案為:53%.
點評 本題以實驗探究“測定放置已久的小蘇打樣品中純堿的質量分數”為載體,考查學生對于實驗原理與裝置理解評價、實驗基本操作、化學計算等,題目難度中等,題目涉及到的小蘇打和純堿的化學知識是多方面的,構成了一道多角度的探究題.


 狀元坊全程突破導練測系列答案
狀元坊全程突破導練測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳的結構式:O-C-O | B. | 過氧化鈉的電子式: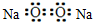 | ||
| C. | 丙烷分子的球棍模型: | D. | Cl-的結構示意圖: |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18gH2O含有的氫原子數目為NA | |
| B. | 標準狀況下,22.4LCO2含有的分子數目為NA | |
| C. | 1L1mol•L-1K2SO4溶液中含有的鉀離子數目為NA | |
| D. | 1molH2在O2中完全燃燒轉移的電子數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過氧化鈉和水反應 Na2O2+H2O=2Na++2OH-+O2↑ | |
| B. | 金屬鋁溶于氫氧化鈉溶液:Al+2OH-=AlO2-+H2↑ | |
| C. | Ca(ClO)2溶液中通入少量二氧化碳:ClO-+H2O+CO2=HClO+CO32- | |
| D. | 向氯化鋁溶液中滴入足量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
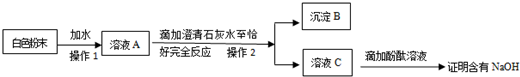
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Y>Z>W | |
| B. | Z的最高價氧化物的水化物為強酸 | |
| C. | 非金屬性最強的元素為W | |
| D. | XW2分子中各原子最外層電子均達到8電子結構 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 136 | B. | 50 | C. | 86 | D. | 222 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com