
���� ��1���������i�c���}���ڼӟ�l���������Ȼ��i���Ț⡢ˮ��
��2���Ț��cˮ���������Ȼ���ʹ����
��3�����������c̼�������ɹ��һ����̼��
��4���Ȼ��F�c�~���������Ȼ����F���Ȼ��~��
��5�����߷������ɚ������X��̼����c��
��� �⣺��1���������i�c���}���ڼӟ�l���������Ȼ��i���Ț⡢ˮ���x�ӷ���ʽ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
�ʴ𰸞飺MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
��2���Ț��cˮ���������Ȼ���ʹ����ᣬ�x�ӷ���ʽ��Cl2+H2O?H++Cl-+HClO��
�ʴ𰸞飺Cl2+H2O?H++Cl-+HClO��
��3�����������c̼�������ɹ��һ����̼�����W����ʽ��SiO2+2C$\frac{\underline{\;�ߜ�\;}}{\;}$Si+2CO����
�ʴ𰸞飺SiO2+2C$\frac{\underline{\;�ߜ�\;}}{\;}$Si+2CO����
��4���Ȼ��F�c�~���������Ȼ����F���Ȼ��~���x�ӷ���ʽ��2Fe3++Cu=2Fe2++Cu2+��
�ʴ𰸞飺2Fe3++Cu=2Fe2++Cu2+��
��5�����߷������ɚ������X��̼����c���x�ӷ���ʽ��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�ʴ𰸞飺AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�c�u ���}�������x�ӷ���ʽ�ĕ��������_���|�����|���x�ӷ�������ʽ���������ǽ��}�P�I���}Ŀ�y�Ȳ���


 �_���ܠ�Ԫ�yԇ��ϵ�д�
�_���ܠ�Ԫ�yԇ��ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | �˜ʠ�r�£�22.4LNO�c11.2LO2��ϣ���Ϛ��w�������Ӕ�(sh��)��NA | |
| B�� | 1molAl3+���еĺ�����Ӕ�(sh��)��10NA | |
| C�� | ���س����£�1mol���⺬�е�ԭ�ӿ���(sh��)��NA | |
| D�� | 1L1mol/LFeCl3��Һȫ���Ƴ��z�w�����к��z���Ĕ�(sh��)ĿС��NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
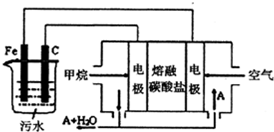 늸��x���۷��ǹ��I(y��)�ϲ��õ�һ�N��ˮ̎��������ͨ�^늽���ˮ��K���ɵ�Fe��OH��3������������e�����_����ˮ��Ŀ�ģ�ꎘO�a���Ě��ݰ���ˮ�БҸ����ˮ���γɸ����ӣ���ȥ�����ӣ������˸��x���������ã�ij����С�M��������ԭ�����OӋ����D��ʾ���b�ã�
늸��x���۷��ǹ��I(y��)�ϲ��õ�һ�N��ˮ̎��������ͨ�^늽���ˮ��K���ɵ�Fe��OH��3������������e�����_����ˮ��Ŀ�ģ�ꎘO�a���Ě��ݰ���ˮ�БҸ����ˮ���γɸ����ӣ���ȥ�����ӣ������˸��x���������ã�ij����С�M��������ԭ�����OӋ����D��ʾ���b�ã��鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
| A�� | ��ˮ | B�� | �����\ | C�� | �����c | D�� | �Ȼ��~ |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
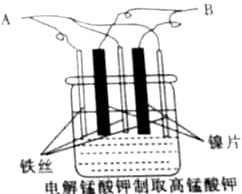 �Ƃ�KMnO4����ѷ�����늽ⷨ����������Ƭ�������c���������F�z��늘O��늽�K2MnO4��ˮ��Һ���Gɫ���Ƃ�KMnO4���b����D��
�Ƃ�KMnO4����ѷ�����늽ⷨ����������Ƭ�������c���������F�z��늘O��늽�K2MnO4��ˮ��Һ���Gɫ���Ƃ�KMnO4���b����D���鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| �x� | ������ | ���F(xi��n)�� | �YՓ |
| A | ��KI��Һ�м���CCl4����ʎ���o�� | Һ�w�ӣ��ӳ��ϼtɫ | ��������CCl4���y����ˮ |
| B | ��Fe��NO3��2��Ʒ����ϡH2SO4 | ��Һ��׃�t | ϡ���������Fe2+ |
| C | ��SO2ͨ��Ba��N03��2��Һ�� | �o���@�F(xi��n)�� | SO2�cBa��NO3��2������ |
| D | ��������Һ�c����Cu��OH��2��ϼӟ� | ���ɴu�tɫ���� | �����Ƿ����к���ȩ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | �������ȉ�������׃�����t�f��ԓ�������_ƽ�� | |
| B�� | ����ǰH2S���|������2.5mol | |
| C�� | CO��H2S�_ƽ�����D������ͬ | |
| D�� | ��ƽ����ټ���CO���t���������������淴�����ʜpС |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | �����wϵ�ضȣ�ƽ�ⳣ��(sh��)K�pС | |
| B�� | �����wϵ������ƽ�ⳣ��(sh��)K���l(f��)��׃�� | |
| C�� | ƽ�ⳣ��(sh��)���_ʽ��K=$\frac{[CO][{H}_{2}]}{[C][{H}_{2}O]}$ | |
| D�� | ����C��s��������ƽ�������Ƅ� |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com