
 ;
;分析 (1)P元素基態原子電子排布為1s22s22p63s23P3,所以3P能級上電子排布圖為 ;
;
(2)在白磷分子(P4)中,P原子在由4個P原子構成的正四面體上,形成6個P-P單鍵,所以鍵角為60°;
(3)根據價層電子對互斥理論確定分子或離子中中心原子的價層電子對數,再判斷雜化類型;
(4)PCl5是一種白色晶體,在恒容密閉容器中加熱可在148℃液化,形成一種能導電的熔體,說明生成自由移動的陰陽離子,一種正四面體形陽離子是PCl4+和一種正六面體形陰離子是PCl6-,即發生反應為:2PCl5=PCl4++PCl6-;
(5)PBr5氣態分子的結構與PCl5相似,說明PBr5也能電離出能導電的陰陽離子,而產物中只存在一種P-Br鍵長,所以發生這樣電離PBr5═PBr4++Br-.
解答 解:(1)P元素基態原子電子排布為1s22s22p63s23P3,所以3P能級上電子排布圖為 ,故答案為:
,故答案為: ;
;
(2)在白磷分子(P4)中,P原子在由4個P原子構成的正四面體上,形成6個P-P單鍵,所以每個分子中含6個σ鍵,鍵角為60°,故答案為:6;60○;
(3)PCl3分子中P的價層電子對數=3+$\frac{1}{2}$(5-3×1)=4,屬于sp3雜化,故答案為:sp3;
(4)PCl5是一種白色晶體,在恒容密閉容器中加熱可在148℃液化,形成一種能導電的熔體,說明生成自由移動的陰陽離子,一種正四面體形陽離子是PCl4+和一種正六面體形陰離子是PCl6-,即發生反應為:2PCl5=PCl4++PCl6-,故答案為:PCl4+和PCl6-;
(5)PBr5氣態分子的結構與PCl5相似,說明PBr5也能電離出能導電的陰陽離子,而產物中只存在一種P-Br鍵長,所以發生這樣電離PBr5═PBr4++Br-,故答案為:PBr5═PBr4++Br-.
點評 本題考查物質結構和性質,涉及電子排布圖、雜化方式的判斷、電離方式和微粒結構等,側重于基礎知識的綜合應用的考查,題目難度中等.


科目:高中化學 來源: 題型:解答題
| 序號 | a | b | c | d | e | f |
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaAlO2 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
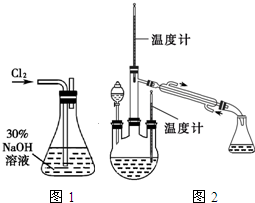 肼是重要的化工原料.某探究小組利用下列反應制取水合肼(N2H4•H2O).
肼是重要的化工原料.某探究小組利用下列反應制取水合肼(N2H4•H2O).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬和漂白粉常用于自來水的凈化和殺菌消毒,兩者的作用原理相同 | |
| B. | 石油裂解、煤的氣化、海水制鎂等過程中都包含化學變化 | |
| C. | 煤經氣化、液化和干餾三個物理變化過程,可變為清潔能源 | |
| D. | 通過化學變化可以實現235U與238U的相互轉化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 推測 | 操作和現象 | 結論 |
| 雜質中的正鹽成分可能有: A,、Na2S B,、Na2CO3 C,、Na2SO4 D,、Na2SO3 | ①取Wg產品配成稀溶液; ②向溶液中滴加過量BaCl2溶液,有白色沉淀生成,過濾,得沉淀和濾液; ③向沉淀中加入過量鹽酸,沉淀完全溶解,并有刺激性氣味的氣體產生. ④向濾液滴加2滴淀粉溶液,再逐滴加0.1000mol•L-1碘的標準溶液,消耗碘的標準溶液體積為18.10mL. | 產品雜質中: 一定含有Na2SO3, 可能含有Na2CO3Na2S, 一定不含有Na2SO4. 操作④發生的反應是: 2S2O32-+I2═S4O${\;}_{6}^{2-}$+2I- Ⅰ、判斷達到滴定終點的現象是溶液由無色變藍色,且半分鐘不褪色 Ⅱ、產品純度:(9/W)×100%. |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
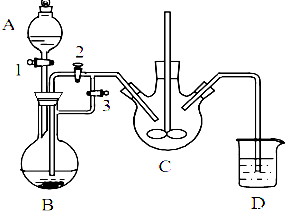 乳酸亞鐵([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一種常用的補鐵劑,可通過乳酸與碳酸亞鐵反應制得:
乳酸亞鐵([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一種常用的補鐵劑,可通過乳酸與碳酸亞鐵反應制得:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | M只能是堿類 | B. | M只能是鹽類 | C. | M一定為電解質 | D. | M可能為非電解質 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com