
【題目】水鈷礦中除SiO2外,還有9.24%CoO、2.78%Fe2O3、0.96%MgO、0.084%CaO。


(1)在一定濃度的![]() 溶液中,鈷的浸出率隨時間、溫度的變化如圖1所示
溶液中,鈷的浸出率隨時間、溫度的變化如圖1所示![]() 考慮生產成本和效率,最佳的浸出時間為______小時,最佳的浸出溫度為______
考慮生產成本和效率,最佳的浸出時間為______小時,最佳的浸出溫度為______![]()
(2)請配平下列除鐵的化學方程式:____________
_ _Fe2(SO4)3+ H2O + Na2CO3 == Na2Fe6(SO4)4(OH)12↓+ Na2SO4 + CO2↑
(3) “除鈣、鎂”的原理反應為:![]() ;
;![]() 已知
已知![]() ,加入過量NaF溶液反應完全后過濾,則濾液中
,加入過量NaF溶液反應完全后過濾,則濾液中![]() ____________________.
____________________.
(4) “沉淀”中含雜質離子主要有![]() 、
、![]() 、_________和__________;“操作X”包括_________和_________。
、_________和__________;“操作X”包括_________和_________。
(5)某鋰離子電池正極是![]() ,含
,含![]() 導電固體為電解質
導電固體為電解質![]() 充電時,
充電時,![]() 還原為Li,并以原子形式嵌入電池負極材料碳
還原為Li,并以原子形式嵌入電池負極材料碳![]() 中
中![]() 如圖2所示
如圖2所示![]() 電池反應為
電池反應為![]()
![]()
![]() ,寫出該電池放電時的正極反應式 ________________________________________.
,寫出該電池放電時的正極反應式 ________________________________________.
【答案】 12 90 ![]()
![]() =1.5
=1.5 ![]()
![]() 洗滌 干燥
洗滌 干燥 ![]()
【解析】根據流程圖,浸出時間越長浸出率越高,溫度越高,浸出率越高,但浸出12h后,浸出率變化不大,90℃和120℃浸出率相差不大,且時間過長,溫度過高導致成本較大,所以最佳的浸出時間為12h,最佳的浸出溫度為90℃。
(2)除鐵反應為非氧化還原反應,根據原子守恒配平方程式,所以其方程式為:3Fe2(SO4)3+6H2O +6Na2CO3 ==Na2Fe6(SO4)4(OH)12↓+5Na2SO4 +6 CO2↑,因此,本題答案為:![]()
(3)由Ksp(CaF2)=c(Ca2+)![]() c2(F-)=1.11
c2(F-)=1.11![]() 10-10,Ksp(MgF2)= c(Mg2+)
10-10,Ksp(MgF2)= c(Mg2+)![]() c2(F-)=7.40
c2(F-)=7.40![]() 10-11
10-11
![]() =
=![]() =1.5
=1.5
(4)流程中加入的Na+、![]() 、
、![]() 、NH4+ 未除去,因此 “沉淀”中含雜質離子主要有
、NH4+ 未除去,因此 “沉淀”中含雜質離子主要有![]() 、
、![]() 、
、![]() 、
、![]() ;對過濾后的沉淀進行洗滌、干燥后能得到草酸鈷晶體。因此本題正確答案為:
;對過濾后的沉淀進行洗滌、干燥后能得到草酸鈷晶體。因此本題正確答案為: ![]() ;
;![]() ;洗滌 ;干燥。
;洗滌 ;干燥。
(5)放電時,該電池是原電池,原電池正極發生還原反應,反應式為:CoO2+Li++e-=LiCoO2 。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】2005年諾貝爾化學獎授予了研究烯烴復分解反應的科學家,以表彰他們作出的卓越貢獻。烯烴復分解反應原理如下:C2H5CH=CHCH3 + CH2=CH2 ![]() C2H5CH=CH2 + CH2=CHCH3,現以烯烴C5H10為原料,合成有機物M和N,合成路線如下:
C2H5CH=CH2 + CH2=CHCH3,現以烯烴C5H10為原料,合成有機物M和N,合成路線如下:

(1)按系統命名法,有機物A的名稱是___________。
(2)B的結構簡式是___________。
(3)C![]() D的反應類型是___________。
D的反應類型是___________。
(4)寫出D![]() M的化學方程式___________。
M的化學方程式___________。
(5)寫出E![]() F合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)___________。
F合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)___________。
(6)已知X的苯環上只有一個取代基,且取代基無甲基,則N的結構簡式為___________。
(7)滿足下列條件的X的同分異構體共有___________種,寫出任意一種的結構簡式___________。
①遇FeCl3溶液顯紫色 ②苯環上的一氯取代物只有兩種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制一定物質的量濃度的KOH溶液時,導致濃度偏低的原因可能是( )
A. 用敞口容器稱量KOH且時間過長
B. 配置前先向容量瓶中加入少量蒸餾水
C. 容量瓶盛過KOH溶液,使用前未洗滌
D. 溶解后快速轉移到容量瓶,然后加足量蒸餾水,定容
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗操作或判斷正確的有![]()
①用10mL量筒準確量取稀硫酸溶液![]() ;
;
②用干燥的pH試紙測定氯水的pH;
③能說明亞硝酸是弱電解質的是:用![]() 溶液作導電試驗,燈泡很暗;
溶液作導電試驗,燈泡很暗;
④使用容量瓶配制溶液時,俯視液面定容后所得溶液的濃度偏大;
⑤將飽和![]() 溶液滴入蒸餾水中即得
溶液滴入蒸餾水中即得![]() 膠體;
膠體;
⑥圓底燒瓶、錐形瓶、蒸發皿加熱時都應墊在石棉網上;
⑦除去鐵粉中混有的少量鋁粉![]() 可加入過量的氫氧化鈉溶液,完全反應后過濾;
可加入過量的氫氧化鈉溶液,完全反應后過濾;
⑧為測定熔融氫氧化鈉的導電性,可在瓷坩堝中熔化氫氧化鈉固體后進行測量;
⑨用食醋除去水壺中的水垢.
A. 3個 B. 4個 C. 5個 D. 6個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F為前四周期原子序數依次增大的六種元素,A、C、D原子均有兩個未成對電子,A、B、C同周期,A與D、B與F分別同主族,E是生活中用量最大的金屬。請回答下列問題:
(1)E比較穩定的離子核外電子排布式_____________________________.
(2)A、B、C的第一電離能由小到大的順序為_________________![]() 用元素符號表示
用元素符號表示![]() 、B、C的簡單氫化物中最易汽化的物質的化學式___________.
、B、C的簡單氫化物中最易汽化的物質的化學式___________.
(3)C與D形成的物質的晶體類型是____________,IT產業中該晶體用于生產____________.
(4)由A、B、C三種元素中的一種或兩種元素形成的分子中,有的互為等電子體,寫出其中一組等電子體的化學式:______![]() 并寫出對應的結構式_______________.
并寫出對應的結構式_______________.
(5)B的單質晶胞與![]() 的相似,則一個晶胞中含B的原子個數為____
的相似,則一個晶胞中含B的原子個數為____![]() 與氫形成的分子空間構型是_______.
與氫形成的分子空間構型是_______.
(6)“砒霜”是一種含C,F的化合物,其分子結構如圖1所示,該化合物的分子式為F4C6,F原子采取______雜化;C,D,E組成的化合物的晶胞如圖2,其晶胞參數為a pm,則其密度為___________________g/cm3(列出式子即可,阿伏伽德羅常數為NAmol-1)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知NH4Cl濃度小于0.1 mol/L時,溶液pH > 5.1現用0.1 mol/L HCl溶液來滴定10 mL 0.05 mol/L氨水,用甲基橙作指示劑,達到終點時所用鹽酸的體積( )
A. = 10 mL B. = 5 mL C. > 5 mL D. < 5 mL
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 羰基庚酸是一種重要的化工中間體,下面合成它的流程圖:
羰基庚酸是一種重要的化工中間體,下面合成它的流程圖:
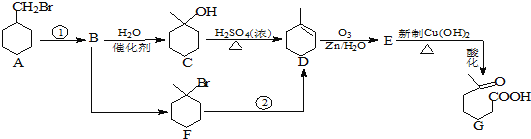
已知:![]()
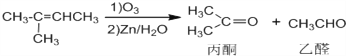
![]()
回答下列問題:
(1)反應![]() 的條件是 _______________ ;1mol化合物C完全燃燒需要消耗O2 ___________ mol
的條件是 _______________ ;1mol化合物C完全燃燒需要消耗O2 ___________ mol
(2)G所含的官能團的名稱是 _____________________ ;
(3)下列說法中正確的是 ______________ :
![]() 與足量的Na反應生成
與足量的Na反應生成![]()
![]() 能被催化氧化成酮
能被催化氧化成酮
![]() 在Ni催化下1molG最多只能與
在Ni催化下1molG最多只能與![]() 加成
加成 ![]() 能發生消去反應生成兩種不同烯烴
能發生消去反應生成兩種不同烯烴
(4)E與新制![]() 的化學方程式為 _________________。
的化學方程式為 _________________。
(5)G的同分異構體有多種,請寫出符合下列要求的同分異構體:___________________________________________________
①結構中含有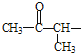 ②屬于酯類 ③能發生銀鏡反應
②屬于酯類 ③能發生銀鏡反應
(6)寫出以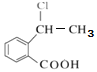 為原料制備
為原料制備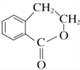 的合成路線流程圖
的合成路線流程圖![]() 無機試劑任用
無機試劑任用![]() ,并注明反應條件。_________________
,并注明反應條件。_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)福州大學王新晨教授以氨基氰(CH2N2)為原料制得類石墨相氮化碳(g-C3N4),其單層結構如圖1。

①氨基氰CH2N2)分子中C、N原子均滿足8電子穩定結構,則該分子的結構式為______;該分子為______(填“極性”或“非極性”)分子。
②氨基氰易溶于水或乙醇,其主要原因是_____________。
③關于g- C3N4的敘述正確的是_________。
A.電負性:C>N B.該物質的熔點比石墨更高
C.該物質屬于原子晶體 D.該物質中C和N原子均采取SP2雜化
(2)NH3與Zn2+可形成[Zn(NH3)6]2+離子,部分結構如圖2。

①NH3的空間構型為_________。
②[Zn(NH3)6]2+離子中存在的化學鍵類型有______;NH3分子中H-N-H鍵角為107.3°,判斷[Zn(NH3)6]2+離子中H-N-H鍵角______107.3°(填">”、"<”或“=”)。
③肼(N2H4)可視為NH3分子中的一個氫原子被-NH2(氨基)取代形成的另一種氮的氫化物。與N2H4互為等電子體的分子有_______。(寫一種)
(3)N元素形成的簡單離子N3-與Xn+形成的晶體的是立方體結構,邊長為anm,如圖3所示。

①Xn+中所有的電子恰好充滿K、L、M三個電子層,則基態X原子的價電子的軌道表示式為________。
②已知該晶體的密度為5.84g·cm-3,則阿伏加德羅常數NA的計算表示式為_____(含a)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷存在于人體所有細胞中,是維持骨骼和牙齒的必要物質,幾乎參與所有生理上的化學反應。磷的化合物在藥物生產和農藥制造等方面用途非常廣泛。請回答下列有關問題:
(1)畫出基態P原子的核外電子排布圖__________。
(2)NH3比PH3易液化的原因是_________。
(3)P4S3可用于制造火柴,其結構如圖1所示。
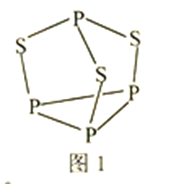
①P4S3中硫原子的雜化軌道類型為________。
②電負性:磷_____硫(填“>”或“<”);第一電離能磷大于硫的原因是________。
(4)NH4BF4是合成氮化硼納米管的原料之一,1molNH4BF4中含有____mol配位鍵。
(5)NF3的鍵角小于NH3的鍵角,其原因是____________。
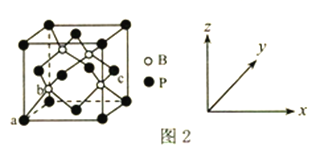
(6)磷化硼是一種超硬耐磨涂層材料,其晶胞結構如圖2所示。原子坐標參數表示晶胞內部各原子的相對位置,圖中a點和c點的原子坐標參數依次為(0,0,0)、(1,![]() ,
,![]() ),則b點的原子坐標參數為________;已知該晶胞中距離最近的兩個磷原子的核間距離為Lpm,則該晶體密度為_____g.cm-3(阿伏加德羅常數用NA表示,列出計算式即可)。
),則b點的原子坐標參數為________;已知該晶胞中距離最近的兩個磷原子的核間距離為Lpm,則該晶體密度為_____g.cm-3(阿伏加德羅常數用NA表示,列出計算式即可)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com