
【題目】下面是石蠟油在熾熱碎瓷片的作用下產生C2H4并檢驗C2H4性質的實驗。請回答下列問題:
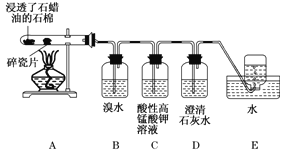
(1)A中碎瓷片的作用是____________。
(2)B裝置中反應的化學方程式為___________。
(3) C裝置中的實驗現象______________ 。
(4) 查閱資料,乙烯與酸性高錳酸鉀溶液反應產生二氧化碳。根據本實驗中裝置________(填裝置字母)中的實驗現象可判斷該資料是否真實。
【答案】催化作用 CH2=CH2+Br2→CH2BrCH2Br 酸性高錳酸鉀溶液褪色 D
【解析】
根據實驗裝置圖,A為石蠟油在熾熱碎瓷片作催化劑的作用下生成乙烯,乙烯通過溴水,與溴發生加成反應,使溴水褪色,乙烯通過高錳酸鉀溶液,被高錳酸鉀氧化成二氧化碳,使高錳酸鉀褪色,生成的二氧化碳能使澄清石灰水變渾,最后用排水集氣法收集反應剩余的氣體,據此分析作答。
(1)石蠟油在熾熱碎瓷片的作用下產生乙烯,可知碎瓷片的作用主要是催化劑,加快反應速率,故答案為:催化作用;
(2)乙烯能夠與溴發生加成反應生成1,2-二溴乙烷,溴水褪色,反應的方程式為CH2=CH2+Br2→CH2BrCH2Br,故答案為:CH2=CH2+Br2→CH2BrCH2Br;
(3)乙烯可與高錳酸鉀發生氧化還原反應而使高錳酸鉀溶液褪色,故答案為:酸性高錳酸鉀溶液褪色;
(4)乙烯與酸性高錳酸鉀溶液反應產生二氧化碳,能使澄清石灰水變渾,D中澄清石灰水如果變渾濁,說明生成二氧化碳,所以根據D中的實驗現象可判斷該資料是否真實,故答案為:D。


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:
【題目】Na2S2O4俗稱保險粉,常用做紡織工業的漂白劑、脫色劑等。某科研小組制備并探究其性質。
資料:Na2S2O4易溶于水,具有極強的還原性,易被空氣氧化,在堿性介質中穩定。
Ⅰ.制備Na2S2O4(加熱等輔助儀器略去)

(1)儀器①的名稱是______。
(2)B裝置用于制備Na2S2O4。第一步反應:Zn+2SO2 ![]() ZnS2O4;第二步,加入NaOH溶液,于28~35℃下反應生成Na2S2O4,該步反應的化學方程式為______。
ZnS2O4;第二步,加入NaOH溶液,于28~35℃下反應生成Na2S2O4,該步反應的化學方程式為______。
(3)B裝置反應前,先進行的實驗操作是______。
(4)反應后除去B中的沉淀,在濾液中加入一定量的NaCl固體攪拌,有Na2S2O4晶體析出。加入NaCl固體的作用是______。
Ⅱ.探究Na2S2O4的性質
(5)隔絕空氣加熱Na2S2O4固體完全分解得到固體產物Na2SO3、Na2S2O3和SO2,但科研小組沒有做到完全隔絕空氣,得到的固體產物中還含有Na2SO4。請設計實驗證明該分解產物中含有Na2SO4。實驗方案是______。(可選試劑:稀鹽酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液、KMnO4溶液)
(6)制備納米級銀粉:用NaOH溶液溶解Na2S2O4,加入一定量的AgNO3溶液,生成納米級的銀粉。在制備銀粉的反應中,氧化劑和還原劑的物質的量之比為2︰1,且生成的含硫物質只有一種,寫出該反應的離子方程式______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在其他條件相同時,反應N2+02=2NO分別在有、無催化劑時的能量變化如下圖所示,下列說法中不正確的是( )

A. 該反應中反應物的總能量比生成物的總能量低
B. 加入催化劑能改變反應的焓變
C. 加入催化劑可以改變反應的活化能
D. 0.2 mol NO完全分解成N2和02時共放出熱量18.26 kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣凈化中的一個反應如下:NO(g)+CO(g)![]() 1/2N2(g)+CO2(g) ΔH=-373.4 kJ·mol-1,在恒容的密閉容器中,反應達到平衡后,改變某一條件,下列示意圖正確的是
1/2N2(g)+CO2(g) ΔH=-373.4 kJ·mol-1,在恒容的密閉容器中,反應達到平衡后,改變某一條件,下列示意圖正確的是
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某反應由兩步反應A![]() B
B![]() C構成,反應過程中的能量變化曲線如圖(E1、E3表示兩反應的活化能)。下列有關敘述正確的是( )
C構成,反應過程中的能量變化曲線如圖(E1、E3表示兩反應的活化能)。下列有關敘述正確的是( )

![]()
A. 兩步反應均為吸熱反應 B. 三種化合物的穩定性順序:B﹤A﹤C
C. 加入催化劑不改變反應的焓變,但能提高轉化率 D. 整個反應的ΔH=E1-E2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖是鋅片和銅片同時插入稀硫酸中所組成的原電池裝置,c、d為兩個電極。則下列有關的判斷不正確的是( )

A、d為負極,發生氧化反應
B、c為鋅片,電池工作時,溶液中SO42-向c移動
C、電池工作的過程中,d電極上產生大量的氣泡
D、電池工作的過程中,溶液中SO42-濃度基本不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,可逆反應N2+3H2![]() 2NH3 △H<0達到平衡后,只改變一個條件,下列敘述錯誤的是
2NH3 △H<0達到平衡后,只改變一個條件,下列敘述錯誤的是
A. 加催化劑,v正、v逆都發生變化,且變化的倍數相等
B. 加壓,v正、v逆都增大,且v正增大的倍數大于v逆增大的倍數
C. 增大氮氣的濃度,N2的平衡轉化率減小,H2的平衡轉化率增大
D. 降溫,v正、v逆都減小,且v正減小的倍數大于v逆減小的倍數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在下圖銀鋅原電池中,以硫酸銅為電解質溶液。

(1)鋅為______極,該電極上發生的是_____________反應(“氧化”或“還原”),電極反應式為__________________________________。
(2)銀為____極,電極上發生的是_______反應(“氧化”或“還原”),電極反應式是__________________,銀片上觀察到的現象是__________________________。
(3)該原電池的總反應式是______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(I)某溫度下,氣體X和Y在體積為2L的密閉容器中反應,生成氣體Z。經測定各物質的物質的量隨時間變化如下圖所示,經10s達到化學平衡狀態,請回答下列問題。
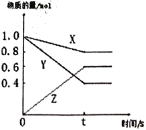
(1)寫出該反應的化學反應方程式____________________________________。
(2)該溫度下此反應的平衡常數______________________。
(Ⅱ).已知可逆反應:M(g)+N(g)![]() P(g)+Q(g) ΔH>0請回答下列問題:
P(g)+Q(g) ΔH>0請回答下列問題:
(3)在某溫度下,反應物的起始濃度分別為:c(M)= 1 mol·L-1,c(N)=2.4 mol·L-1;達到平衡后,M的轉化率為60%,此時N的轉化率為___________;
(4)若反應溫度升高,M的轉化率_______(填“增大”“減小”或“不變”) ;
(5)若反應溫度不變,反應物的起始濃度分別為:c(M)= 4 mol·L-1,c(N)=a mol·L-1;達到平衡后,c(P)=2 mol·L-1,a=_________;
(6)若反應溫度不變,反應物的起始濃度為:c(M)=c(N)=b mol·L-1,達到平衡后,M的轉化率為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com