
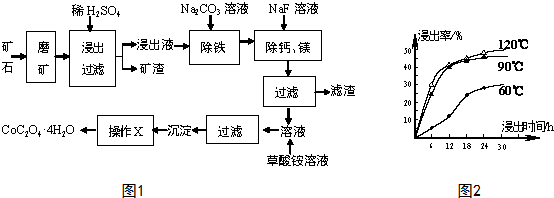
分析 水鈷礦磨礦將礦石粉碎,增大接觸面積,加快反應速率,加入稀硫酸,礦渣為SiO2,濾液中含有:CoSO4、Fe2(SO4)3、MgSO4、CaSO4,加入碳酸鈉,除去Fe2(SO4)3,加入氟化鈉,除去鈣鎂,過濾得主要含CoSO4的溶液,加入草酸銨,通過沉淀、過濾、洗滌、干燥得到四水合草酸鈷,
(1)根據浸出率與時間和溫度的關系及生產成本分析;
(2)根據原子守恒配平方程式;
(3)$\frac{c(Ca{\;}^{2+})}{c(Mg{\;}^{2+})}$=$\frac{Ksp(CaF{\;}_{2})}{Ksp(MgF{\;}_{2})}$;
(4)根據流程圖中加入的物質分析,該沉淀中吸附易溶于水的離子;得到的沉淀要進行洗滌和干燥,才能得到較純凈、干燥的物質;
(5)放電時,該電池是原電池,正極上得電子發生還原反應,依據負極電極材料和題干信息分析計算.
解答 解:(1)根據圖知,時間越長浸出率越高,溫度越高,浸出率越高,但浸出12小時后,浸出率變化不大,90℃和120℃浸出率變化不大,且時間過長、溫度過高導致成本較大,所以最佳的浸出時間為12小時,最佳的浸出溫度為90℃,
故答案為:12;90;
(2)根據原子守恒配平方程式,所以其方程式為:3Fe2(SO4)3+6H2O+6Na2CO3=Na2Fe6 (SO4)4(OH)12↓+5Na2SO4+6CO2↑,
故答案為:3,6,6,1,5,6;
(3)$\frac{c(Ca{\;}^{2+})}{c(Mg{\;}^{2+})}$=$\frac{Ksp(CaF{\;}_{2})}{Ksp(MgF{\;}_{2})}$=$\frac{1.1×10{\;}^{-10}}{7.40×10{\;}^{-11}}$=1.5,
故答案為:1.5;
(4)該沉淀中吸附易溶于水的離子,根據流程圖知,溶液中含有SO42-、NH4+、Na+、F-,所以沉淀上含有SO42-、NH4+、Na+、F-,得到的沉淀要進行洗滌和干燥才能得到較純凈、干燥的物質,
故答案為:SO42-、NH4+、Na+、F-;洗滌、干燥;
(5)放電時,該電池是原電池,正極上得電子發生還原反應,電極反應式為:CoO2+Li++e-=LiCoO2,充電時,Li+還原為Li,并以原子形式嵌入電池負極材料碳-6(C6)中,所以負極為LiC6中Li的化合價為0價,若放電時有1mol e-轉移,CoO2+Li++e-=LiCoO2,正極質量增加為1molLi+的質量=1mol×7g/mol=7g;
故答案為:0;7.
點評 本題考查難溶電解質的溶解平衡、電極反應式的書寫、物質的分離和提純等知識點,難點是(3)題,明確溶度積常數的含義是解此題關鍵,電極反應式的書寫是學習難點,要結合電解質溶液的酸堿性書寫,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | c(Al3+)=0.1mol/L的溶液中:Na+、K+、HS-、SO42- | |
| B. | 使酚酞呈紅色的溶液中:K+、Ba2+、I-、NO3- | |
| C. | 由水電離出的c(H+)=10-13mol/L的溶液中:Na+、HCO3-、Cl-、Br- | |
| D. | 加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ① | B. | ①② | C. | ①③ | D. | ①③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
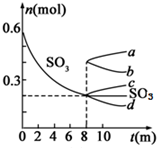 利用催化氧化反應將SO2轉化為SO3是工業上生產硫酸的關鍵步驟.T1℃時,在1L密閉容器中充入0.6molSO3,如圖表示SO3物質的量隨時間的變化曲線.
利用催化氧化反應將SO2轉化為SO3是工業上生產硫酸的關鍵步驟.T1℃時,在1L密閉容器中充入0.6molSO3,如圖表示SO3物質的量隨時間的變化曲線.| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -488.3 kJ/mol | B. | -244.15 kJ/mol | C. | 488.3 kJ/mol | D. | 244.15 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將SO2通入Ba(NO3)2溶液中能生成BaSO4沉淀 | |
| B. | 在Si02+3C$\frac{\underline{\;高溫\;}}{\;}$SiC+2C0的反應中,Si02是氧化劑 | |
| C. | 生鐵在潮濕的空氣中主要發生析氫腐蝕 | |
| D. | 某鉀鹽溶于鹽酸,產生能使澄清石灰水變渾濁的無色氣體,說明該鉀鹽是K2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
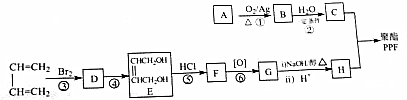

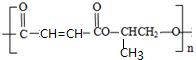 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com