
| A. | 需要加熱才能發生的反應一定是吸熱反應 | |
| B. | 任何放熱反應在常溫條件下一定能發生 | |
| C. | 反應物和生成物所具有的總能量決定了化學反應是放熱還是吸熱 | |
| D. | 一個反應的反應熱等于反應物的總能量減去生成物的總能量 |
分析 化學反應中的能量變化,通常表現為熱量的變化.如果反應物所具有的總能量高于生成的總能量,則在反應中會有一部分能量轉變為熱能的形式釋放,這就是放熱反應,反之則是吸熱反應,并注意反應條件與反應吸熱、放熱無關,以此解答.
解答 解:A.需要加熱才能發生的反應可能是放熱反應,也可能為吸熱反應,加熱只是反應的條件,如鋁熱反應為放熱反應,但在加熱條件下才能進行,故A錯誤;
B.鋁熱反應在高溫下才能進行,故B錯誤;
C.從能量守恒的角度分析,如反應物總能量大于生成物總能量,則為放熱反應,反之為吸熱反應,故C正確;
D.一個反應的反應熱等于生成物的總能量減去反應物的總能量,故D錯誤.
故選C.
點評 本題主要考查了化學反應中能量變化的原因,需要強調的是反應是吸熱反應還是放熱反應與反應的條件無關,為易錯點,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 建立廢舊電池回收站,對其進行回收再利用 | |
| B. | 將木材邊角料制成木屑顆粒,用作環保能源 | |
| C. | 露天焚燒農作物秸稈還田,用作農作物肥料 | |
| D. | 部分煤炭轉直接開采為先在地下氣化或液化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗標號 | 初始濃度/mol•L-1 | 生成N2的初速率/mol•L-1•s-1 | |
| c(NO) | c(H2) | ||
| 1 | 6.00×10-3 | 1.00×10-3 | 3.19×10-3 |
| 2 | 6.00×10-3 | 2.00×10-3 | 6.38×10-3 |
| 3 | 6.00×10-3 | 3.00×10-3 | 9.57×10-3 |
| 4 | 1.00×10-3 | 6.00×10-3 | 0.48×10-3 |
| 5 | 2.00×10-3 | 6.00×10-3 | 1.92×10-3 |
| 6 | 3.00×10-3 | 6.00×10-3 | 4.32×10-3 |
| A. | 增大c(H2),生成N2的初速率增大 | B. | 減小c(NO),生成N2的初速率減小 | ||
| C. | 生成N2的初速率與c(H2)成正比 | D. | 生成N2的初速率與c(NO)成正比 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
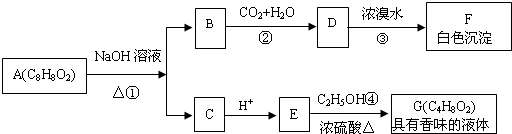
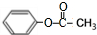 .
.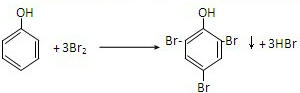 ,該反應的反應類型是取代反應.
,該反應的反應類型是取代反應. CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.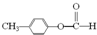 .
.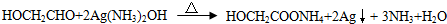 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 在化學課上,圍繞濃硫酸的化學性質進行了如下實驗探究:將適量的蔗糖放入燒杯中,加入幾滴水,攪拌均勻.然后加入適量濃硫酸,迅速攪拌,放出大量的熱,同時觀察到蔗糖逐漸變黑,體積膨脹,并放出有刺激性氣味的氣體.請回答:
在化學課上,圍繞濃硫酸的化學性質進行了如下實驗探究:將適量的蔗糖放入燒杯中,加入幾滴水,攪拌均勻.然后加入適量濃硫酸,迅速攪拌,放出大量的熱,同時觀察到蔗糖逐漸變黑,體積膨脹,并放出有刺激性氣味的氣體.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 燃煤脫硫,防止酸雨 | |
| B. | 使用無磷洗衣粉,防止水體污染 | |
| C. | 提倡使用含鉛汽油,提高汽油的抗爆性 | |
| D. | 為燃料提供適當過量的空氣,使燃料充分燃燒 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鋇溶液與硫酸銅溶液反應的離子方程式為Ba2++SO42-═BaSO4↓ | |
| B. | 氫氣的燃燒熱為285.8KJ/mol,所以表示氫氣燃燒熱的熱化學方程式為2H2(g)+O2(g)═2H2O(l)△H≈-571.6KJ/mol | |
| C. | 原子序數為1和8的兩種元素形成的18電子的化合物的電子式為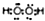 | |
| D. | 銅鋅原電池的正極反應式一定為2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
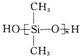 是由二甲基二氯硅烷
是由二甲基二氯硅烷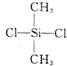 經兩種反應而制得的,這兩種反應依次是( )
經兩種反應而制得的,這兩種反應依次是( )| A. | 消去反應、加聚反應 | B. | 水解反應、縮聚反應 | ||
| C. | 氧化反應、縮聚反應 | D. | 取代反應、加聚反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2與O3互為同位素 | |
| B. | ${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O互為同素異形體 | |
| C. | 麥芽糖與蔗糖互為同分異構體 | |
| D. | CH3-CH2-CH2-CH3與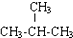 互為同系物 互為同系物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com