
| A、方程式中x=2 |
| B、達平衡后,容器內壓強是反應起始時的2倍 |
| C、向容器中再充入3.0 mol M和2.5 mol N,達新平衡時Q的體積分數減小 |
| D、容器內混合氣體的密度不再變化和平均相對分子質量不再變化均可作為達到平衡狀態的標志 |


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:
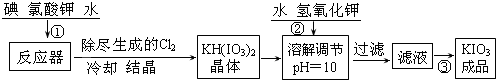
查看答案和解析>>
科目:高中化學 來源: 題型:
| W | 單質是淡黃色固體 | ||
| X | 在地殼中的含量居第二位 | ||
| Y | 原子最外層電子數是電子總數的
| ||
| Z | 第三周期原子半徑最小的金屬 |
| A、氣態氫化物的熱穩定性:X<W |
| B、最高價氧化物對應水化物的酸性:Y>X |
| C、離子半徑:Z>W |
| D、Y的氧化物中含有非極性共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:
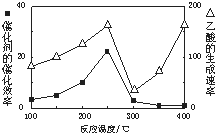 CH4和CO2反應可以制造價值更高的化學產品.
CH4和CO2反應可以制造價值更高的化學產品.| 物 質 | CH4 | CO2 | CO | H2 |
| 平衡濃度(mol?L-1) | 0.5 | 0.5 | 2.0 | 2.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| 氫氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 開始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、該反應的焓變為正值 | ||||
| B、恒溫恒容下,增大壓強,H2濃度一定減小催化劑高溫 | ||||
| C、升高溫度,逆反應速率減小 | ||||
D、該反應的化學方程式為CO+H2O
|
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1 | B、2 | C、13 | D、14 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com