
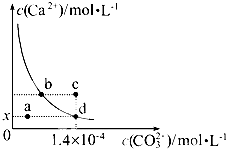
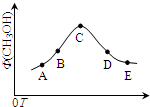
 室溫時,CaCO3在水中的溶解平衡曲線如圖所示,已知:25℃其溶度積為2.8×10-9,下列說法不正確的是( )
室溫時,CaCO3在水中的溶解平衡曲線如圖所示,已知:25℃其溶度積為2.8×10-9,下列說法不正確的是( )| A、加入蒸餾水可使溶液由d點變到a點 |
| B、c點時有碳酸鈣沉淀生成 |
| C、x數值為2×10-5 |
| D、b點與d點對應的溶度積相等 |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、①>②>④>③>⑤ |
| B、③>①>④>②>⑤ |
| C、⑤>③>②>①>④ |
| D、③>④>⑤>②>① |
查看答案和解析>>
科目:高中化學 來源: 題型:
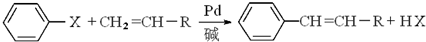 (X為鹵原子,R為取代基)
(X為鹵原子,R為取代基)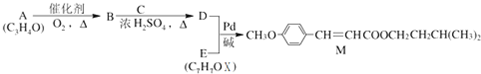
查看答案和解析>>
科目:高中化學 來源: 題型:
| 組別 | 藥品1 | 藥品2 | 實驗現象 |
| Ⅰ | 0.1mol/LNaOH溶液 | 0.1mol/LMgCl2溶液 | 生成白色沉淀 |
| Ⅱ | 0.1mol/L氨水 | 0.1mol/LMgCl2溶液 | 無現象 |
| Ⅲ | 1mol/L氨水 | 1mol/LMgCl2溶液 | 現象Ⅲ |
| Ⅳ | 1mol/L氨水 | 0.1mol/LMgCl2溶液 | 生成白色沉淀 |
| Ⅴ | 0.1mol/L氨水 | 1mol/LMgCl2溶液 | 無現象 |
| A、實驗Ⅱ、Ⅴ無現象,而Ⅳ生成白色沉淀,說明增大c(Mg2+)不能向生成沉淀的方向移動,增大氨水溶液的濃度才能向生成沉淀的方向移動 |
| B、實驗Ⅲ無現象,因為氯化鎂溶液和氨水濃度都增大,則導致氯化銨濃度增大,而氫氧化鎂可以溶解在氯化銨溶液中 |
| C、由于氫氧化鎂可以溶解在氯化銨溶液中,而氯化鎂溶液和氨水反應可以生成氯化銨,所以該兩種溶液混合后可能會出現先生成沉淀后溶解的現象 |
| D、實驗Ⅲ的現象是生成白色沉淀,因為增大兩種溶液中任意一種的濃度,都能使混合液的離子積達到氫氧化鎂的Ksp |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 選項 | 陳述Ⅰ | 陳述Ⅱ | 陳述Ⅲ |
| A | 加壓有利于提高SO2的轉化率 | 工業生產硫酸常在高溫下進行 | Ⅰ對,Ⅱ對;有 |
| B | Cl2和SO2混合后可用來漂白紙漿 | Cl2和SO2都有較好的漂白作用 | Ⅰ對,Ⅱ錯;無 |
| C | 工業生產硫酸用水吸收SO3 | SO3可與水反應 | Ⅰ對,Ⅱ對;有 |
| D | 石墨常用作電解池的電極 | 石墨的化學性質穩定且導電性好 | Ⅰ對,Ⅱ對;有 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
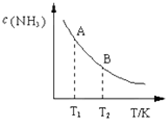 氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產.生活中有著重要作用.請回答下列問題:
氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產.生活中有著重要作用.請回答下列問題:| 一定條件 |
| 時間/min 濃度/mol?L-1 | c (N2) | c (H2) | c (NH3) |
| 0 | 0.6 | 1.8 | 0 |
| 3 | 0.52 | x | 0.16 |
| 6 | 0.36 | 1.08 | 0.48 |
| 9 | 0.36 | 1.08 | 0.48 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 火力發電廠釋放出的大量氧化物(NOx)、SO2、CO2會對環境造成污染.對這些廢氣進行脫硝、脫碳和脫硫處理,可達到節能減排、廢物利用等目的.
火力發電廠釋放出的大量氧化物(NOx)、SO2、CO2會對環境造成污染.對這些廢氣進行脫硝、脫碳和脫硫處理,可達到節能減排、廢物利用等目的.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com