
| A. | 0.533L | B. | 0.267L | C. | 4.0L | D. | 2.0L |
分析 根據(jù)MgCl2和AlCl3的混合溶液與氫氧化鈉溶液的反應可知,要使Mg2+全部轉化為沉淀分離出來,Al3+應恰好轉化為AlO2-,反應后溶液為NaCl、NaAlO2的混合液,由鈉離子守恒可知:n(NaOH)=n(NaCl)+n(NaAlO2),再根據(jù)氯離子、Al元素守恒可計算n(NaOH),進而計算氫氧化鈉溶液體積.
解答 解:將200mL MgCl2,AlCl3的混合溶液中的Mg2+轉化為Mg(OH)2沉淀并分離析出,Al3+應恰好轉化為AlO2-,反應后溶液為NaCl、NaAlO2的混合液,
溶液中n(Cl-)=0.2L×2mol/L×2+0.2L×3mol/L×3=2.6mol,
溶液中n(AlO2-)=n(Al3+)=0.2L×3mol/L=0.6mol,
由鈉離子守恒可知:n(NaOH)=n(NaCl)+n(NaAlO2)=n(Cl-)+n(AlO2-)=2.6mol+0.6mol=3.2mol,
所以至少需要0.8mol/L氫氧化鈉溶液的體積為$\frac{3.2mol}{0.8mol/L}$=4L,
故選:C.
點評 本題考查混合物的有關計算,側重于學生的分析能力和計算能力的考查,難度中等,注意根據(jù)守恒法計算.


科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ①③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
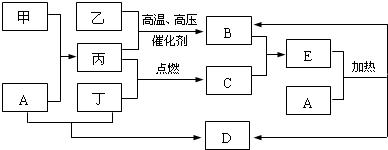
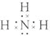 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在地殼中的含量:Al>Fe>Na | |
| B. | 均能與鹽酸反應,生成物中金屬價態(tài)數(shù)值:Al>Fe>Na | |
| C. | 鈉、鋁均能從FeCl3溶液中置換出鐵 | |
| D. | 少量金屬鈉保存在煤油里 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
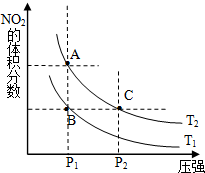 (1)對反應N2O4(g)═2NO2(g)△H>0,在溫度為T1、T2時,平衡體系中NO2的體積分數(shù)隨壓強變化曲線如圖所示.T1<T2(填“>”、“<”或“=”);A、C兩點的速率VA<VC(同上).
(1)對反應N2O4(g)═2NO2(g)△H>0,在溫度為T1、T2時,平衡體系中NO2的體積分數(shù)隨壓強變化曲線如圖所示.T1<T2(填“>”、“<”或“=”);A、C兩點的速率VA<VC(同上).| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 次氯酸電子式 | B. | 核內有8個中子的碳原子${\;}_{6}^{8}$C | ||
| C. | CO2的比例模型 | D. | 純堿的化學式Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
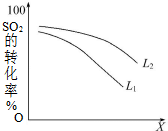 一定溫度下,在2L密閉容器中發(fā)生反應:2SO2(g)+O2(g)?2SO3(g)△H=-196kJ•mol-1
一定溫度下,在2L密閉容器中發(fā)生反應:2SO2(g)+O2(g)?2SO3(g)△H=-196kJ•mol-1查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com