
已知工業(yè)制氫氣的反應(yīng)為CO(g) + H2O(g)  CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2 L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。
CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2 L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。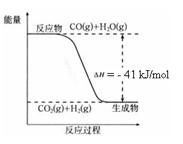
(1)增加H2O(g)的濃度,CO的轉(zhuǎn)化率將 (填“增大”“減小”或“不變”)。
(2)平衡常數(shù)的表達(dá)式K = 。400 ℃時的平衡常數(shù)K 9(填“>”“<”或”“=”)。
(3)500 ℃時,10 min內(nèi)v(H2O)= ,在此過程中體系的能量將 (填“增加”或“減少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol
結(jié)合上圖寫出CO完全燃燒生成CO2的熱化學(xué)方程式: 。
科目:高中化學(xué) 來源: 題型:
已知工業(yè)制氫氣的反應(yīng)為CO(g) + H2O(g) ![]() CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2 L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。
CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2 L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。
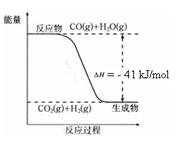
(1)增加H2O(g)的濃度,CO的轉(zhuǎn)化率將 (填“增大”“減小”或“不變”)。
(2)平衡常數(shù)的表達(dá)式K = 。400 ℃時的平衡常數(shù)K 9(填“>”“<”或”“=”)。
(3)500 ℃時,10 min內(nèi)v(H2O)= ,在此過程中體系的能量將 (填“增加”或“減少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol
結(jié)合上圖寫出CO完全燃燒生成CO2的熱化學(xué)方程式: 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
已知工業(yè)制氫氣的反應(yīng)為CO(g) + H2O(g) CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。
(1)增加H2O(g)的濃度,CO的轉(zhuǎn)化率將 (填“增大”“減小”或“不變”)。
(2)平衡常數(shù)的表達(dá)式K = 。400 ℃時的平衡常數(shù)K 9(填“>”“<”或”“=”)。
(3)500 ℃時,10min內(nèi)v(H2O)= ,在此過程中體系的能量將 (填“增加”或“減少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O(g) ΔH=-484kJ/mol
結(jié)合上圖寫出CO完全燃燒生成CO2的熱化學(xué)方程式: 。
查看答案和解析>>
科目:高中化學(xué) 來源:2010-2011學(xué)年北京市朝陽區(qū)高三第一學(xué)期期末考試化學(xué)試卷 題型:填空題
已知工業(yè)制氫氣的反應(yīng)為CO(g) + H2O(g)  CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2
L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。
CO2(g) + H2(g),反應(yīng)過程中能量變化如右圖所示。在500 ℃時的平衡常數(shù) K = 9。若在2
L的密閉容器中CO和水蒸氣的起始濃度都是0.1 mol/L,10 min時達(dá)到平衡狀態(tài)。
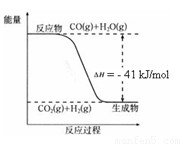
(1)增加H2O(g)的濃度,CO的轉(zhuǎn)化率將 (填“增大”“減小”或“不變”)。
(2)平衡常數(shù)的表達(dá)式K = 。400 ℃時的平衡常數(shù)K 9(填“>”“<”或”“=”)。
(3)500 ℃時,10 min內(nèi)v(H2O)= ,在此過程中體系的能量將 (填“增加”或“減少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol
結(jié)合上圖寫出CO完全燃燒生成CO2的熱化學(xué)方程式: 。
查看答案和解析>>
科目:高中化學(xué) 來源:北京期末題 題型:填空題
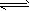 CO2(g)+H2(g),反應(yīng)過程中能量變化如圖所示。在500 ℃時的平衡常數(shù)K=9。若在2L的密閉容器中CO和水蒸氣的起始濃度都是0.1mol/L,10min時達(dá)到平衡狀態(tài)。
CO2(g)+H2(g),反應(yīng)過程中能量變化如圖所示。在500 ℃時的平衡常數(shù)K=9。若在2L的密閉容器中CO和水蒸氣的起始濃度都是0.1mol/L,10min時達(dá)到平衡狀態(tài)。 
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com