
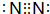 .
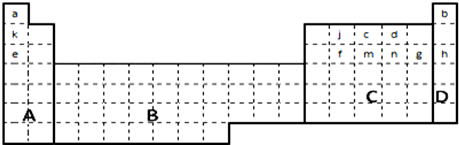
. 分析 由元素在周期表中位置,可知a為H、b為He、k為Li、j為C、c為N、d為O、e為Na、f為Si、m為P、n為S、g為Cl、h為Ar.
(1)元素周期表中全部是金屬元素的是過渡元素區(qū)域;
(2)現(xiàn)有甲、乙兩種短周期元素,室溫下,甲元素單質在冷的濃硫酸或濃硝酸中,表面都生成致密的氧化膜,則甲為Al,乙元素原子核外M電子層與K電子層上的電子數(shù)相等,M層電子數(shù)為2,故乙為Mg;
(3)①同周期自左而右非金屬性增強、同主族自上而下非金屬性減弱;
②離子電荷越小、離子半徑越大,金屬鍵越弱,金屬晶體熔點越低;
③元素的非金屬性越強,對應氫化物越穩(wěn)定;
④電子層結構相同的離子,核電荷數(shù)越大離子半徑越小,離子電子層越多,離子半徑越大;
⑤工業(yè)上用焦炭與二氧化硅反應制備Si,反應還生成CO;
⑥C的單質為N2,分子中N原子之間形成3對共用電子對.
解答 解:由元素在周期表中位置,可知a為H、b為He、k為Li、j為C、c為N、d為O、e為Na、f為Si、m為P、n為S、g為Cl、h為Ar.
(1)A區(qū)中含有H元素,C區(qū)中含有金屬、非金屬,D炔區(qū)為稀有氣體,元素周期表中全部是金屬元素的是過渡元素區(qū)域,即為B區(qū)域,故答案為:B;
(2)現(xiàn)有甲、乙兩種短周期元素,室溫下,甲元素單質在冷的濃硫酸或濃硝酸中,表面都生成致密的氧化膜,則甲為Al,乙元素原子核外M電子層與K電子層上的電子數(shù)相等,M層電子數(shù)為2,故乙為Mg,
①甲元素在元素周期表中位置:第三周期ⅢA族,故答案為:第三周期ⅢA族;
②同周期自左而右元素金屬性減弱,故金屬性Mg>Al,
A.在空氣中放置已久的這兩種元素的塊狀單質表面均得到氧化鎂,氧化鋁、氧化鎂不溶于水,會阻止金屬與熱水的反應,故A錯誤;
B.金屬單質與酸反應越劇烈,該金屬元素的金屬性越強,故B正確;
C.金屬鎂和熱水反應,得到氫氧化鎂顯弱堿性,而金屬鋁和熱水不反應,可以確定金屬性的強弱,故C正確;
D.均為金屬氫化物,不能利用氣態(tài)氫化物穩(wěn)定性比較金屬性強弱,可以比較非金屬性強弱,故D錯誤.
故選:Mg;BC;
③甲的氧化物為Al2O3,e的最高價氧化物對應的水化物為NaOH,二者反應的離子方程式為:,
故答案為:Al2O3+2OH-═2AlO2-+H2O;
(3)①同周期自左而右非金屬性增強、同主族自上而下非金屬性減弱,故非金屬性N>C>Si,故答案為:N;
②Na、Mg、Al晶體中,Na+離子所帶電荷最小、離子半徑最大,金屬鍵最弱,故Na晶體熔點最低,故答案為:Na;
③非金屬性Cl>S>P>Si,元素的非金屬性越強,對應氫化物越穩(wěn)定,故HCl最穩(wěn)定,故答案為:GCl;
④電子層結構相同的離子,核電荷數(shù)越大離子半徑越小,離子電子層越多,離子半徑越大,故離子半徑為:Al3+<Mg2+<Na+<O2-<N3-,故答案為:Al3+<Mg2+<Na+<O2-<N3-;
⑤工業(yè)上用焦炭與二氧化硅反應制備Si,反應還生成CO,反應方程式為:SiO2+2C$\frac{\underline{\;高溫\;}}{\;}$2CO+Si,故答案為:SiO2+2C$\frac{\underline{\;高溫\;}}{\;}$2CO+Si;
⑥C的單質為N2,分子中N原子之間形成3對共用電子對,電子式為: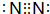 ,故答案為:
,故答案為: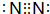 .
.
點評 本題考查元素周期表與元素周期律綜合應用,比較基礎,注意對元素周期律的理解掌握,注意掌握元素金屬性、非金屬性強弱比較及實驗事實.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 一定條件下,將1molN2和3molH2混合,充分反應后轉移的電子數(shù)為NA | |
| B. | 1.5molNO2與足量水反應,轉移的電子數(shù)為1.5NA | |
| C. | 6.4g由S2、S4、S8組成的混合物含硫原子數(shù)為0.2NA | |
| D. | 常溫常壓下,11.2LCl2含氯原子數(shù)為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 3種 | C. | 4種 | D. | 5種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
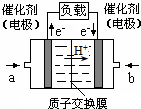 可給筆記本電腦供電的甲醇燃料電池已經(jīng)面世,其結構示意圖如下.甲醇在催化劑作用下提供質子(H+)和電子.電子經(jīng)外電路、質子經(jīng)內電路到達另一極與氧氣反應.該電池總反應式為:2CH3OH+3O2═2CO2+4H2O.下列說法中正確的是( )
可給筆記本電腦供電的甲醇燃料電池已經(jīng)面世,其結構示意圖如下.甲醇在催化劑作用下提供質子(H+)和電子.電子經(jīng)外電路、質子經(jīng)內電路到達另一極與氧氣反應.該電池總反應式為:2CH3OH+3O2═2CO2+4H2O.下列說法中正確的是( )| A. | 右邊的電極為電池的負極,b處通入的是空氣 | |
| B. | 左邊的電極為電池的負極,a處通入的是甲醇 | |
| C. | 電池負極的反應式為:CH3OH+H2O═CO2+6H++4e- | |
| D. | 電池正極的反應式為:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水的離子積常數(shù)KW隨著溫度的升高而增大,說明水的電離過程是吸熱的 | |
| B. | 弱電解質溶液稀釋后,溶液中各種離子濃度一定都減小 | |
| C. | 某鹽的水溶液呈酸性,該鹽一定是強酸弱堿鹽 | |
| D. | 中和相同體積相同pH的鹽酸和醋酸溶液所需NaOH的物質的量相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 據(jù)Ksp(AgCl)=1.77×10-10,Ksp(Ag2CrO4)=2.0×10-12,可推知AgCl溶解度比Ag2CrO4的溶解度大 | |
| B. | 0.1mol/L的ZnCl2溶液中通入足量硫化氫最終得不到ZnS沉淀是因為c(Zn2+)•c(S2-)<Ksp(ZnS) | |
| C. | 向碳酸鋇沉淀中加入稀硫酸,沉淀發(fā)生轉化,可推知硫酸鋇的Ksp比碳酸鋇的大 | |
| D. | AgCl在10 mL 0.1 mol/L的KCl中溶解的質量比在10 mL 0.05 mol/L的AgNO3溶液中少 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{53}^{131}$I與${\;}_{53}^{125}$I 互為同位素 | |
| B. | ${\;}_{53}^{131}$I與${\;}_{53}^{125}$I性質完全相同 | |
| C. | ${\;}_{94}^{224}$Pu位于周期表中第六周期 | |
| D. | ${\;}_{53}^{131}$I的質子數(shù)為78 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com