
某燃料電池以熔融的K2CO3為電解質,以丁烷為燃料,以空氣為氧化劑,以具有催化作用和導電性能的稀土金屬材料為電極。下列敘述錯誤的是( )
A. 該燃料電池的化學反應方程式為
2C4H10+13O2![]() 8CO2+10H2O
8CO2+10H2O
B. 該燃料電池的負極反應式為
2C4H10+26CO![]() -52e-══34CO2+10H2O
-52e-══34CO2+10H2O
C. 該燃料電極的正極反應式為
26CO2+13O2+52e-══26CO![]()
D. 向正極通入的氣體成分主要為N2和O2
 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:閱讀理解

 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+| CO | 2- 3 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
濃度/mol?L-1 / 時間/min |
NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
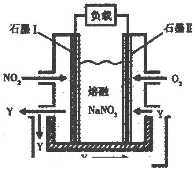
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| n |
| 3 |
| n |
| 3 |
| V/s | 0 | 50 | 100 |
| c(N2O3)/mol?L-1 | 5.00 | 3.52 | 2.48 |
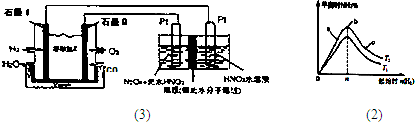
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如圖所示.
CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如圖所示.
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 催化劑 |
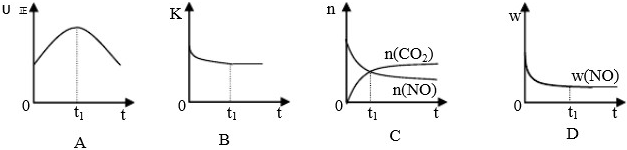
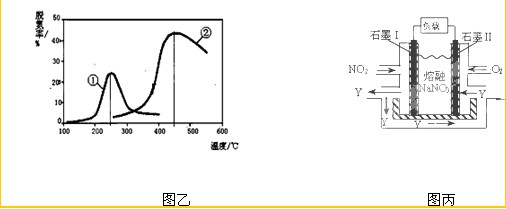
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com