
分析 發生反應:Cl2 +2NaBr=2NaCl+Br2,根據固體質量差利用差量法計算NaBr的質量,進而計算原混合物中NaCl質量,再計算原混合物中NaCl物質的量,最后根據物質的量濃度定義式計算.
解答 解:設混合物中NaBr的質量為m,則:
Cl2 +2NaBr=2NaCl+Br2 固體質量減小△m
206 160-71=89
m 22g-17.55g=4.45g
所以m=$\frac{4.45g×206}{89}$=10.3g
則混合物中NaCl質量為22g-10.3g=11.7g,其物質的量為$\frac{11.7g}{58.5g/mol}$=0.2mol,
則原混合物溶于水,配成100mL溶液,所得溶液中NaCl的物質的量濃度為$\frac{0.2mol}{0.1L}$=2mol/L,
答:原混合物所得溶液中NaCl的物質的量濃度為2mol/L.
點評 本題考查有關混合物反應的計算,題目難度中等,注意掌握差量法在計算出的應用,試題培養了學生的分析理解能力及計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 相同溫度下,0.1 mol•L-1NH4Cl溶液比0.1 mol•L-1NH4HSO4溶液含有的[NH4+]更大 | |
| B. | 將0.1 mol•L-1硫酸溶液從常溫加熱至100℃,溶液的pH保持不變 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1,若將含0.5 mol H2SO4的濃溶液與含1 mol NaOH的溶液混合,放出的熱量等于57.3 kJ | |
| D. | 在蒸發皿中加熱蒸發(低于400℃)FeCl3溶液,可以得到FeCl3固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水的電子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 乙烷的結構簡式:C2H6 | |
| C. | 鋁的原子結構示意圖: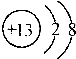 | |
| D. | 硫酸鈉的電離方程式:Na2SO4═2Na++SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
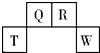 短周期元素T、Q、R、W在元素周期表中的位置如圖所示,其中T所處的周期序數與主族族序數相等.它們的最高價氧化物的水化物依次為甲、乙、丙、丁.下列敘述不正確的是( )
短周期元素T、Q、R、W在元素周期表中的位置如圖所示,其中T所處的周期序數與主族族序數相等.它們的最高價氧化物的水化物依次為甲、乙、丙、丁.下列敘述不正確的是( )| A. | R的氫化物可以既有極性鍵又有非極性鍵 | |
| B. | 常溫下丁的濃溶液可用T單質所制的容器來盛裝 | |
| C. | 丁的濃溶液與Q的單質加熱發生反應,可生成體積比為1:2的兩種氣體 | |
| D. | 甲、乙、丙、丁受熱均易分解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧燃電池在堿性介質中負極的反應式是:O2+2H2O+4e-=4OH- | |
| B. | NaHCO3在水溶液中的水解離子方程式:HCO3-+H2O?CO2↑+OH- | |
| C. | 用FeS為沉淀劑除去廢水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+ (aq) | |
| D. | 鋼鐵發生電化學腐蝕的正極反應式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
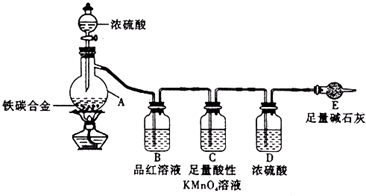
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
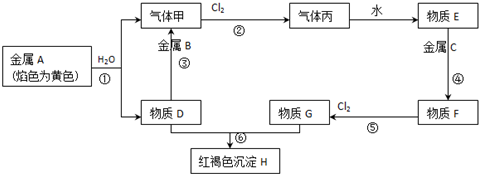
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com