
【題目】3,5-二甲氧基苯酚是重要的有機合成中間體,可用于天然物質白檸檬素的合成。一種以間苯三酚為原料的合成反應如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性質見下表:
物質 | 沸點/℃ | 熔點/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33-36 |
| 易溶于甲醇、乙醚,微溶于水 |
反應結束后,先分離出甲醇,再加入乙醚進行萃取。
(1)①分離出甲醇的操作是的 。
②萃取用到的分液漏斗使用前需 并洗凈,分液時有機層在分液漏斗的 填(“上”或“下”)層。
(2)分離得到的有機層依次用飽和NaHCO3溶液、飽和食鹽水、少量蒸餾水進行洗滌。用飽和NaHCO3 溶液洗滌的目的是 ;用飽和食鹽水洗滌的目的是 。
(3)洗滌完成后,通過以下操作分離、提純產物,正確的操作順序是 (填字母)。
a.蒸餾除去乙醚 b.重結晶 c.過濾除去干燥劑 d.加入無水CaCl2干燥
【答案】(1)①蒸餾 ②檢查是否漏水 上
(2)除去HCl 除去少量NaHCO3 且減少產物損失
(3)dcab
【解析】
試題分析:(1)間苯三酚、3,5-二甲氧基苯酚、甲醇的沸點不同,①分離出甲醇的操作是的蒸餾;②萃取用到的分液漏斗使用前需檢查是否漏水并洗凈,有機物的密度小于水,分液時有機層在分液漏斗的上層。
(2)分離得到的有機層依次用飽和NaHCO3溶液、飽和食鹽水、少量蒸餾水進行洗滌。用飽和NaHCO3 溶液洗滌的目的是除去HCl;用飽和食鹽水洗滌的目的是除去少量NaHCO3,且減少產物損失;(3)洗滌完成后,通過以下操作分離、提純產物,正確的操作順序是加入無水CaCl2干燥、過濾除去干燥劑、蒸餾除去乙醚、重結晶。


科目:高中化學 來源: 題型:
【題目】某探究小組設計如圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗。查閱資料,有關信息如下:

①制備反應原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能發生的副反應:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相關物質的相對分子質量及部分物理性質:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相對分子質量 | 46 | 147.5 | 163.5 | 64.5 |
熔點/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸點/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 與水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)儀器A中發生反應的化學方程式為____________。
(2)裝置B中的試劑是____________,若撤去裝置B,可能導致裝置D中副產物____________(填化學式)的量增加;裝置D可采用____________加熱的方法以控制反應溫度在70℃左右。
(3)裝置中球形冷凝管的作用為____________,寫出E中所有可能發生的無機反應的離子方程式____________。
(4)反應結束后,有人提出先將D中的混合物冷卻到室溫,再用過濾的方法分離出CCl3COOH。你認為此方案是否可行____________。
(5)測定產品純度:稱取產品0.40g配成待測溶液,加入0.1000molL-1碘標準溶液20.00mL,再加入適量Na2CO3溶液,反應完全后,加鹽酸調節溶液的pH,立即用0.02000molL-1Na2S2O3溶液滴定至終點。進行三次平行實驗,測得消耗Na2S2O溶液20.00mL。則產品的純度為____________(計算結果保留三位有效數字)。
滴定的反應原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)為證明三氯乙酸的酸性比乙酸強,某學習小組的同學設計了以下三種方案,你認為能夠達到實驗目的是____________
a.分別測定0.1molL-1兩種酸溶液的pH,三氯乙酸的pH較小
b.用儀器測量濃度均為0.1molL-1的三氯乙酸和乙酸溶液的導電性,測得乙酸溶液的導電性弱
c.測定等物質的量濃度的兩種酸的鈉鹽溶液的pH,乙酸鈉溶液的pH較大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把下列物質分別加入盛冷水的錐形瓶內,立即塞緊帶U形管的塞子。已知U形管內預先裝有少量水且液面相平(為便于觀察,預先染成紅色),加入下列
哪些物質后,發生如圖變化( )

①NaOH粉末;②濃硫酸;③硝酸銨晶體;④過氧化鈉固體;⑤生石灰
A.①②④⑤ B.①②③ C.②③⑤ D.③④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【加試題】甲醇又稱“木醇”或“木精”,沸點64.7℃,是無色有酒精氣味易揮發的液體.甲醇有毒,誤飲5~10mL能雙目失明,大量飲用會導致死亡.甲醇是重要的化學工業基礎原料和液體燃料,可用于制造甲醛和農藥,并常用作有機物的萃取劑和酒精的變性劑等。
(1)工業上可利用CO2和H2生產甲醇,方程式如下:
CO2(g)+3H2(g)![]() CH3OH(l)+H2O(g) △H=Q1kJmol﹣1
CH3OH(l)+H2O(g) △H=Q1kJmol﹣1
又查資料得知:①CH3OH(l)+1/2O2(g)![]() CO2(g)+2H2(g) △H=Q2kJmol﹣1
CO2(g)+2H2(g) △H=Q2kJmol﹣1
②H2O(g)=H2O(l)△H=Q3kJmol﹣1,則表示甲醇的燃燒熱的熱化學方程式為 。
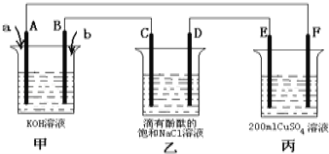
(2)甲醇燃料電池是符合綠色化學理念的新型燃料電池,下圖是以甲醇燃料電池(甲池)為電源的電解裝置.已知:A、B、C、D、E、F都是惰性電極,丙中為0.1mol/L CuSO4溶液 (假設反應前后溶液體積不變),當向甲池通入氣體a和b時,D極附近呈紅色.回答下列問題:
①a物質是 ,A電極的電極反應式為 。
②乙裝置中的總化學反應方程式為 。
③當乙裝置中C電極收集到224mL(標況下)氣體時,丙中溶液的pH= 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將甲烷設計成燃料電池,其利用率更高,如圖所示(A, B為多孔性碳棒)。持續通入甲烷,在標準狀況下,消耗甲烷體積VL,則下列說法錯誤的是()

A.通入CH4的一端為原電池的負極,溶液中OH-向負極區移動
B.當0<V ≤22.4L時,電池總反應式為CH4+2O2+2KOH=K2CO3+3H2O
C.當22.4L<V≤44.8L時,負極電極反應為CH4-8e-+9CO32-+3H2O=10HCO3-
D.當V=33.6L時,溶液中陰離子濃度大小關系為c(CO32-)>c(HCO3-)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A由碳、氫、氧三種元素組成。現取3g A與4.48L氧氣(標準狀況)在密閉容器中燃燒,燃燒后生成二氧化碳、一氧化碳和水蒸氣(假設反應物沒有剩余)。將反應生成的氣體依次通過濃硫酸和堿石灰,濃硫酸增重3.6g,堿石灰增重4.4g。回答下列問題:
(1)3gA中所含氫原子、碳原子的物質的量各是多少?
(2)通過計算確定該有機物的分子式。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙炔是一種重要的有機化工原料,以乙炔為原料在不同的反應條件下可以轉化成以下化合物。完成下列各題:

(1)正四面體烷的二氯取代產物有________種。
(2)關于乙烯基乙炔分子的說法正確的是________。
A.能使酸性KMnO4溶液褪色
B.1摩爾乙烯基乙炔能與3摩爾Br2發生加成反應
C.乙烯基乙炔分子內含有兩種官能團
D.等質量的乙炔與乙烯基乙炔完全燃燒時的耗氧量不相同
(3)寫出與環辛四烯互為同分異構體且屬于芳香烴的分子發生加聚反應的化學方程式
(4)寫出與苯互為同系物且一氯取代產物只有兩種的物質的結構簡式(舉兩例):__________________、__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常用于制備食品香料的有機化合物A,其相對分子質量為120,A燃燒只生成二氧化碳和水。A既可以與乙醇發生酯化反應,又可以與乙酸發生酯化反應,且測得A與乙醇完全酯化所得有機產物B的相對分子質量為176。請回答下列問題:
(1)A的分子式為 。
(2)B的結構簡式 。
(3)A與乙酸發生酯化反應的化學方程式 。
(4)由丙烯經過六個步驟可以合成有機化合物A,流程如下:
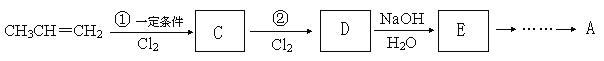
若C的分子式為C3H5Cl,D的分子式為C3H5Cl3,則①的反應類型為 。
D→E反應的化學方程式為 。
請補充完成E→A的反應流程 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】BPA的結構簡式如右下圖所示,常用來生產防碎塑料聚碳酸酯。

(1)該物質的分子式為___________,含氧官能團的名稱是_________,屬于____類。
(2)該物質最多_____個碳原子共面。
(3)充分燃燒0.1mol該有機物,消耗的O2在標準狀況下的體積為_________。
(4)下列關于BPA的敘述中,不正確的是_______。
A.可以發生還原反應
B.遇FeCl3溶液紫色
C.1mol該有機物最多可與2molH2反應
D.可與NaOH溶液反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com